badania analityczne i farmaceutyczne
widma absorpcji
spektrum absorpcji tiaminy zarejestrowano w stosunku do wody (Fig.1), stwierdzono, że tiamina wykazuje maksymalny szczyt absorpcji (λ max) przy 235 nm. Ze względu na silnie przesunięte na niebiesko λ max tiaminy, jej oznaczanie w postaci dawkowania oparte na bezpośrednim pomiarze jej absorpcji dla ultrafioletu jest podatne na potencjalne zakłócenia ze strony wspólnych zaróbek. Dlatego derywatyzacja tiaminy w celu osiągnięcia widocznych gatunków absorbujących zasięg była niewątpliwie konieczna. W ten sposób przeprowadzono derywatyzację tiaminy za pomocą NBD-Cl i zarejestrowano spektrum absorpcji produktu w stosunku do ślepej próby odczynnika (Fig.1). Stwierdzono, że produkt jest koloru brązowego wykazujący λmax przy 434 nm, a λmax NBD-Cl wynosił 342 nm. Λmax pochodnej tiaminy-NBD-Cl był przesunięty ku czerwieni, eliminując wszelkie potencjalne zakłócenia. Długość fali 434 nm została więc ustalona jako optymalna.
optymalizacja warunków reakcji
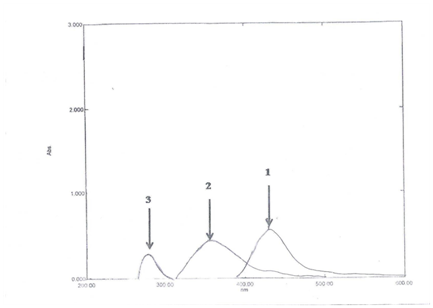
Rysunek 1: widma absorpcji tiaminy (3), NBD-Cl (2) i kompleksu między nimi (1).
optymalne warunki dla opracowanej metody zostały ustalone poprzez zmianę parametrów jeden po drugim, przy zachowaniu pozostałych parametrów na stałym poziomie i zgodnie z wpływem wywieranym na absorbancję barwnego produktu. W celu ustalenia warunków eksperymentalnych badano wpływ różnych parametrów, takich jak pH, czas, objętość bufora i stężenie NBD-Cl.
wpływ pH
wpływ pH na reakcję między tiaminą i NBD-Cl badano zmieniając postać pH 7,0 do 12,0. Jak pokazano na fig. 2, absorbancja produktu jest niska przy pH 7,0, co wskazuje, że tiamina nie może reagować z (NBD-Cl) w neutralnych mediach. Wynikało to prawdopodobnie z istnienia grupy aminowej tiaminy w postaci soli chlorowodorkowej, która hamuje zdolność substytucji nukleofilowej. Gdy pH wzrosło z 7 do 12, odczyty gwałtownie wzrosły, uwalniając grupę aminową tiaminy i ułatwiając podstawienie nukleofilowe. Maksymalna absorpcja została osiągnięta przy wartości pH 10,5. Przy wartościach pH większych niż 10,5 nastąpiło zmniejszenie wchłaniania. Wiązało się to prawdopodobnie ze wzrostem ilości jonu wodorotlenkowego, który zwiększa szybkość reakcji wstecznej tiaminy z NBD-Cl.
wpływ czasu reakcji
absorbancja produktu reakcji była monitorowana w różnym czasie (ryc. 3). Zachowując inne warunki nienaruszone, absorbancję produktu reakcji następowała po odstawieniu przez różne rozpiętości czasowe w temperaturze 25°C. Wyniki pokazują, że tiamina reaguje z NBD-Cl w temperaturze 25 ° C, a absorbancja zaczyna stopniowo wzrastać i osiąga maksimum po 25 minutach. W przypadku dłuższych czasów reakcji zaobserwowano niewielki spadek absorbancji. Odpowiednio ustalono 25min jako dogodny czas reakcji do oznaczenia.
wpływ ilości buforu
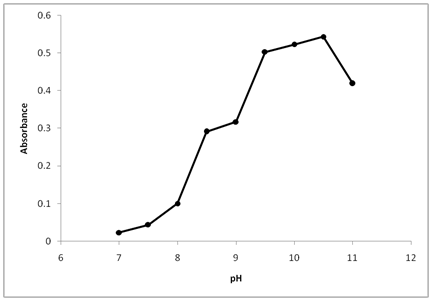
Rysunek 2: Wpływ pH na reakcję tiaminy z NBD-Cl.
tiamina (20µg/ml): 1 ml, NBD-Cl conc. 0,2% (w / v), Czas reakcji 20 min.
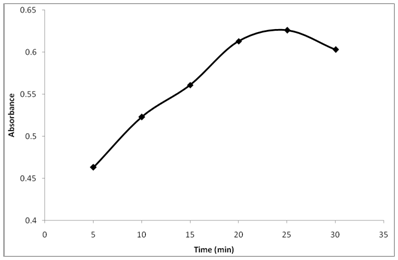
Rysunek 3: Wpływ czasu reakcji na reakcję tiaminy z NBD-Cl.
tiamina (20 µg/ml): 1 ml, Bufor (pH 10.5): 1,5 ml, NBD-CL conc. 0, 2% (w/v).
utrzymując pH na poziomie 10,5 badano również wpływ ilości roztworu buforowego na absorbancję produktu reakcji (Fig.4). Rysunek pokazuje, że absorbancja produktu reakcji zwiększa się szybko wraz ze wzrostem ilości roztworu buforowego i staje się maksymalna, gdy ilość roztworu buforowego osiągnie 1,5 mL. Dlatego tak dobrano ilość 1,5 mL roztworu buforowego, aby zapewnić najwyższą absorbancję.
wpływ stężenia NBD-Cl
badanie wpływu stężeń NBD-Cl wykazało, że reakcja była zależna od stężenia odczynnika. Największą intensywność absorpcji uzyskano przy stężeniu NBD-Cl wynoszącym 0,2% (w / v), A wyższe stężenie NBD-Cl prowadzi do zmniejszenia absorbancji (ryc. 5).
z powyższych eksperymentów dostosowujących parametry optymalnymi warunkami zastosowanymi do oznaczenia były: pH 10,5, stężenie NBD-Cl 0,2% (w/v), objętość buforu 1,5 mL, Czas reakcji 25min i temperatura 25ºC.
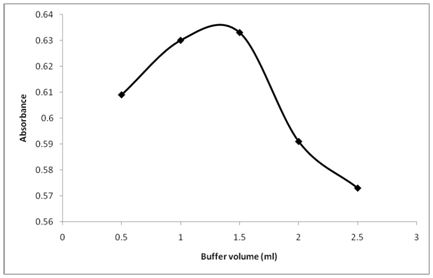
Rysunek 4: wpływ ilości buforu (ml) na reakcję tiaminy z NBD-Cl.
tiamina (20µg/ml): 1 ml, pH buforu: 10,5, NBD-CL conc. 0,2% (w / v), Czas reakcji 25 min.
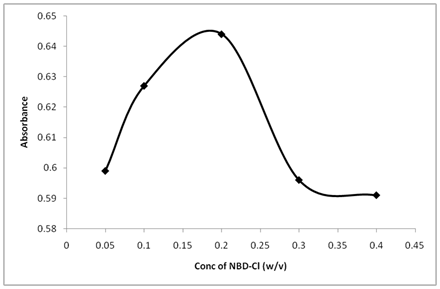
Rysunek 5: wpływ stężenia NBD-Cl na jego reakcję z tiaminą.
tiamina (20µg/ml): 1 ml, Bufor (pH 10,5): 1,5 ml, Czas reakcji 25 min.
Walidacja metody
metoda została zwalidowana dla następujących parametrów: specyficzność, liniowość, precyzja, dokładność, granica wykrywalności (LOD), granica ilościowości (LOQ) i wytrzymałość zgodnie z wytycznymi Międzynarodowej Konferencji harmonizacji (ICH).
Liniowość, granica wykrywalności (LOD) granica oznaczalności (LOQ)
liniowość oceniano za pomocą analizy regresji liniowej wyznaczonej przez konstruowanie siedmiu stężeń tiaminy w zakresie 05–35µg/mL, które obliczono metodą regresji najmniejszej kwadratowej w celu obliczenia równania kalibracyjnego i współczynnika korelacji. Krzywe kalibracji zostały skonstruowane przez wykreślenie stężenia w stosunku do absorbancji, przy użyciu analizy regresji liniowej. Równanie regresji dla wyników wynosiło A = 0,033 x-0,009 (r2=0,999), gdzie A jest absorbancją przy 434 nm, x jest stężeniem tiaminy w µg/mL w zakresie 05-35 µg/mL, A r jest współczynnikiem korelacji (Tabela 1). Stwierdzono, że liniowy zakres stężeń jest porównywalny z naszą poprzednią metodą wykorzystującą NQS . Granicę wykrywalności (LOD) i granicę oznaczalności (LOQ) wyznaczono według następującego wzoru LOD=3.3×SDa / b i LOQ=10×SDA / B, SDa jest odchyleniem standardowym punktu przecięcia; B jest nachyleniem zgodnie z wytycznymi ICH . Stwierdzono, że Lod i LOQ wynosiły odpowiednio 0,667 i 2,020 µg/mL (Tabela 1).
|
parametr |
wartość |
|
długość fali pomiarowej (nm) |
|
|
zakres liniowy (µg/ml) |
|
|
równanie regresji |
y = 0,033 x – 0.009 |
|
Intercept |
|
|
Standard deviation of intercept |
|
|
Slope |
|
|
Standard deviation of slope |
|
|
Correlation coefficient (r2) |
|
|
Limit of detection, LOD (μg/mL) |
|
|
Limit of quant., LOQ (μg/mL) |
Table 1: Parameters for the performance of the proposed method.
dokładność
dokładność proponowanej metody przeprowadzono stosując 3 różne stężenia 10, 20 i 30 µg / mL leku tiaminy w zakresie liniowym obliczonym jako procent leku odzyskanego z próbek (Tabela 2).
|
Sample No |
Sample Content (µg/mL) |
Thiamine Standard Amount (µg/mL) |
Amount Found (Total) (µg/ml) |
Recovery + SD* |
|
96.29+0.015 |
||||
|
98.90+0.018 |
||||
|
101.47+0.148 |
Table 2: Badania odzysku w celu określenia tiaminy za pomocą proponowanej metody.
*wartości są średnią z trzech oznaczeń.
błąd względny (RE) wynosił w granicach 0,24%, a odpowiednie odchylenie standardowe w granicach 0,004 dla trzech różnych oznaczeń (Tabela 3).
|
Sample No |
Concentration (μg/mL) |
Concentration |
Recovery (% + SD) |
Relative Error (%) |
|
95.5±0.004 |
||||
|
96.46±0.002 |
||||
|
97.50±0.003 |
tabela 3: ocena dokładności i precyzji.
mechanizm reakcji: donoszono, że NBD-Cl reaguje z grupą aminową pierwszorzędowych lub drugorzędowych pochodnych Amin . Podobnie grupa aminowa tiaminy może działać jako nukleofil ze względu na samotną parę elektronów na atomie azotu, tendencyjnie atakując centrum z niedoborem elektronów w NBD-Cl (Tabela 4 & Rysunek 6). Jednocześnie udowodniono, że skład produktu wynosi 1:1 tiaminy i NBD-Cl (ryc. 7). Stwierdzono więc, że grupa aminowa tiaminy reaguje z NBD-Cl, tworząc brązowy addukt. Równanie reakcji przedstawiono na fig. 7.

Rysunek 6: The Job’s method plot for the stoichiometry of the reaction of Thiamine with NBD-Cl Vr: Volume of NBD-Cl (7.5×10-4 mol/L), Vt: Volume of Thiamine (7.5×10-4 mol/L), Vr + Vt=10 ml.
|
Parameter |
Recovery (% ± SD) |
|
Recommended condition |
97.50±0.003 |
|
NBD-Cl concentration (0.22%) |
98.75±0.002 |
|
NBD-Cl concentration (0.180%) |
96.76%±0, 003 |
|
PH bufora(10, 7) |
96, 90±0, 002 |
|
Ph bufora(10, 3) |
95, 79±0, 22 |
|
czas reakcji min (23) |
96, 09±0, 009 |
|
czas reakcji min (27) |
98, 01±0, 003 |
Tabela 4: wpływ niewielkich zmian w warunkach badania na wydajność analityczną proponowanej metody spektrofotometrycznej oznaczania tiaminy przy użyciu odczynnika NBD-CL.
zastosowanie proponowanej metody do analizy postaci dawkowania tiaminy
tabletki tiaminy zostały poddane analizie za pomocą proponowanej i oświadczenie na etykiecie zgadza się dobrze z naszą nową metodą pokazaną w tabeli 5. Proponowana metoda ma tę zaletę, że jest praktycznie wolna od zakłóceń przez substancje pomocnicze.
|
Brand Name of Label Claim (Mg) |
Amount Found (Mg) |
(% Found ± SD)a |
|
Thiamine tablets (100 mg) |
99.9±0.025 |
Table 5: Analysis of Thiamine-containing dosage form by the proposed method.
a: values are mean of five determinations.
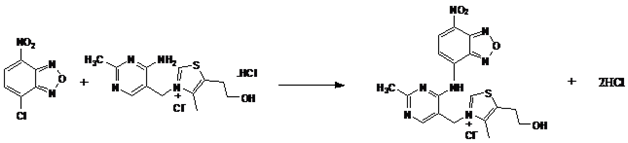
Figure 7: Reakcja tiaminy z NBD-Cl pokazująca stechiometrię 1:1.
Leave a Reply