VSEPR 2
de inhoud die volgt is de inhoud van de Algemene Scheikunde Lecture 34. In deze lezing gaan we verder met de bespreking van VSEPR met die atomen die het octet kunnen overschrijden.
wanneer een element zich in of voorbij de derde periode in het periodiek systeem bevindt, heeft het de mogelijkheid om de octetregel te overschrijden, wat betekent dat het meer dan 4 bindingen met andere atomen kan maken. In VSEPR zijn er twee structuren die we moeten weten die in deze categorie vallen: AX5 en AX6.
AX5
net Als met eerdere modellen is de uitgebreide octet modellen beginnen met obligaties op alle punten rond het centrale atoom:
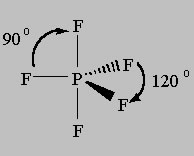
De EPG en MG voor dit model heet Trigonale Bipyramidal omdat het tekenen van de lijn van de axiale (omhoog-omlaag) atomen en de equatoriale (ongeveer in het midden) atomen toont twee 3 piramiden:
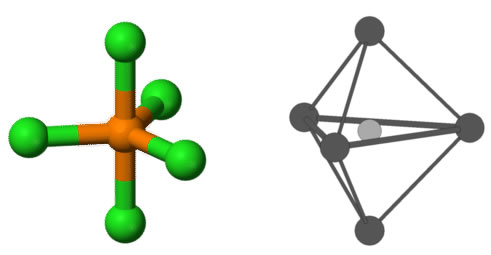
Vanaf hier, als we beginnen te verwijderen obligaties en vervang ze met eenzame paren, de EPG blijft constant met de 5 regio ‘ s van het elektron dichtheid, maar de moleculaire geometrie verandert. Studies werden gedaan om te bepalen waar het eerste atoom zou worden verwijderd en er werd vastgesteld dat de structuur zou het meest energetisch gunstig verliezen van een Equatoriaal atoom eerste, tweede en dan derde.
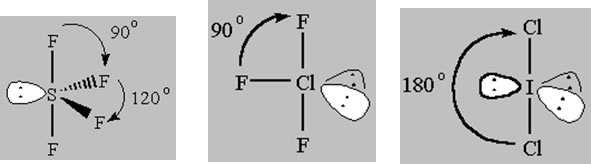
See-Saw MG (AX4E), T-vormige MG (AX3E2)en vervolgens lineair (AX2E3)
AX6
voor de laatste van de VSEPR modellen zullen we kijken naar 6 perifere atomen die aan het centrale atoom zijn gekoppeld.
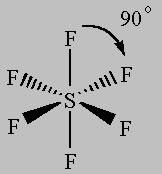
de tekening van de posities van de atomen in deze opstelling lijkt op het Cartesiaanse coördinatenstelsel:
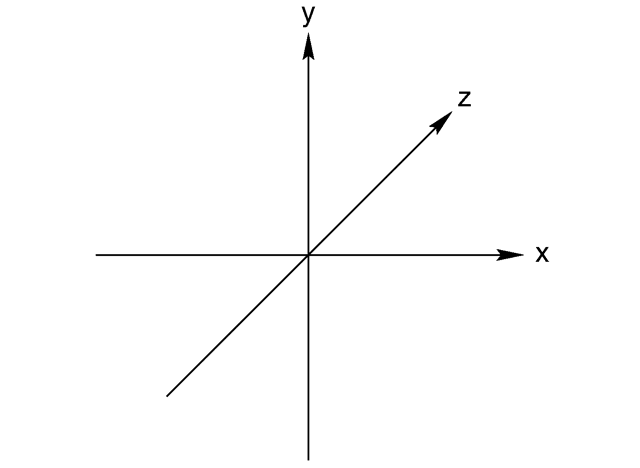
met de randatomen aan het einde van elke as.
net als bij de vorige modellen worden de EPG en MG hetzelfde genoemd wanneer alle 6 atomen aan het centrale atoom gebonden zijn. In dit geval wordt de structuur Octaëdraal (8 zijden) genoemd.
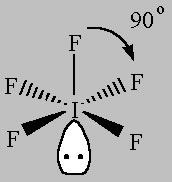
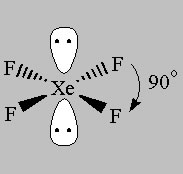
wanneer u atomen verwijdert en eenzame paren achterlaat, verschijnen de volgende structuren:
 |
 |
|
Square Pyramidal (AX5E)
|
Square Planar (AX4E2)
|
Leave a Reply