Servier-Flebolymphology
Download this issue Back to summary
update en huidige
aanbevelingen
Bourgoin-Jallieu, Frankrijk
Abstract
aanvankelijk werd oppervlakkige veneuze trombose (SVT) beschouwd als een goedaardige ziekte of een veel voorkomende complicatie van spataderen. Recente studies hebben de mogelijke ernst van SVT aangetoond en de plaats ervan binnen de veneuze trombo-embolische (VTE) ziekten, samen met diepe veneuze trombose (DVT) en longembolie (PE) gedefinieerd. Een gelijktijdige DVT werd vastgesteld bij 25% tot 30% van de patiënten bij presentatie en een PE bij 4% tot 7% van de patiënten. Daaropvolgende VTE werd gemeld bij 3 tot 20% van de patiënten, afhankelijk van de follow-up duur. Tot voor kort zijn talrijke antistollingsstrategieën getest, zonder duidelijk aangetoond klinisch voordeel. Echter, de recente CALISTO studie (vergelijking van Arixtra bij oppervlakkige veneuze trombose in de onderste ledematen met placebo) bevestigde een anticoagulans therapie protocol gebaseerd op fondaparinux, 2,5 mg per dag gedurende 45 dagen, resulterend in bijgewerkte aanbevelingen voor de behandeling van SVT. Dit artikel zal een update presenteren over het beheer van onderbeen SVT en de huidige aanbevelingen en richtsnoeren. In het kort moeten alle patiënten met SVT een bilaterale duplex-scan ondergaan om de diagnose SVT te bevestigen, de precieze locatie en omvang van de SVT te bepalen en de aanwezigheid van DVT te diagnosticeren of uit te sluiten. Bij patiënten met symptomatische SVT met een lengte van ten minste 5 cm wordt aanbevolen een profylactische dosis fondaparinux of laagmoleculair heparine voor te schrijven gedurende 45 dagen zonder anticoagulatie (graad 2B), en wanneer de kosten van de behandeling met fondaparinux aanvaardbaar zijn, wordt aanbevolen fondaparinux 2,5 mg per dag te gebruiken vs laagmoleculair heparine (graad 2C). Echter, de aanbevelingen en richtlijnen hebben toegewezen deze behandelingen met een lage graad, en vragen blijven over SVT management. Enkele risicofactoren voor het later ontwikkelen van een VTE zijn geïdentificeerd, maar verder onderzoek is nodig om subgroepen van patiënten met een hogere incidentie van een VTE na een SVT te definiëren.
Inleiding
oppervlakkige veneuze trombose (SVT) wordt beschouwd als een goedaardige ziekte of een veel voorkomende complicatie van spataderen; recente studies hebben echter de mogelijke ernst ervan aangetoond en hun plaats binnen de veneuze trombo-embolische (VTE) ziekten, samen met diepe veneuze trombose (DVT) en longembolie (PE) gedefinieerd.
antistollingstherapie wordt tegenwoordig veel gebruikt in plaats van niet-steroïdale anti-inflammatoire geneesmiddelen (NSAID ‘ s), die tot het laatste decennium algemeen werden gebruikt. Een recente studie heeft voor het eerst een therapeutisch protocol gevalideerd.1 Er blijven echter vragen over de behandeling van SVT: (i) is antistollingstherapie vereist voor de behandeling van alle patiënten met SVT in de onderste ledematen?; (ii) moeten profylactische of therapeutische doses worden gebruikt?; (iii) Wat is de aanbevolen behandelingsduur?; (iv) moet de behandeling hetzelfde zijn voor SVT die voorkomt in spataderen en niet-spataderen?; (v) kunnen de risicofactoren voor VTE-complicaties na SVT worden voorspeld?; en (vi) is chirurgie nog steeds aangewezen voor de behandeling van een acute SVT?
in dit artikel worden de beweegredenen voor de actualisering voor het beheer van SVT ‘ s van de legs en de huidige aanbevelingen en richtsnoeren uiteengezet.
incidentie van oppervlakkige veneuze trombose van de onderste ledematen
SVT wordt als een veel voorkomende ziekte beschouwd, maar de werkelijke incidentie in de volwassen populatie blijft onbekend. Een recente studie,uitgevoerd in Frankrijk 2, toonde aan dat het jaarlijkse diagnosecijfer 0,6% bedroeg. Het was hoger bij vrouwen en nam toe met de gevorderde leeftijd, ongeacht het geslacht. Verrassend genoeg was het jaarlijkse diagnosecijfer van SVT lager dan verwacht en lager dan het jaarlijkse diagnosecijfer van DVT (ongeveer de helft van dat van DVT). Volgens een andere Franse studie, die met vergelijkbare methoden werd uitgevoerd, was de jaarlijkse incidentie van DVT en PE in de onderste ledematen respectievelijk 1,24% en 0,6%.3
oppervlakkige veneuze trombose met gelijktijdige diepe veneuze trombose bij presentatie
The POST (prospectieve observationele oppervlakkige tromboflebitis) en OPTIMEV studies (OPTimisation de l ‘interrogatoire dans l’ évaluation du risque trombo – Embolique Veineux), twee grote observationele en epidemiologische studies, onlangs gepubliceerde essentiële gegevens over SVT.4,5 in totaal werden 844 patiënten met SVT van de benen geanalyseerd in het POST-onderzoek, 4 en een DVT of PE werd geïdentificeerd bij 25% van de patiënten met SVT bij presentatie en een proximale DVT werd gediagnosticeerd bij 9,7% van de patiënten. We moeten benadrukken dat DVT niet aan SVT grenst bij 41,9% van de patiënten met DVT. In totaal werden 788 patiënten met SVT opgenomen in het OPTMEV-onderzoek5,waarbij een SVT geassocieerd werd met een DVT bij inclusie bij 29% van de patiënten, waarbij distale DVT optrad bij 59,5% van deze patiënten (128/215; de exacte locatie van DVT ontbrak bij 12 patiënten).
deze gegevens bevestigen eerdere onderzoeken die aantonen dat DVT geassocieerd was met SVT bij 23% tot 36% van de patiënten en tonen samenhang tussen de verschillende onderzoeken (tabel I).2,4-10
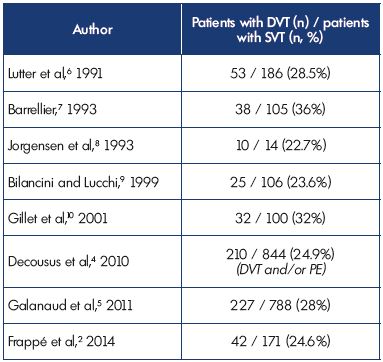
tabel I. oppervlakkige veneuze trombose met gelijktijdige diepe veneuze trombose bij presentatie.
Afkortingen: DVT, diepe veneuze trombose; PE, longembolie; SVT,
oppervlakkige veneuze trombose.
oppervlakkige veneuze trombose geassocieerd met longembolie bij presentatie
bij inclusie werd symptomatische PE gediagnosticeerd bij 3,9% en 6.9% van de patiënten in respectievelijk de POST-en OPTIMEV-onderzoeken. SVT met PE, maar zonder DVT, was echter slechts goed voor 2,2% van alle SVT met DVT of PE. Deze gegevens bevestigen de bevindingen van eerdere studies (tabel II).2,4-7,9,10
in de praktijk is een dubbelzijdig scanonderzoek verplicht bij patiënten met SVT om de diagnose te bevestigen (figuur 1), De precieze locatie en omvang van de SVT te bepalen en de aanwezigheid van DVT te diagnosticeren of uit te sluiten.
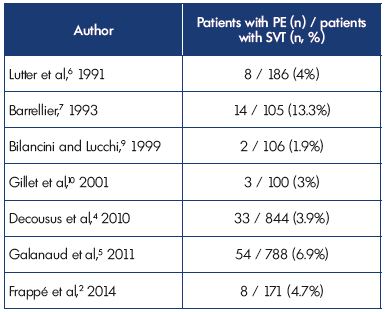
tabel II. oppervlakkige veneuze trombose met gelijktijdige longembolie bij presentatie.
Afkortingen: PE, longembolie; SVT, oppervlakkige veneuze trombose.
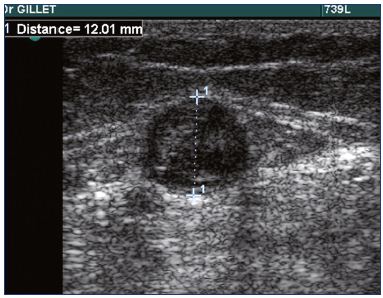
figuur 1. Echografie van trombose van de kleine sapheneuze ader.

resultaat en veneuze trombo-embolische recidief
in de literatuur varieert het percentage trombo-embolische recidieven van 3% tot 20%, afhankelijk van de duur van de follow-up. In een persoonlijk onderzoek 13 meldden we het optreden van symptomatische VTE ‘ s bij 16,4% van de patiënten met geïsoleerde SVT, met een gemiddelde follow-up van 14,5 maanden. De VTE-voorvallen omvatten DVT( 31%), PE (6%), een andere SVT in een ander sapheneus systeem (37,5%) en een terugkerende SVT in hetzelfde sapheneus systeem (25%).
in het POST-onderzoek, 4 8.3% van de patiënten met een geïsoleerde SVT bij inclusie ontwikkelde ten minste 1 symptomatische VTE-gebeurtenis na 3 maanden (symptomatische DVT, 2,8%; symptomatische PE, 0,5%; symptomatische verlenging van SVT, 3,3%; en symptomatische recidief van SVT, 1,9%). In het OPTIMEV-onderzoek ontwikkelden 5 3% van de patiënten met een geïsoleerde SVT en 5,4% van de patiënten met een SVT geassocieerd met DVT bij presentatie een VTE na 3 maanden; het percentage VTE ‘ s was 12,5% bij de 3-jarige follow-up. In het onderzoek met Dewar en Panpher 14 trad een symptomatische DVT op bij 4% van de patiënten met een geïsoleerde SVT bij een follow-up van 6 maanden.
deze epidemiologische bevindingen tonen de mogelijke ernst van SVT aan. Ze moeten niet langer worden beschouwd als een goedaardige aandoening. Bijgevolg is hun plaats nu duidelijk gedefinieerd binnen de VTE-ziekten.
risicofactoren voor het ontwikkelen van een trombo-embolische gebeurtenis
een multivariate analyse van de POST-studie4 identificeerde mannelijk geslacht, voorgeschiedenis van DVT of PE, eerdere kanker en geen spataderen als risicofactoren voor een symptomatische VTE na 3 Maanden, Inclusief recidief of verlenging van de SVT. In het STENOX-onderzoek (oppervlakkige tromboflebitis behandeld met enoxaparine) werden 15 voorgeschiedenis van een VTE (DVT of PE), mannelijk geslacht en ernstige chronische veneuze insufficiëntie geïdentificeerd als onafhankelijke voorspellende factoren voor een VTE na 3 maanden. Alleen ernstige chronische veneuze insufficiëntie was een onafhankelijke voorspellende factor voor DVT of PE. In een gepoolde analyse van de POST-en OPTIMEV-studies toonden 16 Galanaud et al aan dat mannelijk geslacht,kanker, persoonlijke voorgeschiedenis van VTE en saphenofemorale of saphenopopliteale betrokkenheid het risico op een volgende VTE of DVT/ PE in een univariate analyse significant verhoogde. In multivariate analyses verhoogde alleen het mannelijk geslacht significant het risico op een volgende recidief van VTE of DVT/PE. Voor kanker en een persoonlijke voorgeschiedenis van VTE lagen de aangepaste hazard ratio ‘ s slechts iets onder het niveau van statistische significantie (P=0,06 voor beide), wat erop wijst dat Voor deze factoren het onderzoek slechts onvoldoende statistisch vermogen had.
in het STEFLUX-onderzoek (Superficial trombo-embolie FLUXum) werden 17 met een body mass index (BMI) tussen 25 en 30 kg/m2 en een samenstelling van een eerdere SVT en/of VTE en/of familiegeschiedenis van VTE geïdentificeerd als significante onafhankelijke risicofactoren voor een VTE-gebeurtenis (samengesteld uit symptomatische en asymptomatische DVT,PE en SVT recidief of extensie).
Vein status
spatader status is gemeld om het risico van het vertonen van DVT bij presentatie te beïnvloeden. In de POST4-en OPTIMEV-onderzoeken werden 5 SVT ’s die in een niet–spataderen (NVV-SVT) optraden vaker geassocieerd met een gelijktijdige DVT of PE dan SVT’ s die in een spataderen (VV-SVT) optraden. Soortgelijke bevindingen werden gemeld door Gorty et al.18
tijdens de follow-up van 3 maanden in het OPTIMEV-onderzoek werd geïsoleerde NVV-SVT niet geassocieerd met een hoger risico op bijwerkingen (dat wil zeggen overlijden, recidief van VTE en bloeding). Geïsoleerde NVV-SVT had een hoger verband met symptomatische DVT-of PE-recidief (2,7% Versus 0,6%), maar dit resultaat bereikte geen statistische significantie (P=0,07).
in het POST-onderzoek werd de afwezigheid van spataderen geïdentificeerd als een risicofactor voor de verdere ontwikkeling van een symptomatische VTE bij patiënten met een geïsoleerde symptomatische SVT bij presentatie (P=0,049). In het STEFLUX-onderzoek 17 was de afwezigheid van spataderen een risicofactor voor VTE (P=0,004) nadat de behandeling met laagmoleculaire heparine was gestopt.
In de placebo-groep van de CALISTO onderzoek (Vergelijking van Arixtra in de onderste Ledematen Oppervlakkige veneuze Trombose met placebo),1 trombo-embolische complicaties opgetreden vaker wanneer de SVT betrokken de grote vena saphena magna (GSV), werd uitgebreid tot binnen 10 cm van de saphenofemoral splitsing (SFJ), die betrokken zijn aderen boven de knie, en bij patiënten met een voorgeschiedenis van VTE.
veneuze stase is het primaire mechanisme van SVT bij patiënten met spataderen. Ontsteking kan een essentiële rol spelen bij trombusvorming bij patiënten zonder spataderen; daardoor leidt dit tot een hoger risico op een meer klinisch ernstige trombo-embolie. Screening op trombofilie wordt niet aanbevolen voor de routinematige behandeling van patiënten met NVV-SVT, hoewel gegevens uit de literatuur aantoonden dat trombofilie frequent was in deze situatie. In een persoonlijk prospectief onderzoek 10 identificeerden we trombofilie bij 50% van de patiënten met NVV-SVT, terwijl slechts 15% van de patiënten met VV-SVT trombofilie had. In een andere prospectieve studie onder 42 patiënten met NVV-SVT 19 identificeerden we trombofilie bij 20 (47,6%) patiënten. De meest voorkomende trombofilie was het gevolg van de heterozygote factor V Leiden mutatie. In een onderzoek onder 63 patiënten met geïsoleerde NVV-SVT identificeerden 20 Martinelli et al.trombofilie bij 30% van de patiënten. Screening op trombofilie is aan te raden, na uitsluiting van occulte kanker, vooral bij patiënten met trombusprogressie ondanks een geschikte antistollingstherapie.11,21
behandeling van oppervlakkige veneuze trombose
behandeling van SVT is altijd een controversieel onderwerp geweest. Grote variaties in de behandeling worden gemeld, vooral met betrekking tot antistollingstherapie. De POSTSTUDIE 4,die tussen maart 2005 en oktober 2006 in Frankrijk werd uitgevoerd, leverde interessante informatie op over de behandeling met SVT. In totaal 634 patiënten hadden een geïsoleerde SVT bij inclusie. Informatie over de behandeling die zij gedurende de observatieperiode van 3 maanden kregen, was beschikbaar voor 597 patiënten, waarbij 90,5% van de patiënten één of meer antistollingsmiddelen had gekregen. Van de patiënten die anticoagulantia kregen, kreeg 63% therapeutische doses, 36,7% profylactische doses en 16,8% vitamine K-antagonisten. De behandelingsduur was sterk variabel. In totaal 47.2% van de patiënten kreeg een topische NSAID, 8,2% een orale NSAID en 10% onderging een veneuze operatie (strippen of hoge ligatie).
deze gegevens toonden de noodzaak aan om de rol van antistollingstherapie bij de behandeling van SVT te verduidelijken. Het gebruik van antistollingstherapie bij patiënten met een SVT werd voor het eerst gemeld in 1962 door Zollinger et al.22,nadat het optreden van een PE was waargenomen, die fataal was bij 34 (10,1%) van een reeks van 335 patiënten met een SVT. Hoewel tot voor kort talrijke anticoagulansstrategieën waren getest, waaronder niet-gefractioneerde heparine of heparine met een laag moleculair gewicht, bij profylactische of therapeutische doses gedurende verschillende perioden, had geen enkele daarvan duidelijk enig klinisch voordeel aangetoond.
De STENOX-studie23 was een gerandomiseerd dubbelblind onderzoek met 427 patiënten, waarin laagmoleculaire heparine (enoxaparine in therapeutische en profylactische doses) werd vergeleken met NSAID en placebo. De patiënten werden gedurende 10 dagen behandeld, met een follow-up van 3 maanden. Na 10 dagen waren er meer VTE ‘ s in de placebogroep (P24 vergeleek therapeutische Versus profylactische doses van nodraparine bij 163 patiënten met een geïsoleerde SVT in de GSV, en patiënten werden gedurende 1 maand behandeld. Bij de follow-up van 3 maanden waren de resultaten in beide groepen vergelijkbaar (respectievelijk 7,2% en 8,6% optreden van een VTE; p=0,7), wat geen voordeel van de therapeutische dosering liet zien. Tijdens de follow-up werd een” catch-up “of rebound-fenomeen waargenomen, aangezien veel VTE’ s werden gemeld, vooral bij de groep patiënten die met de therapeutische dosering werden behandeld. Een” catch-up ” – fenomeen werd ook waargenomen na het staken van de behandeling met laagmoleculaire heparine na 1 maand in het STEFLUX-onderzoek.Deze bevindingen pleiten, net als die van de STENOX-studie, voor de keuze van profylactische doses laagmoleculaire heparine in SVT. Het optreden van de meerderheid van de VTE ‘ s gedurende de 2 en 3 maanden na het staken van de behandeling met laagmoleculaire heparine in de groep die therapeutische doses kreeg, benadrukt opnieuw de kwestie van de optimale duur van de antistollingstherapie.
in de gerandomiseerde, dubbelblinde Calisto-studie1 werd fondaparinux 2,5 mg per dag gedurende 45 dagen vergeleken met placebo bij 3002 patiënten met een geïsoleerde symptomatische SVT in de onderste ledematen die ten minste 5 cm lang was. De belangrijkste uitsluitingscriteria waren de behandeling van kanker in de voorafgaande 6 maanden, DVT of PE in de voorafgaande 6 maanden, SVT gelegen binnen 3 cm van de SFJ, en ernstige nierinsufficiëntie (creatinineklaring 26 de 2,5 mg dosis fondaparinux werd gekozen op basis van de gedachte dat een profylactische dosis voldoende zou zijn om patiënten met SVT te behandelen. Bovendien bleek deze dosis werkzamer te zijn voor de preventie van VTE ‘ s na een grote orthopedische ingreep dan een profylactische dosis laagmoleculaire heparine, en even werkzaam als de therapeutische dosis laagmoleculaire heparine bij patiënten met acute coronaire syndromen, wat erop wijst dat 2,5 mg fondaparinux zou overeenkomen met de aanbevelingen van de American College of Chest Physicians (ACCP) uit 200827 die het gebruik van profylactische of intermediaire doses laagmoleculaire heparine voor de behandeling van patiënten met SVT bepleiten. De duur van 45 dagen werd gekozen omdat een behandelingsperiode van 30 dagen of minder te kort zou kunnen zijn, aangezien de meeste symptomatische VTE ‘ s optreden na het staken van de behandeling. Het primaire werkzaamheidsresultaat was een samenstelling van overlijden door welke oorzaak dan ook, een symptomatische PE, een symptomatische DVT, een symptomatische uitbreiding van de SFJ of een symptomatische herhaling van SVT op dag 47. Er was een follow-up periode van 77 dagen voor de patiënten.
het primaire effectiviteitsresultaat kwam voor bij 0,9% van de patiënten in de fondaparinuxgroep en 5.9% in de placebogroep (P28
Het is interessant om de wijziging van de aanbevelingen van de ACCP guidelines van 2008 op te merken.We moeten er echter rekening mee houden dat het aanbevelingen van lage kwaliteit zijn (graad 2B of 2C).
in de update van de Cochrane Database Systematic Review on “Treatment for superficial thromboflebitis of the leg”kwamen 29,30 Di Nisio et al.tot dezelfde conclusies. Deze beoordeling was gebaseerd op de analyse van 30 gerandomiseerde gecontroleerde onderzoeken waarbij 6507 deelnemers met SVT van de benen betrokken waren. De auteurs concluderen dat een profylactische dosis fondaparinux, toegediend gedurende 6 weken, een geldige therapeutische optie lijkt te zijn voor SVT van de benen. Het bewijs van orale behandelingen, topische behandeling of chirurgie is te beperkt en geeft geen informatie voor gebruik in de klinische praktijk over de effecten van deze behandelingen in termen van VTE-en SVT-progressie.
chirurgie versus antistollingstherapie
een overzicht van studies waarin chirurgie en antistollingstherapie worden vergeleken, toont geen enkel voordeel voor chirurgische behandeling. De percentages van SVT-progressie waren vergelijkbaar, terwijl de incidentie van VTE en complicaties hoger waren bij een operatie.Lozano et al. vertoonden gedurende 4 weken geen verschil tussen chirurgie en enoxaparine.32
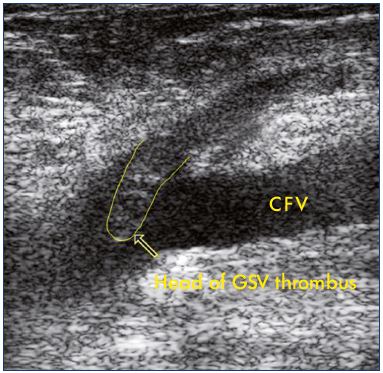
Figuur 2. Echografie van een uitbreiding van een trombose van de grote sapheneuze ader in de gemeenschappelijke femurader.
Afkortingen: CFV, gemeenschappelijke femorale ader; GSV, grote sapheneuze ader
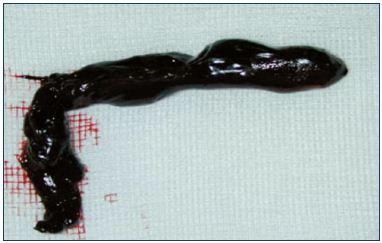
Figuur 3. Trombose van de saphenofemorale verbinding.figuur met dank aan Dr Nicolini.

in de praktijk bevelen de meeste deskundigen aan patiënten met verlengde SVT in SFJ of SPJ gedurende 3 maanden te behandelen met antistollingstherapie in therapeutische doses.
conclusie
SVT mag niet langer als een goedaardige ziekte worden beschouwd. Recente epidemiologische studies, waarbij een groot aantal patiënten betrokken was, hebben de mogelijke ernst van SVTs aangetoond en hebben hun plaats binnen de VTE-ziekten duidelijk gedefinieerd. Een gelijktijdige DVT werd vastgesteld bij 25% tot 30% van de patiënten bij presentatie en een PE bij 4% tot 7% van de patiënten. Daarom moeten alle patiënten met SVT dubbelzijdig scannen om de diagnose SVT te bevestigen, de precieze locatie en omvang van de SVT te bepalen en de aanwezigheid van DVT te diagnosticeren of uit te sluiten. Tegenwoordig is de behandeling met SVT veranderd, waarbij antistollingstherapie op grote schaal wordt gebruikt in plaats van NSAID ‘ s. Tot aan het recente CALISTO-onderzoek had geen enkel antistollingsprotocol een duidelijk klinisch voordeel aangetoond. De aanbevelingen werden bijgewerkt nadat de CALISTO-studie het anticoagulans therapie protocol gevalideerde op basis van fondaparinux 2,5 mg per dag gedurende 45 dagen. Voor patiënten met een symptomatische SVT van de benen van ten minste 5 cm lang, wordt een profylactische dosis fondaparinux of laagmoleculaire heparine gedurende 45 dagen aanbevolen zonder anticoagulatie (graad 2B). Wanneer de kosten van de behandeling met fondaparinux aanvaardbaar zijn, wordt aanbevolen fondaparinux 2,5 mg dagelijks te gebruiken in combinatie met een profylactische dosis laagmoleculaire heparine (graad 2C). De aanbevelingen en richtlijnen zijn echter van laag niveau en er blijven vragen over SVT-management. Enkele risicofactoren voor het later ontwikkelen van een VTE zijn geïdentificeerd, maar verder onderzoek is nodig om duidelijk subgroepen van patiënten met een hogere incidentie van VTE na SVT te definiëren.
1. D ecousus H, Prandoni P, Mismetti P, et al; Calisto studiegroep. Fondaparinux voor de behandeling van oppervlakkige veneuze trombose in de benen. N Engl J Med. 2010;363:1222-1232.
2. Frappé P, Buchmuller-Cordier A, Bertoletti L, et al; Steph studiegroep. Jaarlijkse diagnose percentage oppervlakkige veneuze trombose van de onderste ledematen: de STEPH community – based studie. J Tromb Hemost. 2014;12:831-838.
3. Oger E; Epi-GETBO studiegroep. Incidentie van veneuze trombo-embolie: een community-based studie in West-Frankrijk. Tromb Hemost. 2000;83:657- 660.
4. D ecousus H, Quéré I, Presles E, et al; POST studiegroep. Oppervlakkige veneuze trombose en veneuze trombo-embolie: een grote prospectieve epidemiologische studie. Ann Stagiair Med. 2010;152:218-224.
5. G alanaud JP, Genty C, Sevestre MA, et al; OPTIMEV SFMV Investigators. Voorspellende factoren voor gelijktijdige diepe veneuze trombose en symptomatische veneuze trombo-embolische recidief in geval van oppervlakkige veneuze trombose. Tromb Hemost. 2011;105:31-39.
6. Lutter KS, Kerr TM, Roedersheimer R, Lohr JM, Sampson MG, Cranley JJ. Oppervlakkige tromboflebitis gediagnosticeerd door dubbelzijdig scannen. Chirurgie. 1991;100:42-46.
7. Barrellier MT. Trombose veineuses superficielles des membres inférieurs . Werkelijke Vasc Int. 1993;17:7-9.
8. Jorgensen JO, Hanel KC, Mogan AM, Hunt JM. De incidentie van diepveneuze trombose bij patiënten met oppervlakkige tromboflebitis van de onderste ledematen. J Vasc Sur. 1993; 18: 70-73.
9. Bilancini S, Lucchi M. Les thromboses veineuses superficielles sont-elles polymorphes ? Phlébologie. 1999;52:41-43.
10. G illet JL, Perrin M, Cayman R. oppervlakkige veneuze trombose van de onderste ledematen: prospectieve analyse bij 100 patiënten . J Mal Vasc. 2001;26:16-22.
11. Kalodiki E, Stvrtinova V, Allegra C, et al. Oppervlakkige veneuze trombose: een consensusverklaring. Int Angiol. 2012;31:203-216.
12. Nicolaides A. Oppervlakkige veneuze trombose bij preventie en behandeling van veneuze trombo-embolie. Int Angiol. 2013;32:237-242.
13. G illet JL, Perrin M, Cayman R. trombo-embolische recidief na oppervlakkige tromboflebitis van de onderste ledematen. J Flebologie. 2002;2:103-118.
14. D ewar C, Panpher S. incidentie van diepe veneuze trombose bij patiënten gediagnosticeerd met oppervlakkige tromboflebitis na indiening bij een poliklinische dienst voor diepe veneuze trombose van de afdeling spoedeisende hulp. Emerg Med J. 2010; 27: 758-761.
15. Quenet S, Laporte S, Décousus H, Leizorovicz A, Epinat m, Mismetti P; STENOX Group. Factoren die veneuze trombotische complicaties voorspellen bij patiënten met geïsoleerde oppervlakkige veneuze trombose. J Vasc Sur. 2003; 38: 944-949.
16. G alanaud JP, Bosson JL, Genty C, et al. Oppervlakkige veneuze trombose en recidiverende veneuze trombo-embolie: een gepoolde analyse van twee observationele studies. J Tromb Hemost. 2012;10:1004-1011.
17. Cosmi B, Filippini M, Campana F, et al; STEFLUX onderzoekers. Risicofactoren voor recidiverende voorvallen bij proefpersonen met oppervlakkige veneuze trombose in de gerandomiseerde klinische studie SteFlux (oppervlakkige trombo-embolie Fluxum). Trombb Res. 2014; 133: 196-202.
18. G orty s, Patton-Adkins J, DaLanno M, Starr J, Dean s, Satiani B. oppervlakkige veneuze trombose van de onderste ledematen: analyse van risicofactoren, en recidief en rol van anticoagulatie. Vasc Med. 2004;9:1-6.
19. G illet JL, Allaert FA, Perrin M. oppervlakkige tromboflebitis in niet-spataderen van de onderste ledematen. Een prospectieve analyse bij 42 patiënten . J Mal Vasc. 2004;29:263-272.
20. Martinelli I, Cattaneo M, Taioli E, De Stefano V, Chiusolo P, Mannucci PM. Genetische risicofactoren voor oppervlakkige veneuze trombose. Tromb Hemost. 1999;82:1215-1217.
21. Milio G, Siragusa S, Malato a, Grimaudo S, Pinto A. oppervlakkige veneuze trombose: rol van erfelijke deficiëntie van natuurlijke anticoagulantia in extension to deep aders. Int Angiol. 2009;28:298- 302.
22. Zollinger RW, Williams RD, Briggs DO. Problemen bij de diagnose en behandeling van tromboflebitis. Arch Sur. 1962; 85: 34-40.
23. D ecousus H; studiegroep enoxaparine. Een pilot gerandomiseerde dubbelblinde vergelijking van een laag-moleculair gewicht heparine, een niet-steroïdale anti-inflammatoire agent, en placebo in de behandeling van oppervlakkige veneuze trombose. Arch Int Med. 2003;163:1657-1663.
24. Prandoni P, Tormene D, Pesavento R; Vesalio Investigators Group. Hoge vs. lage doses laagmoleculaire heparine voor de behandeling van oppervlakkige veneuze trombose van de benen: een dubbelblinde, gerandomiseerde studie. J Tromb Hemost. 2005;3:1152-1157.
25. Cosmi B, Filippini M, Tonti D, Avruscio G, Ghirarduzzi A, Bucherini E; STEFLUX onderzoekers. Een gerandomiseerd dubbelblind onderzoek naar laagmoleculaire heparine (parnaparine) voor oppervlakkige veneuze trombose: STEFLUX (oppervlakkige trombo-embolie en Fluxum). J Tromb Hemost. 2012;10:1026-1035.
26. D ecousus H, Frappé P, Accassat S, et al. Epidemiologie, diagnose, behandeling en behandeling van oppervlakkige veneuze trombose van de benen. Beste Praktijk Res Clin Haematol. 2012;25:275-284.
27. Kearon C, Kahn SR, Agnelli G, Goldhaber s, Raskob GE, Comerota AJ; American College of Chest Physicians. Antitrombotische therapie voor veneuze trombo-embolische ziekte: American College Of Chest Physicians Evidence-Based Clinical Practice Guidelines (8e editie). Borst. 2008; 133 (suppl 6): 454S-545S.
28. Kearon C, Akl EA, Comerota AJ, et al; American College of Chest Physicians. Antitrombotische therapie voor de ziekte van VTE: Antitrombotische therapie en preventie van trombose, 9e ed: American College of Chest Physicians Evidence-Based Clinical Practice Guidelines. Borst. 2012; 141(suppl 2): e419S-e494S.
29. D I Nisio M, Wichers IM, Middeldorp S. Behandeling voor oppervlakkige tromboflebitis van het been. Cochrane Database Syst Rev.2013;30;4:CD004982.
30. D I Nisio M, Middeldorp S. Treatment of lower extremity superficial thromboflebitis. JAMA. 2014;311:729- 730.
31. Sullivan V, Denk PM, Sonnad SS, Eagleton MJ, Wakefield TW. Ligatie versus anticoagulatie: behandeling van oppervlakkige tromboflebitis boven de knie waarbij het diepe veneuze systeem niet betrokken is. J Am Coll Sur. 2001; 193: 556-562.
32. Lozano FS, Almazan A. heparine met laag moleculair gewicht versus saphenofemorale disconnectie voor de behandeling van Grotere sapheneuze tromboflebitis boven de knie: een prospectieve studie. Vasc Endovasculaire Surg. 2003; 37: 415-420.
33. Chengelis DL, Bendick PJ, Glover JL, Brown OW, Ranval TJ. Progressie van oppervlakkige veneuze trombose naar diepe veneuze trombose. J Vasc Sur. 1996; 24: 745-749.
34. Hingorani A, Ascher E. oppervlakkige veneuze tromboflebitis. In: Gloviczki P, ed. Handboek van veneuze aandoeningen. Richtlijnen van het American Venous Forum. 3rd ed. London, UK: Hodder Arnold; 2009: 314-319.
Leave a Reply