Eerstelijnsbehandeling voor gemetastaseerde Castraatresistente prostaatkanker
in 2019 is prostaatkanker (PCa) verantwoordelijk voor bijna 1 op de 5 nieuwe diagnoses van kanker bij mannen in de VS.1 In de laatste jaren daalde de totale incidentie van prostaatkanker (PCa) met ongeveer 7% per jaar.1 De scherpe daling in incidentie is algemeen toegeschreven aan verminderde prostaat-specifiek antigeen (PSA) testen van 2008 tot 2013. Het verminderde gebruik van PSA-screening werd veroorzaakt door de aanbevelingen van de United States (US) Preventive Services Task Force tegen routinematige PSA-screening. Dit was een graad D aanbeveling specifiek bij mannen van 75 jaar en ouder, die werd verklaard in 2008, en later uitgebreid tot alle mannen in 2011, als gevolg van toenemende bezorgdheid van overdiagnose en overbehandeling.2 Hoewel de prevalentie van PSA-tests stopte met afnemen en zich stabiliseerde van 2013 tot 2015,3 is het effect van screeningsreductie op de incidentie van gevorderde ziekte nog onduidelijk. Een analyse van een groot Kankerregister dat 89% van de Amerikaanse bevolking beslaat, meldde dat de algemene daling van de incidentie van PSA in feite een toename van diagnoses op afstand vanaf 2010 over leeftijd en ras maskeert.Ongeacht de gegeven behandeling, ontwikkelt ongeveer 20% -30% van de patiënten met gelokaliseerde PCa zich tot gemetastaseerde ziekte, gewoonlijk behandeld met hormonale therapie.Dit kan worden toegediend door chirurgische castratie (bilaterale orchidectomie) of door medische castratie met behulp van androgeendeprivatietherapie (ADT). Beide methoden Bereiken een castraatniveau van serumtestosteron dat wordt beschouwd als de standaard van zorg voor de behandeling van metastatische hormoon-gevoelige PCa (mHSPC). MHSPC is echter bestemd om verder te gaan naar metastatische castraatresistente prostaatkanker (mCRPC).De toestand van castraatresistente prostaatkanker (CRPC) wordt gedefinieerd als ziekteprogressie ondanks het bereiken van castraattestosteronspiegels (serumtestosteron < 50 ng/dL of 1.7 nmol / L), en kan zich presenteren als een continue stijging van serum PSA-spiegels, progressie van reeds bestaande ziekte, en/of het verschijnen van nieuwe metastasen.CRPC heeft een mediane overleving van ongeveer drie jaar8 en wordt geassocieerd met een significante verslechtering van de kwaliteit van leven.9 het precieze mechanisme van de overgang van mHSPC naar mCRPC is nog onduidelijk. Nochtans, is het bekend dat ondanks castraatniveaus van androgens, de androgen receptor (AR) actief blijft en PCA vooruitgang in CRPC blijft drijven.10 Dit heeft geleid tot de ontwikkeling van nieuwe agenten gericht op verdere vermindering van androgen productie of het blokkeren van AR functie. Nochtans, zijn er andere biologische wegen die onafhankelijk van androgen signaleren functioneren en ook in CRPC resulteren. er hebben zich verscheidene significante verschuivingen voorgedaan in de behandelingsopties van de mHSPC-ruimte, resulterend in een aanzienlijk overlevingsvoordeel (zie “de snel evoluerende managementstrategie van metastatische hormoongevoelige prostaatkanker” link), waaronder de introductie van chemotherapie in de chaarted-studie11 en STAMPEDE-studie12,de toevoeging van abirateronacetaat en prednison in de LATITUDE-studie13 en STAMPEDE-studie 14,de toevoeging van enzalutamide in de ARCHES-studie15 en de ENZAMET-studie16 en tot slot, de toevoeging van apalutamide, een oraal niet-steroïdaal anti-androgeen, die zoals enzalutamide, bindt direct aan het ligand-bindende domein van AR en verhindert ar translocatie, DNA-band, en AR-gemedieerde transcriptie.Het TITAN-onderzoek toonde een overall survival (OS) voordeel bij met apalutamide behandelde mHSPC-patiënten.Apalutamide heeft ook voordeel ten opzichte van placebo getoond in de niet-gemetastaseerde CRPC (nmCRP) setting in de Spartan fase 3 placebogecontroleerde trial,19 vergelijkbaar met het voordeel dat wordt aangetoond door met enzalutamide behandelde niet-gemetastaseerde castraatresistente prostaatkanker (nmCRPC) patiënten in de PROSPER trial20 (zie “de nieuwe behandelingen voor de niet-gemetastaseerde castraatresistente prostaatkanker” link). Deze behandelingsvooruitgang in de mHSPC en nmCRPC setting heeft de vraag doen rijzen welke behandelingsopties aan patiënten in de mcrpc setting moeten worden aangeboden.De behandeling van mannen met CRPC is de laatste 15 jaar drastisch veranderd. Vóór 2004, toen patiënten faalden op primaire ADT, werden behandelingen uitsluitend voor palliatie toegediend. The landmark trials by Tannock et al.22 en Petrylak et al.In 2004 introduceerden docetaxel chemotherapie bij mCRPC-patiënten waarvan werd aangetoond dat ze hun overleving verbeterden. Echter, aangezien docetaxel FDA goedgekeurd was, zijn vijf bijkomende heilzame middelen die een overlevingsvoordeel vertoonden, goedgekeurd door de FDA, gebaseerd op gerandomiseerde klinische studies (Tabel 1). Deze omvatten enzalutamide, en abirateron, die specifiek de androgeenas beïnvloeden, sipuleucel-T, dat het immuunsysteem stimuleert; 24 cabazitaxel, dat een ander chemotherapeutisch middel is; 25 en radium-223, een radionuclidetherapie.26 andere behandelingen voor mCRPC hebben getoond om resultaten te verbeteren maar zijn nog goedgekeurd door de FDA en zullen in een ander overzicht worden besproken. Wegens de substantiële verhoging van veelvoudige FDA-goedgekeurde therapeutische agenten in patiënten met CRPC, worden de artsen uitgedaagd met een overvloed van behandelingsopties en menigte potentiële opeenvolgingen van deze agenten, die klinische besluitvorming in mcrpc beduidend complexer maken.
Tabel 1. Middelen die in de VS zijn goedgekeurd voor de behandeling van gemetastaseerde castraatresistente prostaatkanker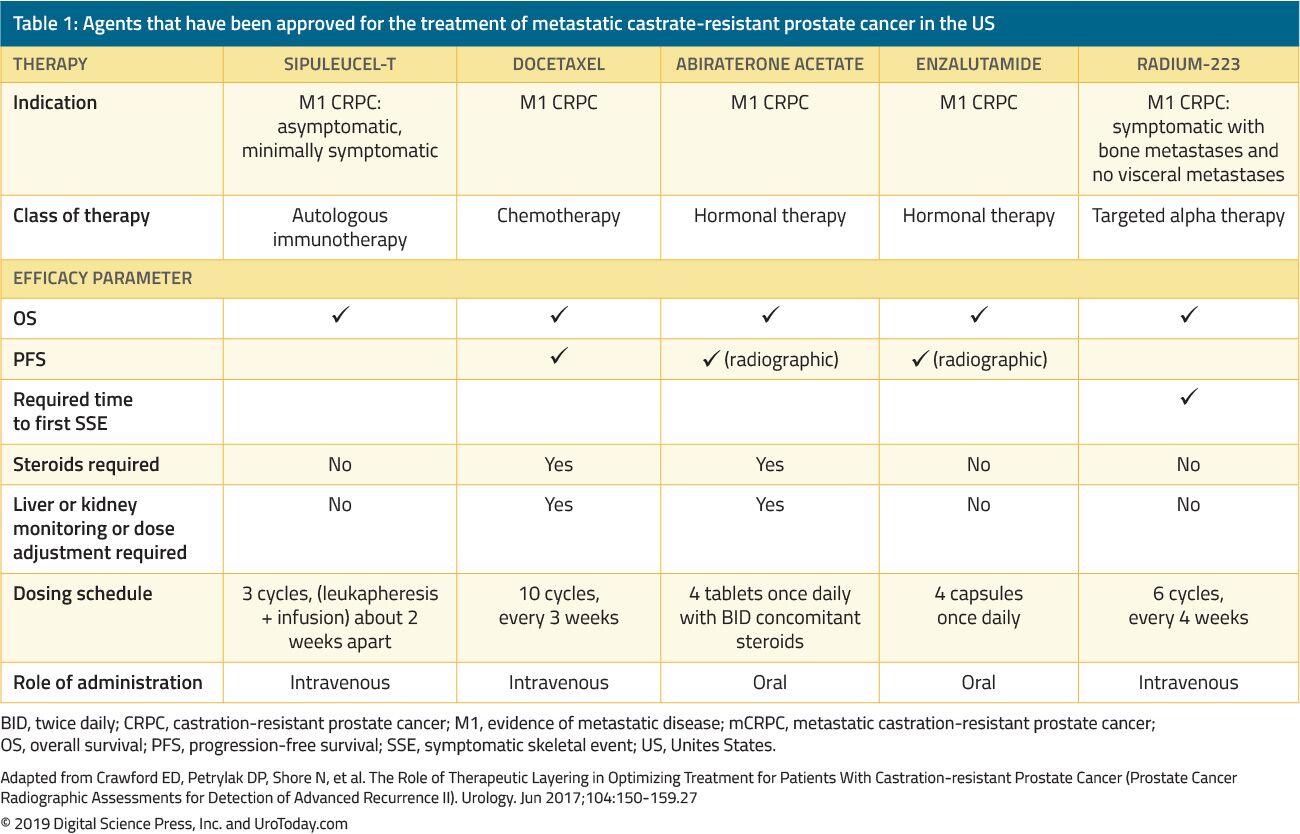
mCRPC is gewoonlijk een slopende ziekte, en patiënten zullen hoogstwaarschijnlijk profiteren van een beheersstrategie die is geformaliseerd door een multidisciplinair team bestaande uit urologen, medische oncologen, stralingsoncologen, verpleegkundigen, psychologen en maatschappelijk werkers.Het is noodzakelijk om palliatiebehandelingsopties te bespreken wanneer aanvullende systemische behandeling wordt overwogen, waaronder behandeling van pijn, constipatie, anorexia, misselijkheid, depressie en vermoeidheid.
Een ander cruciaal punt om rekening mee te houden bij het vaststellen van de juiste behandelingsvolgorde in deze ziektenruimte is de bijbehorende kosten. Bij gebruik van modellen die aanvullende behandelingslijnen voor of na docetaxel omvatten, was de gemiddelde kostprijs van de mcrpc-behandeling gedurende een gemiddelde periode van 28,1 maanden ongeveer $48.000 per patiënt.29 Deze kosten zijn vrij hoog vanwege het feit dat patiënten meerdere therapielijnen kunnen krijgen en lopende medische diensten kunnen krijgen tijdens hun ziekte.Slechts twee studies hebben een marginaal overlevingsvoordeel aangetoond voor patiënten die LHRH-analogen blijven gebruiken in plaats van tweedelijnsbehandelingen en derdelijnsbehandelingen toe te voegen.31, 32 Studies hebben aangetoond dat CRPC niet resistent is tegen ADT, maar eerder overgevoelig voor het.10 behandeling-gemedieerde selectiedruk tijdens ADT veroorzaakt AR om te versterken, en ervoor te zorgen de situatie niet escaleert, ADT wordt voortgezet worden toegediend in de mcrpc-setting. Behandeling-gemedieerde selectiedruk gaat ook door gedurende de gehele levensduur van de tumor, waardoor de noodzaak om correct sequentietherapieën wordt versterkt. Echter, omdat er geen prospectieve gegevens beschikbaar zijn, weegt het minimale mogelijke voordeel van het voortzetten van castratie nog steeds op tegen het minimale risico van deze behandeling. Bovendien zijn alle later goedgekeurde behandelingen onderzocht bij mannen met lopende ADT, waarbij nog een reden wordt toegevoegd waarom het moet worden voortgezet. voordat we ingaan op de beschikbare behandelingsopties, is het belangrijk te erkennen dat het nog steeds onduidelijk is wanneer de behandeling moet worden gestart bij mCRPC-patiënten die volledig asymptomatisch zijn. Het is nog steeds onbekend of eerdere behandeling superieur is, of dat we moeten wachten tot de patiënt symptomatisch wordt en pijn ontwikkelt. Voordat de behandeling wordt gestart, moeten we rekening houden met de bestaande comorbiditeiten van de patiënt en de verwachte bijwerkingen van het starten van de behandeling. Patiënten met een vroeg stadium mCRPC in het COU-AA-302-onderzoek die abirateron kregen, overleefden meestal bijna een jaar langer dan degenen die placebo kregen (mediane OS, 53,6 maanden vs .41,8 maanden, respectievelijk HR, 0,61; 95% BI, 0,43 tot 0,87; P=.006).Daarom hadden mcrpc-patiënten in een vroeg stadium baat bij een eerdere start met abirateron. In dezelfde studie leidde abirateron bij patiënten met asymptomatische of licht symptomatische mCRPC bij baseline PSA < 15,6 ng/mL ook tot een snellere afname en een grotere mate van afname van PSA dan bij placebo.34 hoewel de momenteel beschikbare gegevens beperkt zijn, lijkt het er zeer waarschijnlijk op dat een eerder dan een later begin van de behandeling voordeliger is.
goedgekeurde eerstelijnsbehandelingsopties voor gemetastaseerd castraatresistent prostaatkanker
Abirateron
Abirateron is een antiandrogeen dat een remmer is van 17α-hydroxylase / C17,20-lyase (CYP17) enzym. De cou-AA-302 fase III-studie evalueerde abirateron bij 1.088 chemo-naïeve, asymptomatische of licht symptomatische mcrpc-patiënten zonder viscerale metastasen. In dit onderzoek werden patiënten gerandomiseerd naar abirateronacetaat of placebo, beide gecombineerd met prednisone35 (figuur 1). Patiënten werden gestratificeerd naar de Eastern Cooperative Oncology Group (ECOG) performance status 0 of 1 en naar asymptomatische of licht symptomatische ziekte.OS en radiografische progressievrije overleving (rpfs) waren de co-primaire eindpunten. Het onderzoek toonde aan dat er na een mediane follow-up van 22,2 maanden een significante verbetering van de rPFS was in de abirateron-arm (mediaan 16,5 vs.8,2 maanden, HR 0,52, p < 0,001). Bij de eindanalyse na een mediane follow-up van 49,2 maanden was het OS eindpunt significant positief (34,7 vs.30,3 maanden, HR: 0,81, 95% BI: 0,70-0,93, p = 0,0033).Het is belangrijk te onthouden dat mCRPC een breed prognostisch spectrum overspant, zelfs wanneer het chemotherapie-naïef is.In een analyse van de abirateron-arm van de COU-AA-302-studie hadden patiënten die bij aanvang geen pijn hadden, normale alkalische fosfatase-en LDH-spiegels en minder dan 10 botmetastasen een mediane OS van 42,6 maanden.Patiënten met meer risicofactoren voor progressie hadden echter een significant kortere mediane OS.Bij het beoordelen van het toxiciteitsprofiel van abirateron leek het meer bijwerkingen te veroorzaken die verband hielden met overmaat aan mineralocorticoïden en afwijkingen in de leverfunctie, maar deze waren meestal ingedeeld met 1-2 bijwerkingen. Ten slotte bleek abirateron ook even werkzaam te zijn bij ouderen (> 75 jaar).38
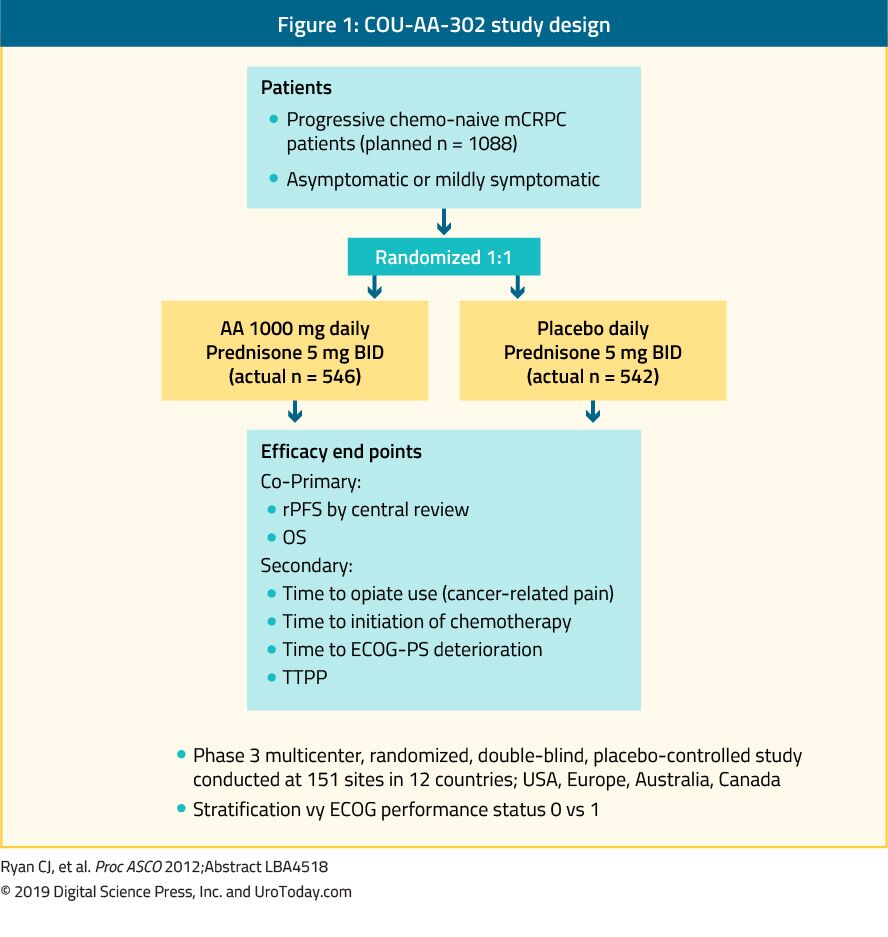
figuur 1. COU-AA-302 onderzoeksopzet
Enzalutamide
Enzalutamide is een niet-steroïdaal antiandrogeen. Het PREVAIL-onderzoek, dat een gerandomiseerd fase III-onderzoek is, omvatte 1.717 chemo-naïeve mcrpc-patiënten en patiënten met viscerale metastasen kwamen ook in aanmerking.In dit onderzoek werd enzalutamide vergeleken met placebo (Figuur 2). Het PREVAIL-onderzoek toonde een significante verbetering bij met enzalutamide behandelde patiënten in beide co-primaire eindpunten, waaronder rPFS (HR: 0,186; CI: 0,15-0,23, p < 0,0001) en OS (HR: 0,706; CI: 0,6-0,84, p < 0,001). Uitgebreide follow-up en definitieve analyse bevestigden een voordeel in OS en rPFS voor enzalutamide.Bij 78% van de met enzalutamide behandelde patiënten werd een PSA-daling van meer dan 50% gemeld. De meest voorkomende klinisch relevante bijwerkingen waren vermoeidheid en hypertensie. Enzalutamide was ook even effectief en goed verdragen bij oudere mannen (> 75 jaar)41 en bij mannen met of zonder viscerale metastasen.Voor mannen met levermetastasen leek er echter geen waarneembaar voordeel te zijn.In het TERRAIN-onderzoek werd enzalutamide vergeleken met bicalutamide, een ouder antiandrogeen, in een gerandomiseerd dubbelblind fase II-onderzoek, waaruit een significante verbetering van PFS bleek (15.7 months vs. 5.8 months, HR: 0.44, p < 0.0001) in favor of enzalutamide.44
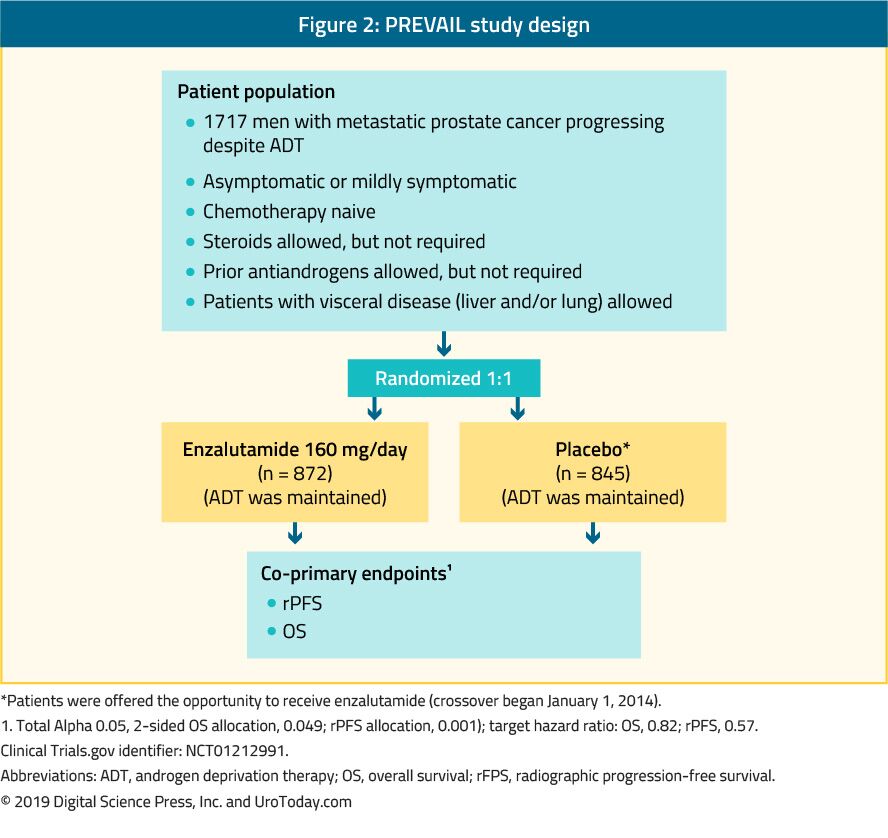
Figure 2. PREVAIL study design
Docetaxel
The landmark trial TAX 327 showed a significant improvement in median OS of 2-2.9 months in mCRPC patients treated with docetaxel-based chemotherapy when compared to patients who were treated with mitoxantrone plus prednisone therapy.22 The SWOG 9916 trial compared mitoxantrone to docetaxel and showed similar results23 (Figure 3). De standaard eerstelijns chemotherapie is docetaxel 75 mg/m2 in driewekelijkse doses gecombineerd met prednison 5 mg tweemaal daags, tot tien cycli. Er zijn verschillende belangrijke prognostische factoren waarmee rekening moet worden gehouden bij toediening van docetaxel: viscerale metastasen, pijn, anemie (Hb < 13 g/dL), progressie van de botscan en voorafgaande behandeling met estramustine. Deze prognostische factoren kunnen helpen de respons op docetaxel te stratificeren. Met behulp van deze prognostische factoren kan de ziekte worden gecategoriseerd in Laag, Gemiddeld en hoog risico, met significant verschillende overeenkomstige mediane OS schattingen van 25.Respectievelijk 7, 18,7 en 12,8 maanden.Hoewel leeftijd op zich geen contra-indicatie is voor docetaxel, moeten patiënten fit genoeg zijn om dit type behandeling te doorstaan en moeten de comorbiditeiten worden beoordeeld voordat de behandeling wordt gestart. Bij mannen van wie wordt aangenomen dat zij de standaarddosis en het standaardschema van docetaxel niet kunnen verdragen, kan dit worden verlaagd van 75 naar 50 mg/m2 elke twee weken, waarbij minder graad 3-4 bijwerkingen optreden en een langere tijd tot falen van de behandeling.46
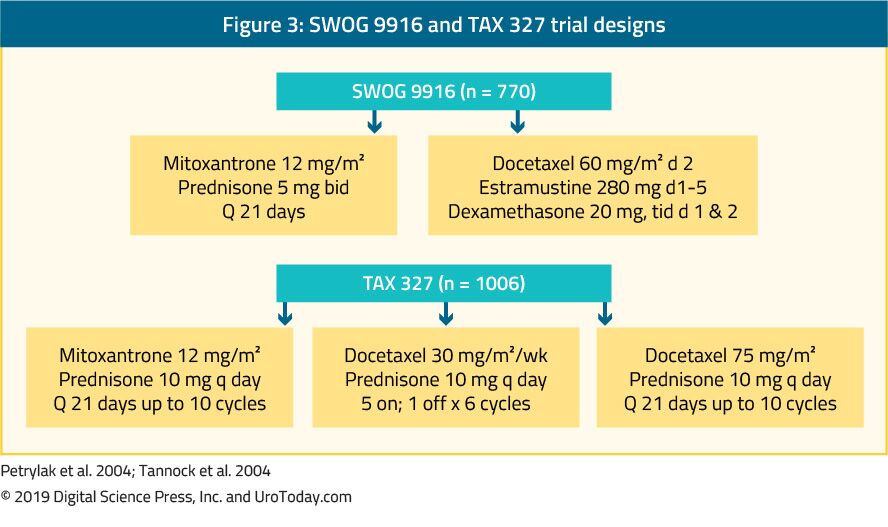
Figuur 3. SWOG 9916 en TAX 327 studieontwerpen
Sipuleucel-T
sipuleucel-T, een autologe actieve cellulaire immunotherapie, bleek in een fase III studie (IMPACT trial) een overlevingsvoordeel te bieden bij 512 asymptomatische of minimaal symptomatische mcrpc patiënten in vergelijking met placebo24 (Figuur 4). Na een mediane follow-up van 34 maanden was de mediane overleving significant hoger in de sipuleucel-T-groep (25,8 vs.21,7 maanden, met een HR van 0,78, p = 0,03).Belangrijk is dat er tijdens of na de behandeling geen PSA-afname werd waargenomen en dat de PFS in beide armen vergelijkbaar was. De totale tolerantie voor sipuleucel-T was zeer goed, waarbij meestal graad 1-2 bijwerkingen optraden. Momenteel is deze behandeling alleen beschikbaar in de VS en is niet langer beschikbaar in Europa.
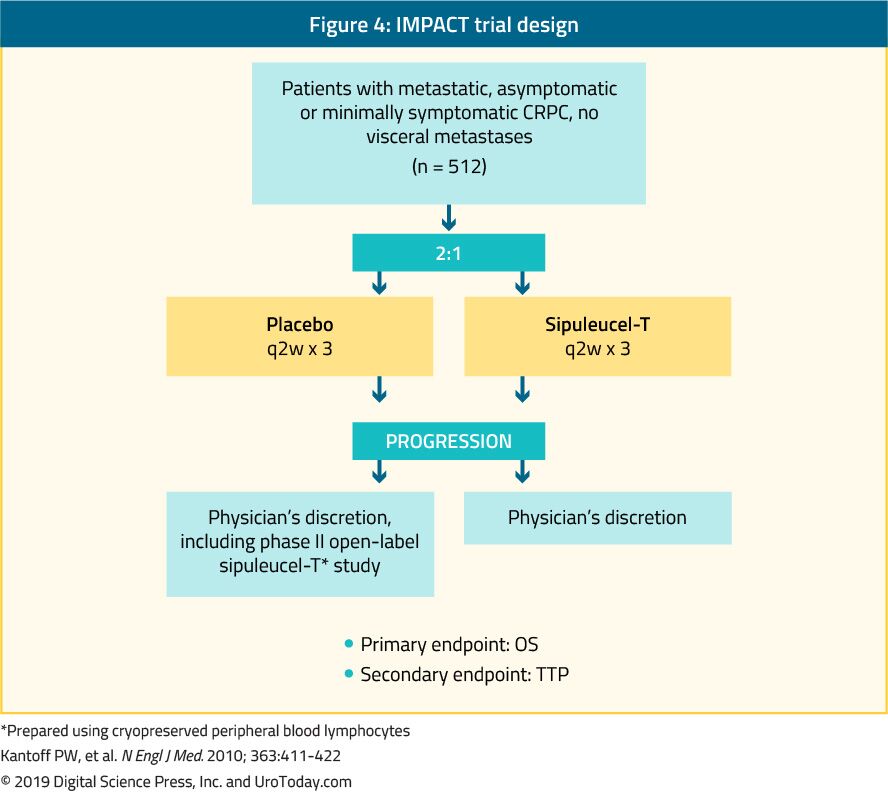
Figuur 4. IMPACT trial design
conclusies
In de afgelopen 15 jaar is er aanzienlijke wetenschappelijke vooruitgang geboekt en is er geïnvesteerd in de ontwikkeling van geneesmiddelen voor patiënten met mCRPC. Dit heeft geresulteerd in de FDA goedkeuring van verscheidene lijnen van systemische therapie op grond van pijn palliation, het minimaliseren van ziekte nadelige gevolgen, en OS verlenging. Tot op heden is de gerapporteerde impact op OS bij mCRPC-patiënten van elk van deze individuele middelen nog bescheiden, wat resulteert in een toevoeging van slechts enkele maanden. Het is noodzakelijk om ons begrip van de ziektebiologie van mCRPC te verbeteren, een uitgebreid moleculair begrip van castratieweerstand te integreren, en mechanismen van weerstand tegen huidige therapieën te analyseren om toekomstige behandelingsontwikkeling te verbeteren. Het is ook essentieel om voorspellende biomarkers te investeren en te ontwikkelen om in de personalisatie van therapie te helpen. Tot slot, op een meer praktische noot, meer gegevens nodig zijn over de juiste tweede en derde-lijn therapieën, en sequencing en combinatie van beschikbare medicijnen, in meer detail besproken in het volgende overzicht artikel (“Beyond first line treatment of metastatic castrate-resistant prostate cancer”).
Publicatiedatum: 19 November 2019
Leave a Reply