Vogt-Koyanagi-Harada (VKH) Disease
tekijät: Anthony P. Mai, BS; Charlene Tran, BS; Caroline W. Wilson, MD; Austin R. Fox, MD; H. Culver Boldt, MD
1.huhtikuuta 2019
alustava esitys
Chief vaiva
suttuinen näkö ja päänsärky
Nykyhistoria sairaus
44-vuotias vietnamilaisnainen, jolla oli 10 päivän historia etenevästä Sumeasta näkökyvystä molemmissa silmissä ja kolmen päivän historia voimakkaasta päänsärystä. Hänen keskeinen näkökykynsä ei ollut parantunut optometristin taitteella. Hänen kovat takaraivopäänsärynsä pahenivat liikkumisen myötä ja ne liittyivät yleistyneeseen huonovointisuuteen, äärimmäiseen väsymykseen, lievään valonarkuuteen ja repimiseen. Parasetamoli lievitti kipua osittain.
hän oli hiljattain matkustanut Vietnamiin, mutta kiisti kohdanneensa siellä sairaita kontakteja. Hän kiisti leuanvedon, kuumeilun tai painonvaihtelut. Hän kiisti ihottumat, kuulomuutokset, tinnituksen, huimauksen, puutumisen tai kihelmöinnin. Hän kiisti koskaan sairastaneensa tuberkuloosia. Hänellä ei ollut aiempia näköongelmia, autoimmuunisairauksia tai syöpää.
aiempi Silmähistoria
- kosmeettisen silmäluomileikkauksen (molemminpuolisen blefaroplastian) historia kolme vuotta aiemmin
- ei ollut silmävammaa tai-sairautta
aiempi sairaushistoria
Ei mitään
lääkkeet
Parasetamoli tarpeen mukaan
allergiat
Ei tunnettuja lääkeallergioita
H3> sukuhistoria
ei ollut silmäsairautta tai autoimmuunisairautta
sosiaalihistoria
hän muutti Vietnamista useita vuosia ennen esillepanoa. Hän on naimisissa ja hänellä on kolme lasta. Hän työskentelee kynsisalongissa. Hän ei käytä tupakkatuotteita, alkoholia eikä laittomia päihteitä. Hän matkustaa Vietnamiin kuuden-kahdentoista kuukauden välein.
Systeemikatsaus
negatiivinen, paitsi mitä on kuvattu yksityiskohtaisesti nykyisen sairauden historiassa
silmätutkimus
näöntarkkuus ja / ilman korjausta (Snellen)
- oikea silmä (OD): 20/300 (ei paranemista neulanreiällä)
- vasen silmä (OS): 20/60-2+2 (ei paranemista neulanreiällä)
silmän motiliteetti / kohdistus
täydet silmänulkoiset liikkeet molemmissa silmissä (OU)
silmänpaine (IOP): (Tonopen)
pupillit
pupillit pupillit oppilaat oppilaat oppilaat sormet)
- od: Keski-SKOTOOMA
- os: täydellinen inferotemporaalinen vika
ulkoinen
normaali molemmin puolin
rakolampun tentti
- luomet / ripset: normaali ou
- sidekalvo / kovakalvo: kirkas ja hiljainen ou
- sarveiskalvo: 1+ välimerkit epiteeliset eroosiot, ei keratiinisaostumia OU
- etukammio: Jälkisolu ja leimahdus ja syvä OU
- värikalvo: normaali arkkitehtuuri ou
- linssi: kirkas OU
Laajentunut silmänpohjakoe (DFE)
- lasiainen: jälki anterioriset lasiaissolut OU
- levy:
- OS: Grade 2-3 levyn turvotus, Hypereeminen
- cup-to-disc Ratio: 0, 0 OU
- Makula:
- od: 3+ kystoidinen makulaödeema (CME) ja subretinaalinen neste (SRF), joka ulottuu levystä ohimomakulaan. Ei lipidejä eikä eritettä. Pahalta näyttävä suonikalvo.
- OS: 2+ CME ja SRF, jotka ulottuvat kiekosta fovean kautta. 1-2 + lineaarinen lipidi, joka ulottuu levystä kohti fovea. Pahalta näyttävä suonikalvo.
- alukset:
- OD: Sheathing temporally
- OS: normaali
- OD: Grade 3 levyn turvotus, hypereeminen
- OD: kystinen verkkokalvon tuft anterior to the equator at 10: 30
- OS: Shallow SRF anterior to the equator at 4:00
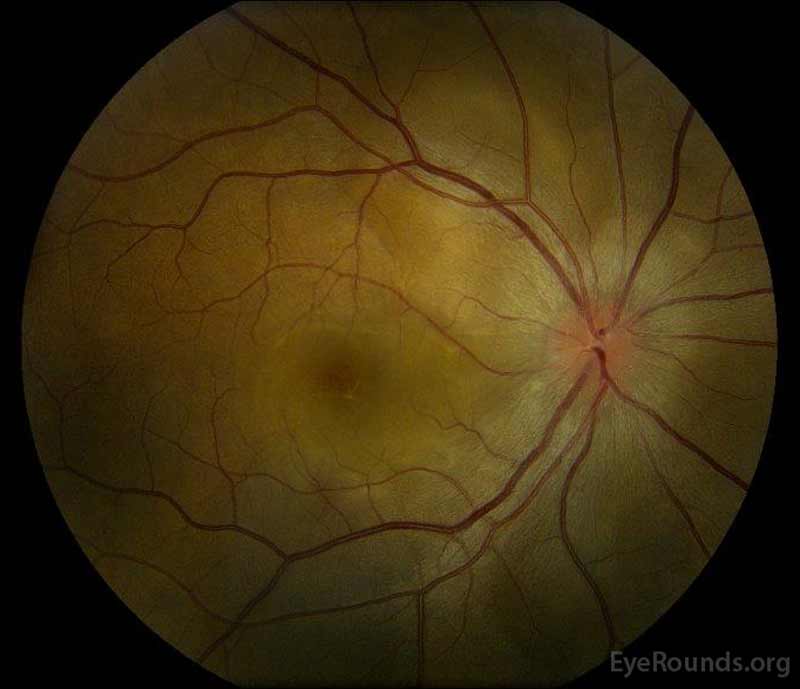 |
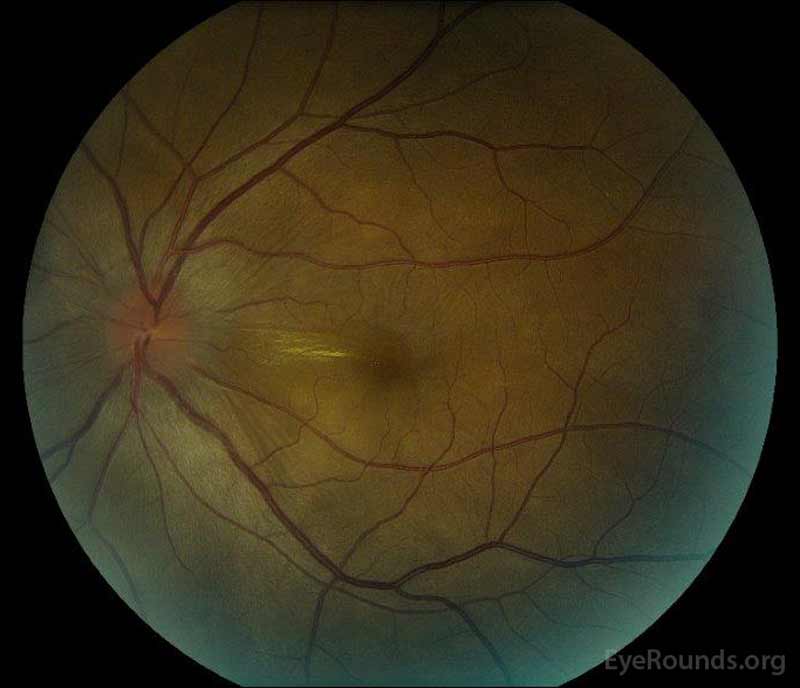
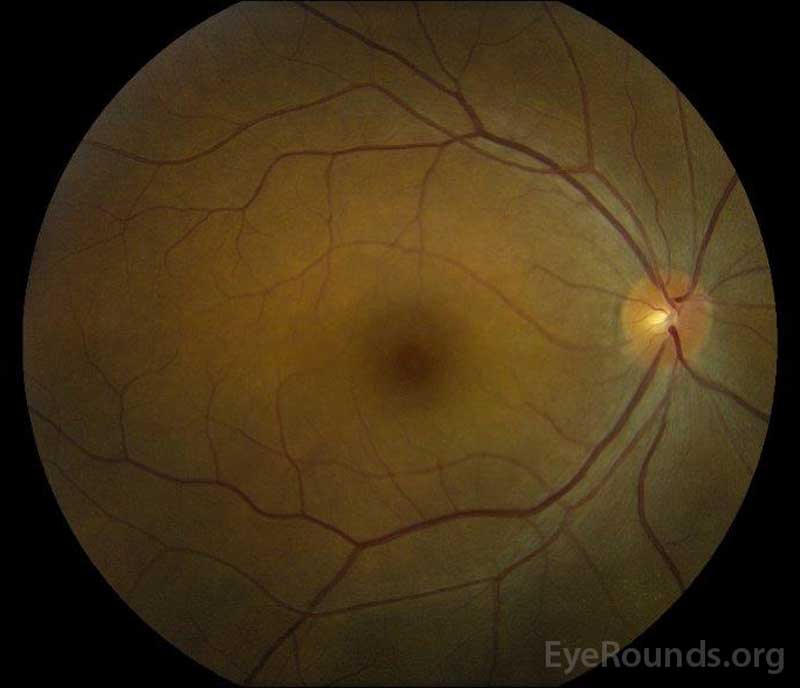
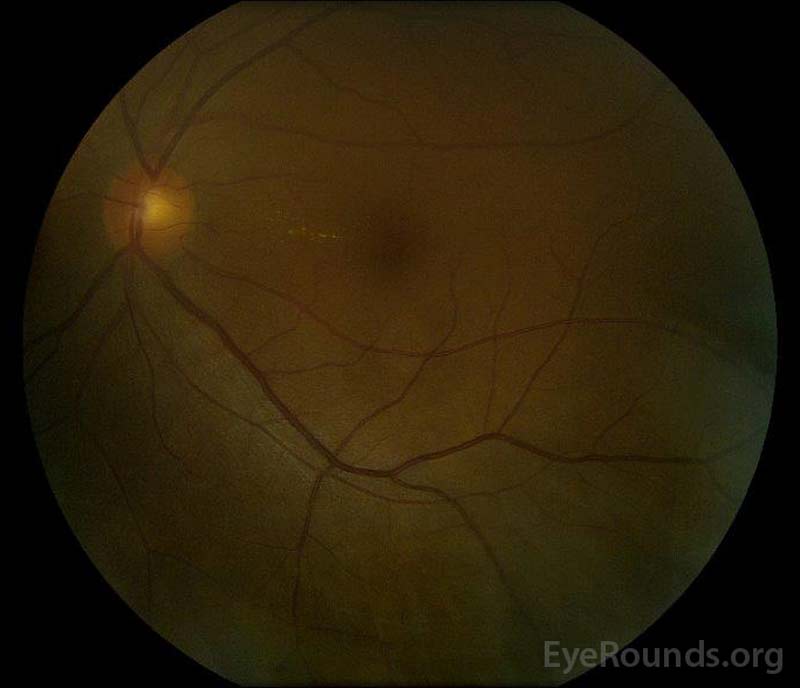
kuva 1: värikynäkuvat esillepanossa: (vasen kuva) oikeassa silmässä on kiekkopöhöä ja lievää hyperemiaa sekä subretinaalista nestettä, joka ulottuu kiekosta tilapäisesti makulan läpi. On myös fokaalinen seroosi verkkokalvon irtauma superotemporaalinen levylle, pitkin superior arcade. (Right image) The left eye has disc edema and mild hyperemia, along with subretinal fluid extending from the disc to the macula and linear lipid deposits in the nasal macula.
 |
 |
 |
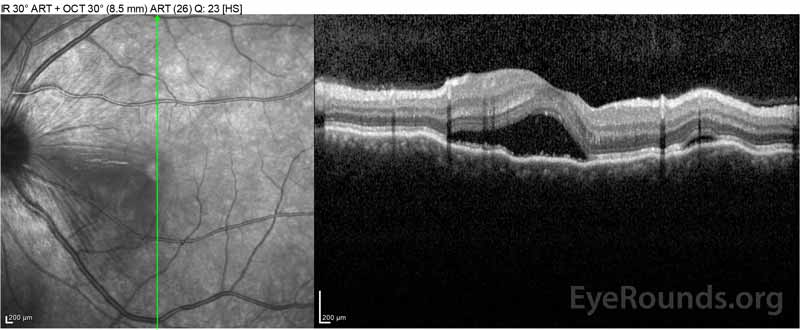 |
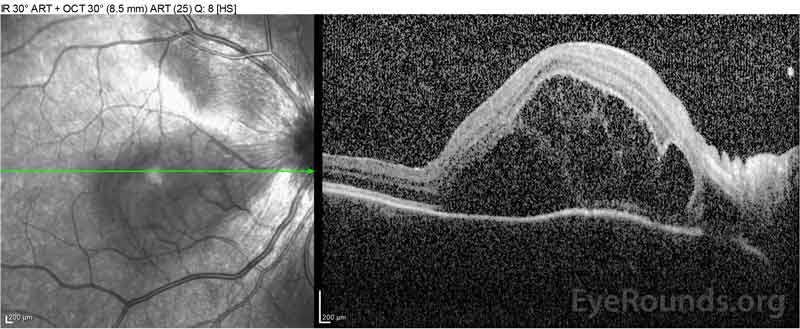
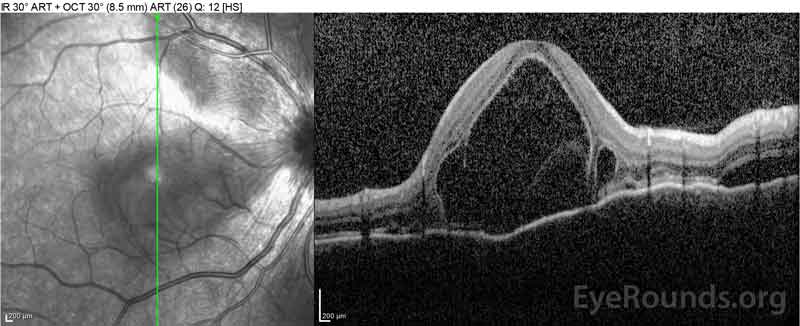
Figure 2: Optinen koherenssitomografia (OCT) oikean silmän (ylempi paneelit) osoittaa seroosi verkkokalvon irtauma mukana fovea laaja päällä intretretinaalinen neste, häiriöitä ulomman verkkokalvon kerrokset, ja aaltoilua paksuuntunut suonikalvo. OCT vasemman silmän (alapaneelit) näyttää seroosi verkkokalvon irtauma nenän makula ulottuu fovea.
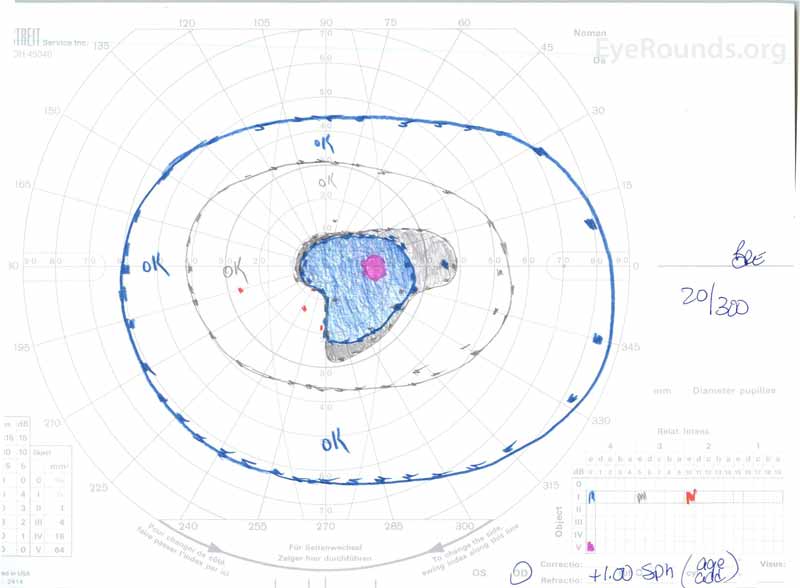
kuva 3: Goldman visual fields (GVF), OU. OS: ssa näkyy suurentunut fysiologinen sokea piste ja lievä Keski-skotooma. OD: ssä on kohtalaisen tiheä Keski-skotooma, johon liittyy fysiologinen sokea piste ja joka ulottuu tilapäisesti.
B-scan: ei merkkejä skleriitistä, lievästä vitreaalisesta samentumasta/alemmista soluista
erotusdiagnoosi
- akuutti posteriorinen multifokaalinen placoidipigmentti epitelopatia (APMPPE)
- keskinen seroosi korioretinopatia
- optinen neuriitti
- Panuveiitti
- autoimmuunisairaus (esim.SLE, sarkoidoosi)
- infektio (e.g., kuppa, tuberkuloosi, Bartonella henselae)
- maligniteetti (esim. silmän lymfooma)
- sympaattinen oftalmia
- Uveaalinen effuusiooireyhtymä
- Vogt-Koyanagi-Haradan oireyhtymä
posteriorinen skleriitti
tutkimus
täydellinen verenkuva
valkosolujen määrä: 4, 9 k/mm3 (ref: 3, 7-10, 5)
punasolujen määrä 3, 99 m/mm3 (ref: 4, 0-5, 2)
hemoglobiini 11, 6 g/dl (Ref: 11, 9-15, 5)
hematokriitti 35 % (ref: 35-47)
Basic metabolic panel
Sodium 138 mEq/L (Ref: 135-145)
Potassium 4.3 mEq/L (Ref: 3.5-5.0)
Chloride 107 mEq/L (Ref: 95-107)
CO2 20 mEq/L (Ref: 22-29)
Blood urea nitrogen 16 mEq/dL (Ref: 10-20)
Creatinine 0.7 mg/dL (Ref: 0.5-1.0)
C-reactive Protein (CRP): <0.5 mg/dL (Ref: <=0.5)
Erythrocyte sedimentation rate (ESR): 12 mm/Hr (Ref: 0-20)
Angiotensin–converting enzyme (ACE): 13 U/L (Ref: 8-52)
QuantiFERON-Tb Gold: negatiivinen
rauta, veri 54 mikrogrammaa/dL (Ref: 37-145)
raudan kokonaissitoutumiskyky 379 mikrogrammaa/dL (Ref: 250-425)
kliininen hoito
ensihoitoyksikkö arvioi potilaan aluksi, koska hänellä oli valituksia uudesta vaikeasta päänsärystä ja näön menetyksestä. Aivojen tietokonetomografia (TT) ja magneettikuvaus (MK) skannaukset olivat merkityksettömiä. ESR ja CRP olivat normaalilla tasolla. Silmätautien klinikka arvioi hänet seuraavana päivänä ja löysi molemminpuolisia serooseja verkkokalvon irtaumia ja panuveiitin. ACE-ja QuantiFERON-Tuberkuloosilaboratoriot olivat molemmat negatiivisia. Hänellä diagnosoitiin Vogt-Koyanagi-Haradan tauti kliinisen esiintymisasunsa ja aasialaisen syntyperänsä perusteella. Hänelle annettiin päivittäin 80 mg prednisonia, päänsärkyyn tarvittavaa parasetamolia sekä D-vitamiini-ja kalsiumlisää. Päänsäryt hävisivät nopeasti, ja näöntarkkuus parani tasaisesti seuraavien kahden viikon aikana. Prednisoniannosta pienennettiin 40 mg: aan kolmen viikon aikana, jolloin oireet hävisivät jatkuvasti ja näöntarkkuus parani. Päänsäryt tai näkökyvyn heikkeneminen eivät uusiutuneet prednisonihoidon aikana. Viimeisimmässä tapaamisessaan hän oli supistunut 5mg: hen joka toinen päivä ilman oireiden paluuta. Hänen näöntarkkuutensa seurantakäynnillä oli 20/15 – 2 OD ja 20/20+2 OS, ja silmänpohjan OKT osoitti täyden resoluution välilevyödeemaa ja serooseja verkkokalvon irtaumia molemmissa silmissä (Kuva 4).
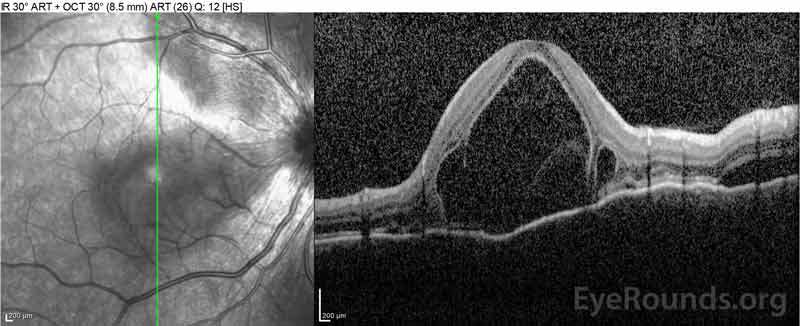
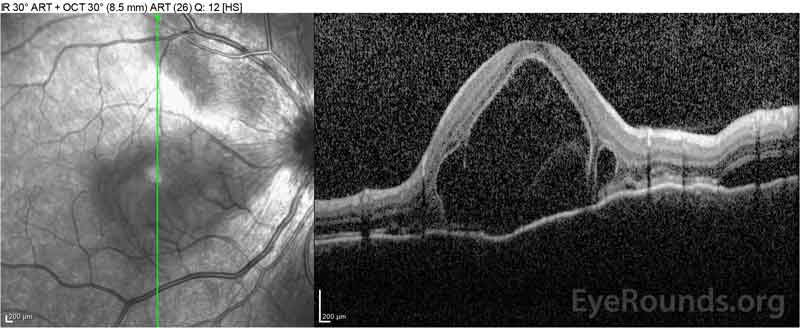
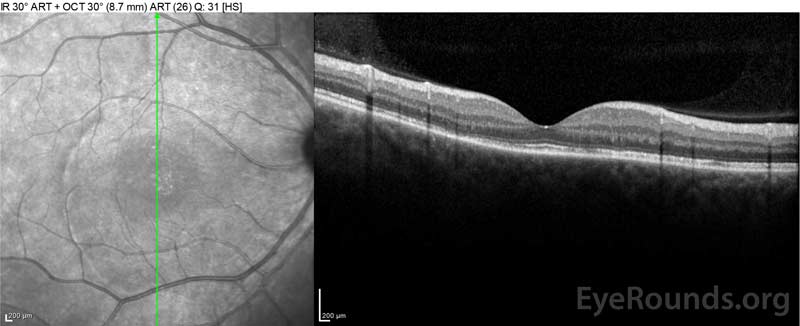
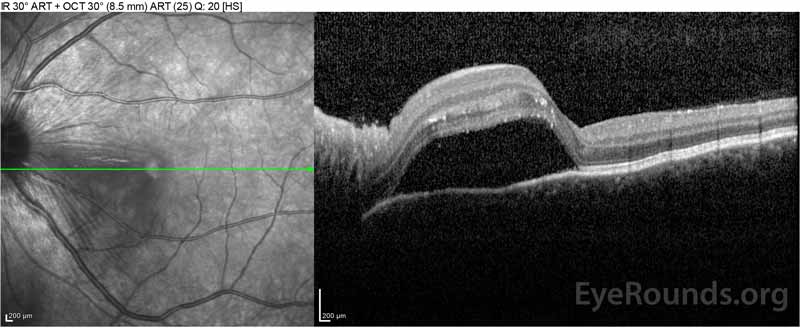
kuva 4: Optinen koherenssitomografia, jossa näkyy subretinaalinestettä lähtötilanteessa (ylhäällä) ja resoluutiota yhden viikon (keskellä) ja viiden viikon (alhaalla) kuluttua, kun potilas saa suuriannoksisen prednisonin suun kautta. Huomaa, että suonikalvon aaltoilut tasoittuvat hoidolla.
kuva 5: Color fundus valokuvaus oikean (A) ja vasemman (B) silmät aikana toipilas vaiheessa osoittaa parannusta subretinal nesteen ja levy turvotus.
diagnoosi
vaillinainen Vogt-Koyanagi-Haradan tauti
keskustelu
Vogt-Koyanagi-Haradan (VKH) tauti on systeeminen autoimmuunisairaus, jolle on ominaista bilateraalinen ei-nekrotisoiva granulomatoottinen panuveiitti, johon liittyy silmän ulkopuolisia kokonaislukumuutoksia, kuten polioosia ja vitiligoa, sekä uveaan, sisäkorvaan, hiuksiin ja selkäydinkalvoon vaikuttava tulehdus. Haradan tauti on eristetty uveiitti, jossa ei ole VKH: n systeemisiä merkkejä tai oireita.
etiologia
VKH-taudin etiologia on nykyisistä tutkimustoimista huolimatta vielä suurelta osin tuntematon. Sen arvellaan olevan hankittu autoimmuunisairaus, johon liittyy t-soluvälitteinen yliherkkyys melanosyyttisille itseantigeeneille, jolla on taustalla geneettinen alttius ja mahdollinen mikrobien laukaisija . Tyrosinaasi ja tyrosinaasi-sukuiset peptidit ovat melanosyyttien antigeenejä, joita on ehdotettu autoimmuuniprosessien kohteiksi VKH: ssa . VKH-taudin lisääntynyt riski ei kuitenkaan Erään tutkimuksen mukaan liittynyt tyrosinaasi-geeniperheeseen .
koska esiintyvyys on lisääntynyt tiettyjen etnisten ja sukupuoliryhmien keskuudessa, VKH: n patogeneesissä arvellaan olevan geneettinen alttius. VKH: hon on eri etnisissä populaatioissa yhdistetty useita geenejä, kuten ihmisen leukosyytti-antigeeni (HLA) ja interleukiini (IL) – geenit . HLA-reseptorit ovat ihmisillä merkittäviä histokompatibiliteettikomplekseja, jotka esittävät peptidejä immuunijärjestelmään. HLA-DR1, HLA-DR4, HLA-DRB1*0405 ja HLA-DRw53 ovat useita haplotyyppejä, joita esiintyy VKH-tautia sairastavilla potilailla . HLA-DR4 on yleisempää japanilaisilla ja latinalaisamerikkalaisilla, kun taas HLA-DRB1*0405 on yleisempää korealaisilla ja Lähi-idän potilailla . Sekä HLA-DR4 että HLA-DRB1*0405-alleeleita löytyy Vietnamilaisilta potilailta . HLA-DRB1-reseptori sitoutuu melanosyyttien antigeeneihin vaihtelevasti. Näistä yhteyksistä huolimatta geenitestausta ei tällä hetkellä suositella.
kun otetaan huomioon VKH: hon liittyvät tavanomaiset prodromaaliset oireet, kuten kuume, päänsärky, meningismus ja tinnitus, viruksen etiologian on ehdotettu laukaisevan VKH: n puhkeamisen molekyylimekanismien kautta geneettisesti alttiilla potilailla. Sytomegaloviruksen kirjekuoren glykoproteiini H: lla on merkittävä aminohappohomologia tyrosinaasi-peptidiin nähden, ja CMV-infektio voi laukaista VKH: n molekyylimimikoinnin kautta (eli HLA-luokan II reseptorien kautta) . Myös Ebstein-bar-virusta (EBV) on käytetty. VKH: n viruksen etiologiasta ei kuitenkaan ole saatu lopullista näyttöä, ja on edelleen epäselvää, mikä laukaisee VKH: n autoimmuunivasteen .
Patofysiologia
VKH: ssa on neljä klassista vaihetta, joilla voi olla vaihtelevia esityksiä: prodromaalinen, akuutti uviittinen, toipilas ja krooninen-uusiutuva. Histopatologiset muutokset alkavat tyypillisesti akuutissa vaiheessa .
akuutille uveitic-vaiheelle on ominaista granulomatoottisen tulehduksen aiheuttama molemminpuolinen uveaalinen paksuuntuminen. Granuloomat koostuvat lymfosyyteistä, makrofageista sekä rakeiden täyttämistä epitelioideista ja jättisoluista . Vaikka epitelioidisolujen uskottiin aiemmin olevan muuttuneita melanosyyttejä, immunohistokemiallinen seurantatutkimus antoi viitteitä sen sijaan kudosmakrofagien alkuperästä . Granuloomat täynnä epitelioidi histiocytes, kutsutaan Dalen-Fuchs kyhmyt, voidaan usein nähdä välillä verkkokalvon pigmentti epiteelin (RPE) ja Bruch n kalvo. Uveal granulomatoottinen tulehdus johtaa suonikalvon paksuuntumista ja eksudatiivinen verkkokalvon irtaumia täynnä proteinaceous nestettä. Lisäksi plesosytoosi (i.e., lisääntynyt solumäärä) voi esiintyä etukammiossa ja lasiaisessa .
toipilasvaihe tunnistetaan suonikalvon ja silmän ulkopuolisten alueiden, myös periokulaarisen ihon ja hiusten depigmentaatiosta. Vaaleaa näköhermoa vasten asetettu depigmentoitu suonikalvo antaa vaikutelman ”auringonlaskun hehkuvasta” silmänpohjasta, mikä on klassinen piirre tässä VKH-vaiheessa . Lisäksi Dalen-Fuchs-kyhmyt tulevat selvemmin RPE: n alle toipilasvaiheessa .
kroonisesti uusiutuvalle vaiheelle on ominaista suonikalvon paksuuden väheneminen, vakavien verkkokalvon irtaumien häviäminen, krooninen lievä vitriitti ja toistuva granulomatoottinen anteriorinen segmentin tulehdus. Suonikalvon neovaskularisaatio (CNV) ja subretinaalinen fibroosi voivat kehittyä tämän vaiheen aikana ja ovat vakavan taudin etenemisen indikaattoreita . Kaihi ja toissijainen glaukooma ovat muita komplikaatioita pitkäaikainen tai toistuva tulehdus tässä vaiheessa .
epidemiologia
VKH on yleistä roduilla, joilla on tummempi ihopigmentti, erityisesti aasialaisilla, Eteläamerikkalaisilla, Lähi-idän asukkailla ja Alkuperäisamerikkalaisilla. VKH-taudin osuus on >10% uveiitista näissä populaatioissa . Vain 1-4 prosentissa uveiittitapauksista arvellaan olevan sekundaarisia VKH-taudille Yhdysvalloissa (7). Yhdysvalloissa useimpien VKH-tapausten on todettu vaikuttavan aasialaisiin, latinalaisamerikkalaisiin ja / tai alkuperäisamerikkalaisiin ihmisarvoisiin . Mielenkiintoista on, että VKH-tauti tarttuu harvoin afrikkalaisiin tummasta pigmentistä huolimatta . VKH-taudin esiintyvyys vaihtelee suuresti naapurimaiden rodullisten alaryhmien välillä . Esimerkiksi Koreassa VKH: n esiintyvyys on vain 2%, paljon pienempi kuin Japanissa ja Kiinassa .
VKH: lla on tyypillinen 20-50 vuoden ikä ; tutkimusten mukaan kuitenkin 3, 1-13, 4% VKH-tapauksista on lapsipotilaita ja 10% ≥65-vuotiaita . Klassisesti VKH: lla ajatellaan olevan mieltymys naissukupuoleen, ja vaikka useimmat tutkimukset osoittavat, että VKH vaikuttaa suhteettomasti naisiin, muutamissa tutkimuksissa on osoitettu, että VKH: lla on miespuolinen alttius tai ei ole sukupuolista alttiutta .
merkit/oireet
kuten edellä todettiin, VKH-taudin neljä vaihetta ovat prodromaalinen, uviittinen, toipilas ja krooninen uusiutuva. Jokaisella vaiheella on erilliset kliiniset piirteet.
- Prodromaali: tämä alkuvaihe voi esiintyä influenssan kaltaisena sairautena, johon liittyy pääasiassa yleisoireita, kuten päänsärkyä, huimausta, kuumetta, väsymystä ja / tai pahoinvointia. Neurologisia oireita aivokalvontulehdus, kallon hermo palsies, ja näköhermon tulehdus, sekä kuulo-oireita tinnitus, dysakusis, ja huimaus on raportoitu . Valonarkuus, näön hämärtyminen, kellunta ja/tai silmäkipu alkavat yleensä 48 tunnin kuluessa prodromaalisista oireista . Prodromaalinen vaihe kestää tyypillisesti muutamasta päivästä viikkoihin.
- akuutti Uveitic: tähän vaiheeseen kuuluu sumea näkö, valonarkuus, sidekalvon pistos ja silmäkipu. Voi olla lievä anterior uveiitti, joka aluksi näyttää ei-granulomatoottinen. Yksipuolinen alkaa tyypillisesti siirtymiä kahdenvälinen osallistuminen sisällä 1-2 viikkoa. Granulomatoottinen anteriorinen uveiitti, johon liittyy lampaanrasvan keraattisia saostumia, voi kehittyä. Posterior tentti havainnot voivat olla näköhermon turvotus ja hyperemia , multifocal alueilla choroiditis, useita alueita vakavien verkkokalvon irtaumia lokalisoitu posteriorisen silmänpohjan, suonikalvon paksuuntuminen, säteilevä chorioretinal taittuu, ja vitriitti . Serous verkkokalvon irtaumat voivat muodostaa apilanlehtikuvion posterior silmänpohjan ja voi edetä laaja rakkulainen irtaumia vaikeissa tapauksissa . Akuutti tulehduksellinen glaukooma on liittynyt tähän taudin vaiheeseen ja voi esittää matala etukammion toissijainen sädekehän turvotus, jäljittelemällä akuutti kulma sulkeminen . Akuutin uveitic-vaiheen kesto riippuu nopeasta diagnoosista ja hoidosta.
- krooninen Uveitic tai toipilas: tämä vaihe kehittyy tyypillisesti useita viikkoja akuutin vaiheen jälkeen ja on ominaista vitiligo (esim., kasvot, kädet, hartiat, tai takaisin), polioosi, ja hiustenlähtö. Depigmentaatio lähellä sarveiskalvon limbus, tunnetaan Sugiura merkki, voidaan nähdä kuukauden kuluttua taudin puhkeamisesta ; kuitenkin, tämä merkki on harvoin nähtävissä ulkopuolella Japanin väestöstä . Suonikalvon depigmentaatio tapahtuu yleensä muutaman kuukauden aikana, ja tuloksena on suonikalvon kirkkaan oranssi-punainen väri ja klassinen ”sunset glow fundus.”Sunset glow silmänpohjan uskotaan olevan tärkein ja ennustavin kroonisen VKH: n diagnosoinnissa . Hyvin määritelty, pyöreä, nummular chorioretinal arvet voivat muodostua Keski-reuna. Krooninen uveitic-vaihe kestää tyypillisesti useita kuukausia.
- krooninen-toistuva: Tämä vaihe on ominaista toistuvat jaksot granulomatous anterior uveiitti lampaan rasva keratic saostuu, iiris kyhmyt, iiris depigmentaatio, posterior synekiae, posterior subcapsular kaihi, toissijainen glaukooma, suonikalvon neovaskulaarinen kalvot, ja, lopulta, subretinal fibroosi ja nummular chorioretinal atrofia . Krooninen vaihe kehittyy tyypillisesti vähintään kuusi kuukautta alustavan esittämisen jälkeen. Vakavien verkkokalvon irtaumat, jotka ovat läsnä akuutin ja toipilasvaiheen aikana, eivät tyypillisesti toistu aggressiivisella kortikosteroidihoidolla .
diagnostiset kriteerit
uusimmat diagnostiset kriteerit, jotka nimettiin VKH: n tarkistetuiksi Diagnostisiksi kriteereiksi (Revised Diagnostic Criteria, RDC), määriteltiin vuonna 1999 ensimmäisessä kansainvälisessä VKH: ta käsittelevässä työpajassa . Ne on esitetty taulukossa 1. RDC: t ovat hyödyllisiä siinä mielessä, että ne jakavat VKH: n kolmeen eri diagnostiseen luokkaan sen sairauden vaiheen perusteella, jonka aikana potilas esiintyy: täydellinen, epätäydellinen ja todennäköinen. Tämä sairauden luokittelu mahdollistaa asianmukaisen ja varhaisen hoidon ” todennäköisessä ”sairaudessa, joka voi auttaa estämään etenemisen” täydelliseksi ” sairaudeksi.
muiden silmätulehduksen syiden, sekä tarttuvan että autoinflammaattisen, tutkiminen on välttämätöntä. Näitä voivat olla punasolujen sedimentaationopeus (ESR), C-reaktiivinen proteiini (CRP), tuberkuloosin kvantiferon-Gold-määritys, syfiliksen nopea plasmareagiini (RPR), angiotensiinikonvertaasientsyymi (ACE) ja rintakehän röntgenkuvaus sarkoidoosin, tumavasta-aineen (ANA) ja p-/c-Anca. Myös, historia viime silmävamma tai silmänsisäinen leikkaus on huomattava ja todennäköisesti viittaa sympaattinen oftalmia (SO) todennäköisempi diagnoosi, koska hyvin samanlainen esitys ja patofysiologia jaettu SO ja VKH .
epäselvissä tapauksissa VKH-diagnoosin tueksi voidaan tehdä lumbaalipunktio lymfosyyttisen ja monosyyttisen plesosytoosin löytämiseksi; tätä käytetään kuitenkin harvoin kliinisesti. Kahdeksankymmentä prosenttia potilaista on plesosytoosi aivo-selkäydinnesteessä (CSF) viikon sisällä ja 97% on plesosytoosi kolmen viikon kuluessa. Kohonneet immuunisoluarvot voivat kestää jopa kahdeksan viikkoa taudin puhkeamisen jälkeen . T-solujen pintamarkkeriprofiilit ovat samanlaiset aivo-selkäydinnesteen ja kammionesteen välillä, mutta poikkeavat verestä. Tämä viittaa aivo-selkäydinnesteen kykyyn heijastaa tarkasti uveaalitulehdusta VKH-taudissa .
Taulukko 1. Tarkistetut Vogt-Koyanagi-Haradan taudin
*diagnostiset kriteerit taulukosta 1 (15).
”täydellinen Vogt-Koyanagi-Haradan tauti (kriteerien 1-5 on oltava olemassa)
- ei ole esiintynyt läpitunkevaa silmävammaa tai leikkausta ennen uveiitin ensimmäistä puhkeamista.
- ei kliinisiä tai laboratoriokokeita, jotka viittaisivat muihin silmäsairauksiin.
- molemminpuolinen silmävamma (a tai b on täytettävä, riippuen sairauden vaiheesta, jolloin potilas tutkitaan).
- sairauden varhaiset ilmenemismuodot.
- täytyy olla näyttöä diffuusista koroidiitista (johon voi liittyä anteriorinen uveiitti, lasiaisen tulehdusreaktio tai näköhermolevyn hyperemia), joka voi ilmetä yhtenä seuraavista:
- sairauden varhaiset ilmenemismuodot.
- subretinaalisen nesteen Polttopistealueet tai
- rakkulainen seroosi verkkokalvon irtauma.
- suonikalvon perfuusion polttoväli, monipaikkaiset vuotoalueet, suuret läiskälealueet hyperfluoresenssissa, kerääntyminen subretinaalinesteen sisälle, näköhermon värjäytyminen (lueteltu peräkkäisessä järjestyksessä) fluoreseiinin angiografiassa ja
- diffuusi suonikalvon paksuuntuminen, ilman merkkejä posteriorisesta skleriitistä ultraäänitutkimuksessa.
- historia viittaa aikaisempaan 3a: n löydöksiin ja joko sekä (2) että (3) alapuolella tai useita merkkejä (3):
- Silmänpigmentaatio (jompikumpi seuraavista ilmenemismuodoista on riittävä): (a) Sunset glow fundus tai (b) Sugiura-merkki.
- muut silmäoireet:
- nummelaisen korioretinaalisen depigmentoituneet arvet, tai
- verkkokalvon pigmenttiepiteelin paakkuuntuminen ja/tai migraatio, tai
- uusiutuva tai krooninen anteriorinen uveiitti.
- Meningismus (huonovointisuus, kuume, päänsärky, pahoinvointi, vatsakipu, niskan ja selän jäykkyys tai näiden yhdistelmä; päänsärky ei kuitenkaan yksin riitä täyttämään meningismuksen määritelmää), tai
- Tinnitus tai
- aivo-selkäydinnesteen pleosytoosi.
- alopesia eli
- Polioosia eli
- vitiligoa.
vaillinainen Vogt-Koyanagi-Haradan tauti (kriteerien 1-3 ja joko 4 tai 5 tulee olla olemassa)
- ei ole aiemmin esiintynyt läpitunkevaa silmävammaa tai leikkausta ennen uveiitin ensimmäistä puhkeamista, ja
- ei ole kliinistä tai laboratorioaineistoa, joka viittaisi muihin silmätautiyksiköihin, ja
- molemminpuolinen silmän osallisuus.
- neurologiset/kuulolöydökset; sellaisina kuin ne on määritelty täydelliselle Vogt-Koyanagi-Haradan taudille edellä tai
- Kokonaislöydöksille; sellaisina kuin ne on määritelty täydelliselle Vogt-Koyanagi-Haradan taudille edellä.
todennäköinen Vogt-Koyanagi-Haradan tauti (eristetty silmätauti; kriteerien 1-3 on oltava olemassa)
- ei ole esiintynyt läpäisevää silmävammaa tai leikkausta ennen uveiitin ensimmäistä puhkeamista.
- ei kliinisiä tai laboratoriokokeita, jotka viittaisivat muihin silmäsairauksiin.
- kahdenvälinen silmävamma siten kuin edellä on määritelty täydellisen Vogt-Koyanagi-Haradan taudin osalta. ”
testaus / Laboratoriotyöskentely
VKH: n alkutyössä tulisi harkita seuraavien testien tekemistä:
- optinen koherenssitomografia (OCT): Akuutissa uveitic-vaiheessa OCT näyttää todennäköisesti merkittäviä suonikalvon paksuuntumista ja serosseja verkkokalvon irtaumia. Subretinaalinesteen kertymissä voi olla septaatioita, joiden uskotaan olevan fibriinikalvoja ja tulehdustuotteita, luoden lobulaarisen rakenteen, joka voidaan nähdä myös fluoreseiinin angiografiassa. Vuonna toipilas vaiheessa, OCT voi havaita alueita verkkokalvon ohenemista jälkeen ratkaistu tulehdus jälkeen kortikosteroidihoito .
- b-scan ultrasonography: Akuutissa vaiheessa, ultraäänitutkimus voi näyttää diffuusi posterior suonikalvon paksuuntuminen, posterior kovakalvon paksuuntuminen, verkkokalvon irtaumia, ja lasiaisen samentumia . Sädekehää voidaan havaita ultraäänibiomikroskopian yhteydessä . Tämä testi on myös hyödyllistä sulkea pois posterior scleritis.
- Fluoreseiiniangiografia (FA): klassisesti FA paljastaa alkuvaiheessa multifokaalisia suonikalvon hypofluoresoivia pisteitä, joita myöhäisessä vaiheessa seuraa useita fokaalisia hyperfluoresoivia alueita, joilla esiintyy hajavuotoja . Väriaine vuotaa RPE: n läpi ja kerääntyy hyperfluoresoivia pisteitä ympäröivään subretinaaliseen tilaan. FA voi olla diagnostisesti hyödyllinen, kun VKH tauti esiintyy ilman ylimääräisiä oireita. Optinen levy hyperfluoresenssi ja ikkunan vikoja aiheuttama atrofinen chorioretinal arvet voidaan nähdä Keski-reuna . FA VKH-taudin kroonisessa toistuvassa vaiheessa näkyy epäspesifisiä ikkunavirheitä, jotka johtuvat RPE-vaurioista, suonikalvon uuvaskularisaatiosta ja subretinaalisesta fibroosista .
- Indosyaniinivihreä (ICG) angiografia: Varhaisen vaiheen ICG kuvaa hyperfluoresoivia stroomalastuja, jotka osoittavat suonikalvon vaskulopatiaa ja hypofluoresoivia tummia pisteitä, jotka vastaavat granuloomia ja suonikalvon verisuonituksen viivästynyttä hajanaista täyttymistä . Myöhäinen vaihe paljastaa sumeita stroomia ja diffuusia suonikalvon hyperfluoresenssia. Välilevyn hyperfluoresenssi viittaa vakavaan sairauteen. ICGA voi havaita subkliinisen suonikalvon tulehduksen hyvin varhaisessa vaiheessa tai jopa systeemisen hoidon jälkeen .
- lannepisto: plesosytoosia aivo-selkäydinnesteessä esiintyy suurimmalla osalla VKH-potilaista. Lannepisto tulee tehdä sairauden alkuvaiheessa, koska pleosytoosi voi ratkaista
hoito/Hoito/ohjeet
VKH: n hoitotavoitteisiin kuuluu aktiivisen tulehduksen varhainen diagnosointi ja tukahduttaminen sekä uusiutuvien tulehdusten ja näköuhkaavien komplikaatioiden, kuten glaukooman, verkkokalvon rakkulaisen irtauman ja suonikalvon uudissuonittumisen ehkäisy.
systeeminen kortikosteroidihoito on ensisijainen vaihtoehto VKH-taudin hoidossa, erityisesti akuutin uveitic-vaiheen aikana. On osoitettu, että kortikosteroidien antoreitti (suun kautta tai laskimoon) ei vaikuta näöntarkkuuteen tai visuaalisesti merkittävien komplikaatioiden esiintymiseen akuutin VKH: n hoidossa . Vaikean sairauden hoidossa ehdotettu protokolla on metyyliprednisolonin antaminen laskimoon kolmen päivän ajan ja sen jälkeen suuriannoksinen prednisonihoito suun kautta. Lievässä tai keskivaikeassa sairaudessa suuriannoksinen oraalinen prednisoni voi riittää annoksella 1-2 mg/kg/vrk. Steroidiannos on hitaasti kapeneva noin kuuden kuukauden aikana toistumisen estämiseksi . Aggressiivinen varhainen hoito, rinnalla sarja FA testaus osoittaa katoaminen väriaine vuoto kautta RPE, voi auttaa estämään edelleen taudin etenemistä, toistuminen, ja ekstraocular ilmenemismuotoja . Ajankohtaisia steroideja ja cycloplegics voi vähentää solujen etukammion ja lasiaisen.
Triamsinolonia on käytetty silmänsisäisen tulehduksen lyhytaikaiseen hallintaan akuutin tai toistuvan vaiheen aikana.; näitä paikallisia hoitoja tulee harkita, jos kyseessä on vastahakoinen sairaus ja potilailla, jotka sietävät huonosti steroidien epäedullisia systeemisiä sivuvaikutuksia, kun otetaan huomioon laajennettu steroidien kartio. Intravitreaalisia anti-VEGF-injektioita käytetään joskus suonikalvon uuvaskularisaation säätelyyn ja silloin, kun kyseessä on pysyvä, vakava verkkokalvon irtauma .
steroideja säästäviä lääkkeitä, mukaan lukien antimetaboliitit, kalsineuriinin estäjät, biologiset lääkkeet, TNF-alfan estäjät tai sytotoksiset aineet, voidaan käyttää VKH: n hoitoon, ja niitä tulee seurata huolellisesti, usein yhteistyössä reumatologian kanssa . Ei-steroidisten immunosuppressiivisten aineiden käytöstä VKH-taudin ensilinjan hoitona on keskusteltu jatkuvasti. Tuoreessa tutkimuksessa ei kuitenkaan havaittu eroja varhaisen ensilinjan immunomodulatorisen hoidon (IMT) ja pelkän prednisonihoidon välillä . Lisäksi immunosuppressiiviset ja biologiset hoidot ovat kalliita ja vaativat huolellista hoitoa edeltävää arviointia sekä tiheää veriarvojen seurantaa vakavien haittavaikutusten arvioimiseksi.
kroonisessa toistumisvaiheessa toistuva uusiutuminen saattaa viitata kortikosteroidilääkityksen resistenssiin ja steroideja säästävän immunomodulatorisen hoidon tarpeeseen . Ensisijainen aine steroidiresistentti toistumisen tai steroidi-intoleranssi on siklosporiini . Infliksimabi, rituksimabi, adalimumabi ja alfa-2a-interferoni ovat biologisia aineita, joita on käytetty myös refraktaarisen uveiitin hoitoon VKH-taudissa.
akuuttiin VKH: hon usein liittyvän anteriorisen uveiitin hoitoon tulee määrätä paikallisesti steroideja (esim.prednisoloniasetaatti 1%) ja paikallisesti cyloplegiaa (esim. syklopentolaatti 1% tai atropiini 1%) etukammion tulehduksen asteesta riippuen.
Silmäkomplikaatiot liittyvät yleisesti VKH-tautiin. Koska potilaan VKH-hoito voi olla monivaiheista ja esitystapojen vaihtelua, hoito voi monissa tapauksissa viivästyä. Vakavissa VKH-muodoissa ja toistuvina silmänsisäinen tulehdus voi olla vaikea hallita ja se voi aiheuttaa rakenteellisia vaurioita. Yli 50%: lle potilaista kehittyy tähän liittyviä komplikaatioita, kuten kaihi, sekundaarinen glaukooma, suonikalvoston neovaskulaariset kalvot, subretinaalinen fibroosi tai näiden yhdistelmä (kuva 6) .
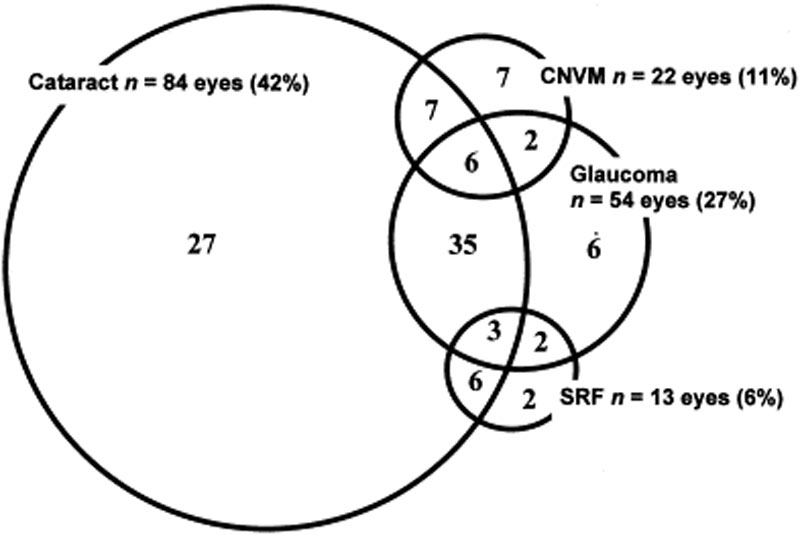
kuva 6: Venn-kaavio VKH-potilaiden komplikaatioista. (Käytetään Am J Ophthalmolin luvalla. 2001;131(5):599-606 )
epidemiologia ja etiologia
|
SIGNS
|
oireet
|
hoito/hoito
|
- Du L, Kijlstra A, Yang P. Vogt-Koyanagi-Harada disease: Novel insights into patofysiology, diagnosis and treatment. Prog Retin Eye Res 2016; 52: 84-111. https://PubMed.gov/26875727. DOI: 10.1016 / j.preteyeres.2016.02.002
- Yamaki K, Gocho K, Hayakawa K, Kondo I, Sakuragi S. tyrosinaasi-suvun proteiinit ovat Vogt-Koyanagi-Haradan taudille ominaisia antigeenejä. J Immunol 2000; 165(12): 7323-7329. https://PubMed.gov/11120868
- Horie Y, Takemoto Y, Miyazaki a, Namba K, Kase s, Yoshida K, Ota M, Hasumi Y, Inoko H, Mizuki n, Ohno S. Tyrosinaasi-geeniperhe ja Vogt-Koyanagi-Haradan tauti japanilaisilla potilailla. Mol Vis 2006; 12: 1601-1605. https://PubMed.gov/17200659
- ng JY, Luk FO, Lai TY, Pang CP. Vogt-Koyanagi-Haradan taudin molekyyligenetiikan vaikutus. 2014; 4: 20. https://PubMed.gov/25097674. DOI: 10.1186 / s12348-014-0020-1
- Bowling B. Uveitis. Kanski ’ s Clinical Oftalmology New York, New York: Elsevier; 2016; chapter 11; s. 395-465.
- Yeh PT YC, Yang CH, Lin CP. Ei-Rhegmatogeeninen Verkkokalvon Irtauma. Vuonna: Schachat AP SS, Hinton DR, Wilkinson CP, Wiedemann P,, toimittaja. Ryanin verkkokalvo. New York: Elsevier; 2018; chapter 99; s. 1828-1849.
- Goto H RK, Rao N. Vogt–Koyanagi–Haradan tauti. In: Schachat AP SS, Hinton DR, Wilkinson CP, Wiedemann P, editor. Ryanin verkkokalvo. New York, New York: Elsevier; 2018; chapter 78; s. 1505-1515.
- Riddington L, Hall AJ, Tait B, Nicholson I, Varney M. Vogt-Koyanagi-Haradan oireyhtymä potilailla, joilla on vietnamilaisia sukujuuria. Aust N Z J Ophthalmol 1996;24(2): 147-149. https://PubMed.gov/9199747
- Sugita s, Takase H, Kawaguchi T, Taguchi C, Mochizuki M. Vogt-Koyanagi-Haradan tautia sairastavien T-solujen aiheuttama tyrosinaasipeptidien ja sytomegalovirusantigeenin välinen ristireaktio. Int Ophthalmol 2007; 27(2-3):87-95. https://PubMed.gov/17253112. DOI: 10.1007 / s10792-006-9020-y
- Freund BK SD, Mieler WF, Yannuzzi LA. Tulehdus. Verkkokalvokartasto. New York, New York: Elsevier 2017; chapter 4; s. 279-398.
- Rao N. Vogt-Koyanagi-Haradan tauti. In: J YMaD, toimittaja. Silmätaudit. New York, New York: Elsevier; 2014; luku 7.17; s. 761-763.
- Rao NA, Xu S, Font RL. Sympaattinen oftalmia. Immunohistokemiallinen tutkimus epitelioideista ja jättisoluista. Oftalmologia 1985; 92 (12): 1660-1662. https://PubMed.gov/4088616
- Nussenblatt RB. Vogt-Koyanagi-Haradan Syndrooma. In: Whitcup RBNaSM, toimittaja. Uveiitti: perusteet ja kliininen käytäntö. 4th Edition ed: Elsevier; 2010; chapter Chapter 24.
- Read RW, Holland GN, Rao NA, Tabbara KF, Ohno s, Arellanes-Garcia L, Pivetti-Pezzi P, Tessler HH, Usui M. Revised diagnostic criteria for Vogt-Koyanagi-Harada disease: report of an international committee on nomenclature. Am J Oftalmol 2001;131 (5): 647-652. https://PubMed.gov/11336942
- Chung H, Choi DG. Uveiitin kliininen analyysi. Korean J Oftalmol 1989; 3(1): 33-37. https://PubMed.gov/2795939. DOI: 10,3341 / kjo.1989.3.1.33
- Abu El-Asrar AM, Al-Kharashi AS, Aldibhi H, Al-Fraykh H, Kangave D. Vogt-Koyanagi-Haradan tauti lapsilla. Silmä (Lond) 2008;22(9):1124-1131. https://PubMed.gov/17479116. DOI: 10.1038 / sj.silmä.6702859
- Martin TD, Rathinam SR, Cunningham ET. Yleisyys, kliiniset ominaisuudet ja näön menetyksen syyt Vogt-Koyanagi-Haradan tautia sairastavilla lapsilla Etelä-Intiassa. Retina 2010;30 (7): 1113-1121. https://PubMed.gov/20168275. DOI: 10.1097 / IAE.0b013e3181c96a87
- Forster DJ, Green RL, Rao NA. Vogt-Koyanagi-Haradan oireyhtymän yksipuolinen ilmentymä 7-vuotiaassa lapsessa. Am J Oftalmol 1991;111 (3): 380-382. https://PubMed.gov/2000916
- Yamamoto Y, Fukushima A, Nishino K, Koura Y, Komatsu T, Ueno H. Vogt-koyanagi-Haradan tauti, joka puhkeaa 68-89-vuotiailla iäkkäillä potilailla. Jpn J Ophthalmol 2007; 51(1): 60-63. https://PubMed.gov/17295144. DOI: 10.1007 / s10384-006-0379-0
- Wang Y, Chan CC. Sukupuolierot vogt-koyanagi-Haradan taudissa ja sympaattisessa oftalmiassa. J Oftalmol 2014;2014: 157803. https://PubMed.gov/24734166. DOI: 10.1155/2014/157803
- Nakao K, Abematsu N, Mizushima Y, Sakamoto T. Optic disc turvotus Vogt-Koyanagi-Haradan taudissa. Invest Ophthalmol Vis Sci 2012; 53 (4): 1917-1922. https://PubMed.gov/22408010. DOI: 10.1167 / iovs.11-8984
- Rao NA, Gupta A, Dustin L, Chee SP, Okada AA, Khairallah M, Bodaghi B, Lehoang P, Accorinti M, Mochizuki M, Prabriputaloong T, Lue RW. Vogt-Koyanagi-Haradan taudin kliinisten erityispiirteiden erottamistiheys. Ophthalmology 2010;117(3):591-599, 599.e591. https://PubMed.gov/20036008. DOI: 10.1016/j.ophtha.2009.08.030
- Veerappan M, Fleischman D, Ulrich JN, Stinnett SS, Jaffe GJ, Allingham RR. The Relationship of Vogt-Koyanagi-Harada Syndrome to Ocular Hypertension and Glaucoma. Ocul Immunol Inflamm 2017;25(6):748-752. https://PubMed.gov/27438521. DOI: 10.1080/09273948.2016.1189578
- Baltmr A, Lightman S, Tomkins-Netzer O. Vogt-Koyanagi-Harada syndrome – current perspectives. Clin Ophthalmol 2016;10:2345-2361. https://PubMed.gov/27932857. DOI: 10.2147/OPTH.S94866
- Kitaichi N, Matoba H, Ohno S. lumbaalipunktion positiivinen rooli Vogt-Koyanagi-Haradan taudin diagnosoinnissa: lymfosyyttien osaset kammionesteessä ja selkäydinnesteessä. Int Ophthalmol 2007; 27(2-3):97-103. https://PubMed.gov/17211585. DOI: 10.1007 / s10792-006-9016-7
- Oshima Y, Harino s, Hara Y, Tano Y. Indosyaniinivihreät angiografiset löydökset Vogt-Koyanagi-Haradan taudissa. Am J Oftalmol 1996;122(1): 58-66. https://PubMed.gov/8659599
- Lue RW, Yu F, Accorinti M, Bodaghi B, Chee SP, Fardeau C, Goto H, Holland GN, Kawashima H, Kojima E, Lehoang P, Lemaitre C, Okada AA, Pivetti-Pezzi P, Secchi A, Katso RF, Tabbara KF, Usui M, Rao NA. Evaluation of the effect on outcomes of the antoreitti of kortikosteroidic in acute Vogt-Koyanagi-Harada disease. Am J Oftalmol 2006;142(1): 119-124. https://PubMed.gov/16815259. DOI: 10.1016 / J.ajo.2006.02. 049
- Rubsamen PE, Gass JD. Vogt-Koyanagi-Haradan syndrooma. Kliininen kurssi, hoito ja pitkäaikainen visuaalinen tulos. Arch Ophthalmol 1991;109(5):682-687. https://PubMed.gov/2025171
- Urzua CA, Velasquez V, Sabat P, Berger O, Ramirez s, Goecke a, Vásquez DH, Gatica H, Guerrero J. aikaisempi immunomoduloiva hoito liittyy parempiin visuaalisiin tuloksiin Vogt-Koyanagi-Haradan tautia sairastavien potilaiden alaryhmässä. Acta Ophthalmol 2015; 93 (6): e475-480. https://PubMed.gov/25565265. DOI: 10.1111 / aos.12648
- Read RW, Rechodouni A, Butani n, Johnston R, LaBree LD, Smith RE, Rao NA. Vogt-Koyanagi-Haradan taudin komplikaatiot ja ennustavat tekijät. Am J Oftalmol 2001;131 (5): 599-606. https://PubMed.gov/11336934
Suggested Citation Format
Mai ap, Tran C, Wilson CW, Fox AR, Boldt HC. Vogt-Koyanagi-Haradan (VKH) tauti. EyeRounds.org Huhtikuuta 2019. Saatavilla http://EyeRounds.org/cases/284-vogt-koyanagi-harada.htm
 tr>
tr>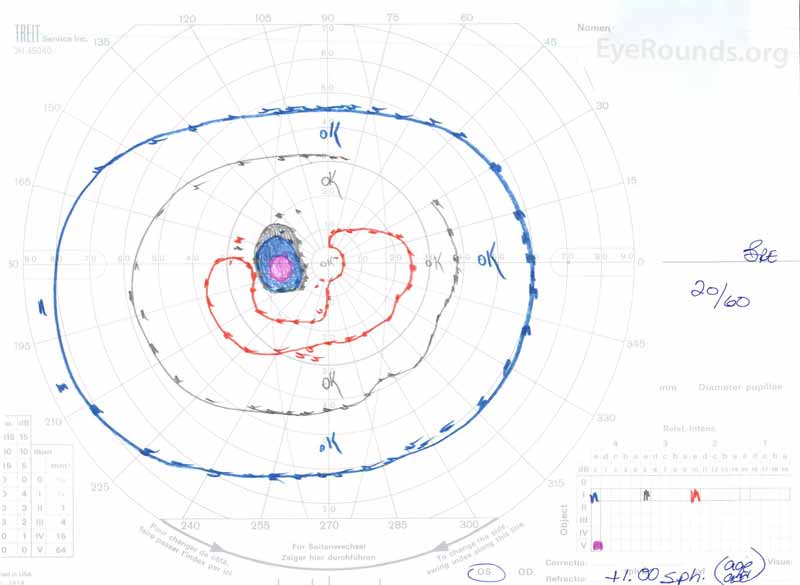
Leave a Reply