Suljettu systeemi
klassisessa mekaniikassa
ei-relativistisessa klassisessa mekaniikassa suljettu systeemi on fysikaalinen systeemi, joka ei vaihda mitään ainetta ympäristönsä kanssa, eikä siihen kohdistu mitään nettovoimaa, jonka lähde on systeemin ulkopuolinen. Suljettu systeemi klassisessa mekaniikassa vastaisi eristettyä systeemiä termodynamiikassa. Suljettuja järjestelmiä käytetään usein rajoittamaan tekijöitä, jotka voivat vaikuttaa tietyn ongelman tai kokeen tuloksiin.
termodynaamikoissa
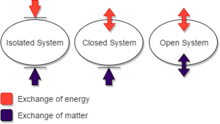
termodynamiikassa suljettu systeemi voi vaihtaa energiaa (lämpönä tai työnä) mutta ei ainetta, jonka surroundings.An eristetty järjestelmä ei voi vaihtaa lämpöä, työtä tai ainetta ympäristön kanssa, kun taas avoin järjestelmä voi vaihtaa energiaa ja ainetta. (Tätä termin määritelmää ei käytetä yhdenmukaisesti, vaikka se on kätevä joihinkin tarkoituksiin. Erityisesti jotkut kirjoittajat käyttävät ”suljettua järjestelmää”, jossa tässä käytetään ”eristettyä järjestelmää”.)
yksinkertaisessa systeemissä, jossa on vain yksi hiukkastyyppi (atomi tai molekyyli), suljettu systeemi tarkoittaa vakiomääräistä hiukkasmäärää. Kemiallisen reaktion läpikäyvissä järjestelmissä reaktioprosessissa voi kuitenkin syntyä ja tuhoutua kaikenlaisia molekyylejä. Tällöin systeemin sulkeutuminen ilmaistaan toteamalla, että jokaisen alkuaineatomin kokonaismäärä säilyy riippumatta siitä, millaisen molekyylin osa se voi olla. Matemaattisesti:
∑ j = 1 m a i j n j = b i {\displaystyle \sum _{j=1}^{m}a_{ij}n_{j}=b_{i}}

missä N j {\displaystyle n_{j}}

on j-tyypin molekyylien lukumäärä, a i j {\displaystyle a_{IJ}}
on alkuaineen I atomien lukumäärä i}

molekyylissä J {\displaystyle j}

ja b i {\displaystyle b_ {I}}

on alkuaineen I {\displaystyle i} atomien kokonaismäärä

systeemissä, joka pysyy vakiona, koska systeemi on suljettu. On olemassa yksi tällainen yhtälö jokaiselle eri osa järjestelmässä.
termodynamiikassa suljettu systeemi on tärkeä monimutkaisten termodynaamisten ongelmien ratkaisemisessa. Sen avulla voidaan poistaa joitakin ulkoisia tekijöitä, jotka voivat muuttaa tuloksia kokeen tai ongelma siten yksinkertaistaa sitä. Suljettua systeemiä voidaan käyttää myös tilanteissa, joissa tarvitaan termodynaamista tasapainoa tilanteen yksinkertaistamiseksi.
Kvanttifysiikoissa
tämä Schrödingerin yhtälöksi kutsuttu yhtälö kuvaa eristetyn tai suljetun kvanttisysteemin eli määritelmän mukaan systeemin käyttäytymistä, joka ei vaihda informaatiota (eli energiaa ja / tai ainetta) toisen systeemin kanssa. Jos siis eristetty systeemi on jossakin puhtaassa tilassa |ψ(t) ∈ h hetkellä t, jossa H merkitsee systeemin Hilbertin avaruutta, tämän tilan aikakehitystä (kahden peräkkäisen mittauksen välillä).
i ℏ ∂ ∂ t ψ ( R , T ) = H ^ ψ ( R , T ) {\displaystyle I\hbar {\frac {\partial }{\partial t}}\psi \Left(\mathbf {r} ,t\right)={\hat {h}}\psi \Left(\mathbf {r} ,t\right)\,\!}


Leave a Reply