maksan tutkimus, häiriöt & hoito
saostumia sapessa on kutsuttu monilla nimillä, kuten sappiliete, sappirakkoliete, mikrolitiasis ja pseudolithiasis. Sappiliete diagnosoidaan parhaiten tutkimalla mikroskooppisesti tuoretta sappirakon sappinäytettä.1 biokemiallisesti liete koostuu limageeliin uponneista kalsiumklirubinaattirakeista ja kolesterolimonohydraattikiteistä. Nämä kalsiumsaostumat, joiden kolesterolikiteet ovat läpimitaltaan 50µ tai enemmän, tuottavat lietteelle tunnusomaisia ultraäänikaikuja. Muotoutuva mucin-geeli on ainutlaatuinen kerrospukeutumis-ja virtausominaisuuksiensa ansiosta.2 Sappiliete kuvattiin ensimmäisen kerran vuonna 1970 kynnyksellä ultraääni ja kuvattu matalan tason kaikuja, että kerros riippuvainen osa sappirakon ilman akustinen varjostus. Se on lähinnä ultraäänitutkimusdiagnoosi, mutta herkkyys vain 55%: lla ja potilailla, joilla on lietettä, on usein normaalit testitulokset. Sappirakon sisällön mikroskooppista tutkimusta pidetään kultastandardina sappilieteen diagnosoinnissa.3 sappirakon sappi voidaan saada aikaan endoskopia tai nasogastric putki pyrkimys pohjukaissuolen sisällön jälkeen infusing kolekystokiniini edistää sappirakon tyhjenemistä. Maksan sappi voidaan kerätä potilailta yhteisen sappitiehyen kautta T-putki salaojitus jälkeen kolekystektomia ja koledochotomy vuonna sappikivitauti ja/tai koledocholithiasis. Tämä malli voi antaa puhdasta maksan sapen arviointia varten melko pitkään.4 sappirakon merkitystä sapen lietteen ja myöhemmin sappikivien patogeneesissä on korostettava. Lietettä sisältävässä sappirakossa on havaittu liman liikaeritystä ja varhaista rauhasepiteeliä metaplasiaa. Rauhasepiteeli metaplasia johtaa sappirakon sapen limapitoisuuden kasvuun, mikä puolestaan johtaa kolesterolikiteiden nukleaatioon ja sappikivien muodostumiseen. Eräs immuunifluoresenssitutkimus sappilieteellä potilailla, joilla oli kolesterolia tai sappikivisekoituksia, osoitti, että sappirakon sapen ultracentrifugoinnin jälkeen puhdistettu sedimentti ilmeni vesicular-aggregaattien ja pigmenttihiukkasten seoksena, johon liittyi kolesterolikiteitä sisältävä muciini-geelimatriisi. Vaikka anioninen polypeptidifraktio ja aminopeptidaasi liitettiin pigmentteihin, IgA levisi tasaisesti ”ydinmäisten” rakenteiden kiteisiin osiin, ja albumiini ilmaantui sen ollessa läsnä satunnaisesti sijoitettuina pieninä täplinä.5 tärkein patogeeninen mekanismi mukana lietteen muodostumista on luultavasti sappirakon dismotility, ja valituilla potilailla toimenpiteet, joiden tarkoituksena on säilyttää riittävä sappirakon supistukset on osoitettu tehokkaasti estää lietteen kehitystä.6 sappirakon hypomotiliteetti on todettu potilailla, joilla on pitkäaikainen parenteraalinen kokonaisravinto ja suuri selkäydinvamma altistaa sappilieteen muodostumiselle. Sappilieteen kliininen kulku vaihtelee täydellisestä resoluutiosta etenemiseen sappikivien muodostumiseen. Se voi aiheuttaa komplikaatioita yleensä liittyy sappikivet, kuten sappikipu, akuutti kolekystiitti, ja akuutti haimatulehdus. Lietteen yleisyys väestössä on suhteellisen alhainen. Useat kliiniset tilat liittyvät kuitenkin erityisen suureen sappilietteen esiintyvyyteen, kuten raskaus, nopea painon lasku, täydellinen parenteraalinen ravitsemus (TPN), oktreotidihoito, luuydin tai kiinteä elinsiirto.6 keftriaksoni on yksi yleisimmin käytetyistä 3.sukupolven parenteraalisista kefalosporiineista, koska sillä on laaja mikrobilääkityksen kirjo, pitkä puoliintumisaika plasmassa, joka mahdollistaa kerran päivässä annon ja se voi jopa tunkeutua veri-aivoesteeseen. Keftriaksonilla voi olla mahdollisia komplikaatioita, jotka ovat sappiliete tai sappilitiasis ja jopa saostuminen virtsateissä, mutta nämä komplikaatiot voivat korjaantua, kun Keftriaksonihoito lopetetaan.7 lietteen luonnonhistoria riippuu altistavista riskitekijöistä. Prospektiivisessa tutkimuksessa, jossa potilaat saivat TPN: ää, 6%: lle potilaista kehittyi lietettä 3-6 viikossa, 50%: lle 4-6 viikossa ja 6-viikon kuluttua sen ilmaantuminen oli yleistä, mutta merkittävästi liete hävisi palauttamalla suun kautta otetun rehun kaikille potilaille 4-viikon loppuun mennessä.8 myös sappilietettä esiintyi useimmin raskauden aikana, mutta se oli yleensä oireeton ja hävisi usein spontaanisti synnytyksen jälkeen.9 selittämättömässä toistuvassa akuutissa haimatulehduksessa sappiliete on todettu etiologiaksi jopa kahdella kolmanneksella potilaista.10 Lee ym.2 tutkituissa sappirakon lietteen luonnollisessa kehityksessä havaittiin, että 50%: lla potilaista liete hävisi itsestään ja pysyi oireettomana 20%: lla potilaista; 5-15%: lle potilaista kehittyi sappikiviä ja 10-15%: lle potilaista kehittyi oireita, jotka vaihtelivat vaikeasta sappikivusta toistuvaan akuuttiin haimatulehdukseen tai ilman sitä.2
koska tällaista sappilietettä pidetään sappikivien esiasteena; siksi myös sappilieteen käsittely muistuttaa sappikivitauteja. Jos sappiliete on oheishavainto muista syistä tehdystä ultraäänitutkimuksesta, potilaalle on tarjottava odottavaa hoitoa ultraäänitutkimusten avulla. Potilaita, joilla ilmenee komplikaatioita tai vaikeita oireita, on hoidettava sen mukaisesti. Kolekystektomia on oireisen sappilieteen lopullinen ja kullanarvoinen hoito. Potilailla, joilla on haimatulehdus tai kolangiitti, jotka eivät ole leikkauskelpoisia, sphincterotomia on järkevä vaihtoehto kolekystektomialle.3 on jo osoitettu, että mucinin ja eri proteiinien kolesterolipitoisuus ja jakautumistapa on samanlainen sapen ”lietteen” sedimenteissä kuin kolesteroli-ja sappikivissä. Tämä viittaa siihen, että sapen ”liete” edustaa sappikivien muodostumisen varhaista vaihetta näillä potilailla.5 koska se on sappikivien esiaste ennemmin tai myöhemmin, se voi aiheuttaa komplikaatioita ja edellyttää kolekystektomiaa, joten hoito on välttämätöntä toiminnan välttämiseksi. Tärkein ei-invasiivinen ei-kirurginen lääketieteellinen hoito kolesteroli sappikivet edustaa edelleen suun litholyysi sappihappojen kanssa. Ensimmäinen onnistunut ja dokumentoitu kolesterolin sappikivien liukeneminen saavutettiin vuonna 1972 antamalla suun kautta chenodeoksikolihappoa (CDCA), joka on primaarinen tri-hydroksisappihappo. CDCA: n käyttö annosriippuvaisen aminotransferaasiarvojen nousun, seerumin pienitiheyksisen lipoproteiinikolesterolin nousun ja sappisuolan aiheuttaman ripulin kehittymisen vuoksi herätti huolta. Koska hydrofiilisempi ursodeoksikolihappo (UDCA) näytti olevan yhtä tehokas sappikiven liukenemisessa, mutta käytännössä vailla sivuvaikutuksia, se korvasi nopeasti CDCA: n ja edustaa kirjallisuudessa eniten tallennettua kokemusta.11 UDCA: n on myös katsottu hoitavan potilaita sapilieteellä. UDCA: n suotuisa vaikutus tässä tilassa on osoitettu kliinisessä tutkimuksessa, jossa idiopaattinen akuutti haimatulehdus on liittynyt mikroskooppisiin sappikiviin tai sapilieteeseen. Tässä tutkimuksessa UDCA: n Anto 3-6 kuukauden kuluessa esti sappikiven uusiutumisen ja useampia haimatulehdusjaksoja 44 kuukauden seurannassa.12
sappiliete, joka sisältää liikaa kolesterolia, luo sappirakon sallivan ympäristön muuttaen normaalia tasapainoa hydrofobisten sappihappojen ja sappirakon suojamekanismien välillä. Sappihapot stimuloivat reaktiivisten happilajien muodostumista, joka kykenee käynnistämään tulehdusprosessit ja kolekystiitti. Niinpä UDCA, vähentämällä ylimääräistä kolesterolia ja” neutraloimalla ” hydrofobiset sappihapot, palauttaa tasapainon aggressiivisten sappitekijöiden ja sappirakon suojamekanismien välillä.13 annamme UDCA 10-15mg/kg kehon paino / päivä 2 jaettuna annoksina ajaksi 4-6 viikkoa.
Didenko ym.14 salmonella-infektion merkitystä sapilieteessä tutkittiin valomikroskopian ja immuunisytokemian tutkimusten avulla S. typhimuriumin ja solususkulaaristen sappikomponenttien yhteisvaikutuksesta kokeellisessa mallissa ”sappibakteerit”.14 Tämän yhteisvaikutuksen osoitettiin johtuneen bakteeri-sappilietteen muodostumisesta. Bakteerien solunulkoiset Muko polysakkaridit matriisi ja flagella on ratkaiseva rooli lietteen muodostumisen mekanismissa.14 harvat Ultraäänitutkimukset vahvistivat myös salmonellan ja sapen lietemuodostumien positiivisen yhteyden eri potilasryhmien välillä.15,16 kun tämä seikka otetaan huomioon, käytimme antaa potilaillemme suun kautta ampisilliini annoksella 500 mg trice päivittäin vähintään kolme tai neljä viikkoa, koska ampisilliini ei ole vain kustannustehokas lääke, mutta tarjoaa myös moninaisia etuja. Se vaikuttaa dramaattisesti sapen lipidikoostumukseen suoraan. Se estää fosfolipidin ja kolesterolin sapen eritystä, mutta ei sappisuolaa, ja vähentää näin ollen kolesterolin mooliprosenttia sapessa. Lisäksi ampisilliini on voimakas kolereetti, joka lisää sapen tilavuutta 100%. Koska sappisuolan kokonaiseritys pysyi vakiona sapen tilavuuden kasvaessa, sapen suolapitoisuus laski 50% ampisilliinin annon aikana. Sapen lipidien erityksen estäminen ja sapen tilavuuden muutokset liittyvät sapen ampisilliinitasoihin ja ovat täysin palautuvia ampisilliinihoidon lopettamisen jälkeen. Ampisilliini-infuusion aikana havaittu sappitilavuuden kasvu johtuu todennäköisesti osmoottisesta kolereesista.17
perinteisten lääkkeiden aikakaudella Intiassa Ayurvedalla on hyvin rikas perintö erilaisten sairauksien, kuten keltaisuuden, hoitamiseen tuhannen vuoden ajalta. Lääkekasvit, joilla on hepatobiliaarinen vaikutustapa, ovat edelleen välttämättömiä terapeuttisia aineita kolestaasin hoidossa. Niitä kutsutaan cholagogs (edistää sapen virtausta maksasta ja sappirakon suolistoon) ja choleretics (lisää sapen tuotantoa). Yksi parhaiten tutkituista kolagogeista on silymariini maitoskasvaimesta Silybum marianum, joka on neljän isomeerisen flavonolignaanin seos; silibiniini (aktiivisin komponentti), isosilibiniini, silydianiini ja silychristiini.18 silymariini indusoi sappihappojen maksatuotantoa ja sappihaposta riippuvaista kolereesia, mutta ei vaikuta sappihaposta riippumattomaan sapen virtaukseen.19 kasvien sekundaariset metaboliset yhdisteet, joilla on cholagogue – vaikutustapa, ovat tärkeitä terapeuttisia aineita kolestaasin ja maksa-ja sappihäiriöiden hoidossa. Herbal cholagogues kohdistaa eri komponenttien monimutkainen sapen tuotanto ja eritys järjestelmä, ja käyttää niiden toimintaa kautta erilaisia reittejä, kuten kolekystokiniini-riippuvainen ja riippumaton sappirakon supistuminen, ylös-säätely sappihapposynteesin, stimulaatio sappisuolan vienti pumppu, monilääkeresistenssiproteiinin transporter järjestelmä, ja osmoottinen sappi virtaus.20
Ayurvedic-klassikoissa on mainittu hyvä määrä lääkkeitä ja niiden muotoiluja keltaisuuden hoitoon. Phalatrikadi kvatha (keittäminen), yksi tärkeimmistä arvostetuista muotoiluista, jotka mainitaan erilaisissa Ayurvedic-klassikoissa, on käytetty menestyksekkäästi antiikin ajalta.21 se sisältää kahdeksan kasviainesta eri suhteissa.21 Srivastava ym.4 arvioi falatrikadi kvathan antioksidanttiominaisuutta, jossa sappinäytteitä analysoitiin eri väliajoin ja tutkimuspisteitä siitä, että lääke alentaa merkittävästi sappinesteen oksidatiivista stressiä. Koska vapaiden radikaalien vamman on osoitettu liittyvän sappikivenmuodostukseen, vapaiden radikaalien muodostumisen väheneminen (oksidatiivinen stressi) parantaa sapen biokemiaa ja siten estää kiven muodostumista.4 tarjoamme joko tuoretta decoction annoksessa 20ml kahdesti päivässä tai tiivistetyssä muodossa tablettina annoksessa 500mg kolmesti päivässä.
ratkaisevasti oireetonta ja komplisoitumatonta sappilietettä sairastaville potilaille on annettava mahdollisuus toipua sairaudestaan tarjoamalla heille ”Srivastava-hoito sappilietettä varten”, joka sisältää oraalista ampisilliinia, UDCA: ta ja Phaltrikadi Kvathaa (keittäminen) tai Ghanbatia (tabletti) vähintään 45 päivän ajan, ruokavalion rasvarajoitus, runsas veden saanti ja välttäen kaikki sappikivitautien mahdolliset sekoittavat tekijät. Useimmilla potilailla sappiliete häviää ja sappirakko näyttää ultraäänitutkimuksissa täysin normaalilta (Kuva 1) (kuva 2). Laparoskooppinen kolekystektomia on edelleen kullanarvoinen hoito monimutkaiselle sappilieteelle. Mielestämme pitäisi yrittää välttää kolekystektomia oireettomissa ja jopa lievissä oireellisissa tapauksissa, koska useimmat potilaat antavat hyväksyttävän vastauksen konservatiiviseen hoitoon. Tällä voimme paitsi välttää tarpeetonta kallista kirurgista taakkaa terveydenhuoltojärjestelmään, mutta myös säästää stressiä meidän potilaiden ja ei vähiten huono sappirakon. Haluamme myös, että tutkijat pohtivat uusia ratkaisevia tutkimuskokeita, jotka auttavat meitä ymmärtämään paremmin sappilietteen patogeneesiä ja selventämään näiden ayurvedisten valmisteiden vaikutusmekanismia molekyylitasolla hoidon tieteelliseksi perustaksi. Olemme suunnitelleet hoito perustuu käytettävissä tieteellisiin tutkimuksiin ja perinteisen ayurvedic kirjallisuuden ja totesi, että integroitu lähestymistapa lääketieteen toimii upeasti ja se tarvitsee aikaa.
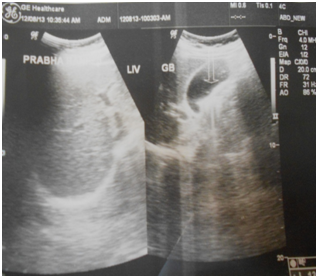
Figure 1 Pre-treatment ultrasonography scan showing biliary sludge.
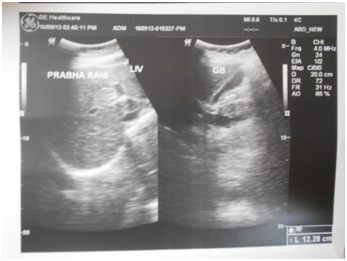
Figure 2 Post-treatment ultrasonography scan showing clear gallbladder lumen.
Leave a Reply