Kemoterapian Ekstravasaatioiden hoito
US Pharm. 2009;34(9)(onkologia suppl):3-11.
Abstrakti: laskimoon annettavat (IV) solunsalpaajalääkkeet voivat aiheuttaa ekstravasaatiovaurioita tai kudosnekroosia antopaikassa. Vaikka suurin osa ekstravasaatioista voidaan estää asianmukaisella ja perusteellisella infuusiolla, useita vastalääkkeitä on tunnistettu ja tutkittu uusien kudosvaurioiden estämiseksi.
infiltraatio ja ekstravasaatio ovat kaksi tunnettua, erillistä laskimonsisäisen Infuusiohoidon komplikaatiota. Infusion Nurses Societyn ja Oncology Nursing Societyn mukaan molempiin komplikaatioihin liittyy IV-liuoksen tahaton vuotaminen ympäröivään kudokseen; liuoksen tyyppi kuitenkin vaihtelee. Infiltraatio on epähuomiossa tapahtuva ei-syövyttävän tai ärsyttävän liuoksen tai lääkkeen antaminen ympäröiviin kudoksiin.1,2 Nonvesiantit ovat aineita, jotka harvoin aiheuttavat akuutteja reaktioita tai tuhoavat kudosta soluttautuessaan. Ärsyttävät aineet voivat aiheuttaa kipua pistoskohdassa tai suonessa, tulehdusreaktiolla tai ilman, yleensä ilman pysyviä kudosvaurioita. Ärsyttävät aineet voivat kuitenkin aiheuttaa pehmytkudoshaavoja vain, jos suuri määrä väkevää lääkeliuosta on epähuomiossa ekstravasoitu tulehdusreaktioiden aiheuttamiseksi ilman pysyviä kudosvaurioita.3, 4
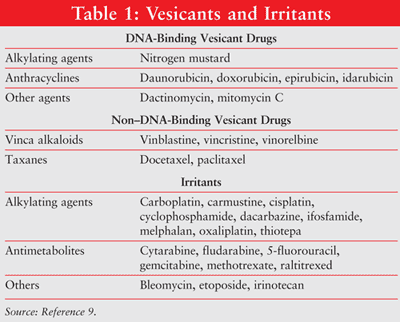
Ekstravasaatiolla tarkoitetaan rakkulamateriaalin tahatonta tiputtamista tai vuotamista suoneen ja ihon alle lääkityksen aikana.1, 2 ekstravasaatio aiheuttaa paikallisia reaktioita, jotka vaihtelevat paikallisesta ärsytyksestä ihon, sitä ympäröivän verisuoniston ja tukirakenteiden vakavaan kudoskuolioon.5-8 solunsalpaajia voidaan luokitella, koska ne voivat aiheuttaa paikallisia kudosvaurioita, kuten rakkuloita, ärsyttävät, tai nonvesicants. (Useita rakkuloita ja ärsyttäviä aineita on esitetty taulukossa 1.9) laskimonsisäisten lääkkeiden satunnaista ekstravasaatiota tapahtuu noin 0, 1-6%: ssa perifeerisen laskimonsisäisen infuusion infuusioista ja 0, 3-4, 7%: ssa implantoiduista laskimoportin infuusioista.10-12
kudosvaurion Patofysiologia
kudosvaurion laajuus riippuu solunsalpaajan sitoutumiskyvystä DNA: han. DNA: ta sitovia aineita ovat muun muassa antrasykliinit, antituumoriantibiootit, platinan analogit ja eräät alkyloivat aineet.3,4 DNA: ta sitovat antineoplastit aiheuttavat kudosvaurioita levittämällä tappavaa DNA: n ristisitoutumista tai vapaiden radikaalien aiheuttamia juosteita, jotka johtavat solun apoptoosiin.13-17 ei-DNA: ta sitovat antineoplastiset aineet (esim., Vinka-alkaloidit, taksaanit, topoisomeraasin estäjät) häiritsevät mitoosia. Muut kuin DNA: han sitoutuvat aineet poistuvat helpommin ekstravasaatioalueilta ja aiheuttavat vähemmän kudosvaurioita kuin DNA: han sitoutuvat aineet.
ekstravasaation riskitekijöitä
ekstravasaation riskejä on useita ja ne ovat suurelta osin muokattavissa. Monet näistä riskeistä johtuvat laitteiden käytön ja sijoittamisen virheistä. IV laite tekijät, jotka vaikuttavat ekstravasation riski ovat neula materiaali (toisin sanoen, metalli), kanyylin koko (suuri muovi vs. pieni muovi), ja katetrin tyyppi (toisin sanoen, keskuslaskimo katetri ). Metallineulat voivat aiheuttaa enemmän vahinkoa insertioon ja ovat joustamattomia aluksen sisällä, kun taas suurikokoiset neulat voivat haitata verenkiertoa, hidastaen infusaatin laimentumista.18, 19 ekstravasaatio CVC: stä voi tapahtua neulan siirtyessä implantoidusta LASKIMOPORTISTA (IVAP), mekaanisessa tukoksessa ja sitä seuraavissa CVC-vaurioissa, katetrin siirtymisessä tai fibriiniholkin muodostumisessa ja tromboosissa. IVAP: n virheellinen sijoittaminen on todennäköisempää potilailla, joilla on uusia laitteita, niillä, joilla on merkittävää leikkauksen jälkeistä turvotusta, ja lihavilla potilailla tai isorintaisilla naisilla.20 mekaaniset okkluusiot voivat johtua trombin muodostumista, lääkkeen sakkaa, retrogradinen katetrin siirtymä, tai hyppysellinen-off (ts., ajoittainen ja positionaalinen katetrin tukos; on syytä epäillä, jos infuusio okkluusio voidaan lievittää, kun potilas siirtää käsivarren paikannus).2, 21, 22 ekstravasaation välttäminen riippuu suuresti laskimonsisäisen infuusiokohdan asianmukaisesta ylläpidosta ja oikean infuusionopeuden varmistamisesta. Nämä riskitekijät liittyvät käytettyihin syöpälääkkeisiin, potilaisiin ja lääkkeen antajaan.
ennaltaehkäisy
potilaiden tarkka seuranta ja sekä potilaiden että lääkärien valistus rakkuloiden ekstravasaation riskeistä ja hallinnasta näyttävät olevan ehkäisyn kulmakiviä. Vaikka lääkärit vastaavat täsmällisten tilausten kirjoittamisesta, sairaanhoitajat ovat vastuussa laitteiden osaavan ja asianmukaisen sijoittamisen varmistamisesta sekä kemoterapia-infuusioiden seurannasta visuaalisesti ja potilashaastatteluin. Rakkuloita annosteltaessa tulee seurata alueen turvotusta, punoitusta ja kipua. Rakkuloita tulee annostella valmistajan suositusten mukaisesti (esim.oikea laimentaminen, määrätty antoaika). LASKIMOLINJAT tulee huuhdella ennen solunsalpaajahoitoa ja sen jälkeen. Apteekkarin rooli olisi auttaa kehittämään politiikkoja, jotka varmistavat kemoterapia-aineiden asianmukaisen todentamisen, merkitsemisen ja annostelun. Yksi tapa, jolla tämä voitaisiin toteuttaa, on käyttää syrjiviä merkintöjä, kun annetaan vesikantaisia syöpälääkkeitä niin, että hoitajat käyttävät asianmukaisia varotoimenpiteitä. Farmaseutit voivat olla olennainen osa koulutusta tarjoamalla lääkeinformaatiota ja rutiininomaisia in-palveluja kaikille terveydenhuollon tiimin jäsenille eri solunsalpaajien asianmukaisesta käytöstä ja antamisesta. Turvallisten käytäntöjen toteutuminen edellyttää monialaista yhteistyötä. Kemoterapian antaminen potilaille edellyttää henkilöstön asianmukaista koulutusta ja potilaiden koulutusta sekä hallinnollista tukea politiikan täytäntöönpanon kautta.2,23
dokumentointi tapahtumista
jokainen ekstravasaatiotapaus on dokumentoitava ja raportoitava huolellisesti. Dokumentoinnilla on useita tarkoituksia, kuten tarkka selvitys tapahtuneesta, asianomaisten terveydenhoitoalan ammattilaisten suojeleminen, tietojen kerääminen ekstravasaatioista ja puutteiden korostaminen käytännössä.23 haittavaikutusten ja lääkitysvirheiden dokumentointi ja raportointi asianmukaisille tahoille on toinen tapa, jolla farmaseutit voivat auttaa ehkäisemään tulevia tapahtumia. Raportoiduista haittavaikutuksista ja lääkitysvirheistä kerättyjä tietoja voitaisiin käyttää oppimisvälineinä, jotta voitaisiin tutkia systeemisesti, millä tavoin näitä tapahtumia esiintyy. Paikalliset menettelyt ja protokollat ovat ensiarvoisen tärkeitä ekstravasaation oikea-aikaisen tunnistamisen ja hallinnan sekä vakavien kudosvaurioiden ehkäisyn kannalta. Yhteistyötä olisi tehtävä, jotta varmistetaan oikea-aikaiset Monialaiset pyrkimykset kouluttaa kaikkia näiden potilaiden hoitoon osallistuvia terveydenhoitotiimin jäseniä tapauksen jälkeen. Lisätoimia olisi tehtävä sellaisten politiikkojen käynnistämiseksi, jotka estäisivät uudet tapahtumat. Jos toimintatavat ovat käytössä, ne olisi saatettava helposti saataville ja päivitettävä säännöllisesti vastaamaan nykyisiä käytäntöjä. European Oncology Nursing Society (EONS) 2007 extravasation guidelines sisältää ehdotettuja tietoja ja malleja, joita voidaan käyttää tietojen keräämiseen tapauksen sattuessa.
ekstravasaation merkkejä ja oireita
rakkulaisen ekstravasaation merkkejä ja oireita ovat turvotus, punoitus ja / tai epämukavuus, jota usein kuvaillaan poltteluksi tai kirvelyksi. Resistenssi lääkkeen antamisen aikana, hidas tai hidas infuusio ja veren paluun puute tai menetys IV kanyylista, implantoidusta portista tai muusta keskuslaskimolaitteesta voivat olla merkkejä vesikantin ekstravasaatiosta.23 värimuutokset ja ihon kovettumat voivat edetä rakkuloiden tai nekroosin ja mahdollisesti haavaumien ja syväkudosvaurioiden kehittymisen myötä. Epiteelivaurion koko laajuuden toteutuminen voi kestää useita päiviä.
solunsalpaajahoidon aiheuttaman ekstravasaation hoito
vesikantin ekstravasaation hoidossa käytettyjä hoitomuotoja ovat solunsalpaajahoidon välitön lopettaminen ja ekstravasaatiokohdan jäähdytys tai laimentaminen. Ekstravasaatioon liittyvän sairastavuuden vähentämiseksi on tärkeää, että lääkärit ovat hyvin perillä saatavilla olevista hoidoista ja työskentelevät nopeasti, jotta potilashaitat eivät lisääntyisi. Nonvesiantin ekstravasaation hoitoon kuuluu tyypillisesti raajan kohottaminen ja jäähtyminen, eikä siihen yleensä kuulu farmakologista hoitoa.23
Vesikantin ekstravasaation alkuvaiheen hoitoa
varhaisvaiheen hoidon helppoutta voidaan helpottaa asettamalla laitoksessa saataville ekstravasaatiopakkaus. Useimmat ekstravasaatiopakkaukset sisältävät kertakäyttöisiä ruiskuja ja kanyyleja, kylmäkuumapakkauksia, sideharsotyynyjä, laastareita, steriilejä ja suojakäsineitä sekä lääkkeitä ekstravasaation hoitoon (esim.hyaluronidaasi, dimetyylisulfoksidi 99%, deksratsoksaani). Luettelo pakkauksen sisällöstä on sijoitettava pakkaukseen ja apteekkihenkilökunnan on säännöllisesti tarkistettava lääkkeen sisältö päivitetyine käyttöpäivineen.2
kun vesikantin ekstravasaatio tapahtuu, lääkärin tulee välittömästi lopettaa infuusio; kanyyli tai ei-kiinnittyvä porttineula on kuitenkin pidettävä paikallaan ja vesiainetta on yritettävä aspiroida 10 mL: n ruiskulla. Ekstravasaatioalue tulee merkitä ja kuvata; sitten kanyyli tai neula tulee poistaa ja ilmoittaa lääkärille. Potilaat saattavat tarvita kipulääkkeiden käyttöä mahdollisen kivun hallitsemiseksi. Kun alustavat toimenpiteet on toteutettu, on erittäin tärkeää dokumentoida huolellisesti tapahtunut haittavaikutus ja/tai lääkitysvirhe.23
vinka-alkaloidien osalta, joissa vesiaineen dispergointi tai laimentaminen on aiheellista, paikallista lämpöä 20 minuutin ajan 4 kertaa päivässä 1 päivän ajan 2 päivän ajan. Muiden rakkuloiden ekstravasaatioissa, antrasykliinit mukaan lukien, hoidon alussa ekstravasoitu aine paikallistetaan ja neutraloidaan kylmäpuristuksella 20 minuutin ajan 4 kertaa päivässä 1-2 päivän ajan, mikä rajoittaa näiden aineiden soluunottoa.
farmakologinen hoito
DMSO: DMSO on yleinen liuotin, joka tunkeutuu kudoksiin ja lisää ihon läpäisevyyttä, mikä voi helpottaa ekstravasoidun lääkkeen imeytymistä. Kun sitä käytetään paikallisesti, sillä on vapaiden radikaalien puhdistus-/antioksidantti-ominaisuuksia, jotka voivat nopeuttaa ekstravasoidun lääkkeen poistamista. DMSO (Rimso-50) on saatavana Yhdysvalloissa vain vähittäismyyntiin 50-prosenttisena (vol/vol) liuoksena vedessä. Tämä liuos on FDA: n hyväksymä vain toistuvan interstitiaalisen kystiitin hoitoon.DMSO: n tehoa kemoterapian ekstravasaation hoidossa kuvattiin ensin useissa tapausraporteissa ja pienissä kliinisissä tutkimuksissa.
yhdessä tapauksessa 10 mg: n daunorubisiinin ekstravasaatiota 42-vuotiaalle miehelle hoidettiin natriumbikarbonaatilla, deksametasonilla (4 mg), jääpakkauksilla ja 1, 5 mL paikallista DMSO 70%: A, jota levitettiin 3-4 tunnin välein 10 päivän ajan. Tämä hoito lievitti kipua ja esti mahahaavan.
Olver ja Schwarz raportoivat kolme ekstravasaatioresoluutiotapausta DMSO: n käytön yhteydessä.Yhdessä tapauksessa doksorubisiinin ekstravasaatiota saaneella potilaalla DMSO 99%: n päivittäinen käyttö 14 vuorokauden ajan johti kivun täydelliseen häviämiseen 2 VUOROKAUDEN kuluessa ilman haavaumia. Potilas sai myös 8, 4% natriumbikarbonaattia ja sopivaa ei-farmakologista hoitoa. (Katso taulukko 2 ei-farmakologiset vaihtoehdot.) Toisessa tapauksessa 49-vuotiasta miestä, joka sai 4-6 mg doksorubisiinia, hoidettiin doksorubisiinin ekstravasaatioon 5 mL: lla 8: aa.4% natriumbikarbonaattia, jääpakkauksia ja 99% DMSO: ta käytetään päivittäin 14 päivän ajan. Haavaumia ei esiintynyt, mutta kyynärpään ojennusta rajoittava 3 x 2, 5 cm: n alue induroitui.26 kolmannessa tapauksessa DMSO: n 99%: n paikallinen käyttö (6 tunnin välein 1 viikon ajan ja sitten kahdesti päivässä toisen viikon ajan) esti haavaumien syntymisen; jäljellä oleva pigmentti kuitenkin säilyi.
Berghammer ja muut raportoivat myös dosetakselin ekstravasaatiotapauksesta.Ekstravasaatti laimennettiin normaalilla (0, 9%) suolaliuoksella ja käsiteltiin jääpusseilla. DMSO: ta annosteltiin 3 kertaa 45 minuutin välein, ja ekstravasaatiopäivänä annettiin kortikosteroideja ja diklofenaakkia suun kautta. Kaikki oireet hävisivät 24 tunnin kuluessa, mutta viivästyneet oireet (ruskea värjäytyminen, ihon hyperplasia) ilmaantuivat 5.päivänä ja lisääntyivät sen jälkeen. Plastiikkakirurgisia toimenpiteitä ei tarvittu. Vaikka DMSO yhdistettynä hypotermiaan ja isotoniseen suolaliuokseen ei ollut tehokas estämään viivästyneitä oireita, se rajoitti tulehdusta ja kudosnekroosia.
Ludwig ja muut raportoivat, että 90-prosenttisen DMSO: n ja 10-prosenttisen alfa-tokoferoli-seoksen käyttö 48 tunnin kuluessa antrasykliinien tai mitomysiini C: n ekstravasaation jälkeen 8 potilaalla ei aiheuttanut ihohaavoja eikä toiminnallista tai neurovaskulaarista vajaatoimintaa.28 valitettavasti alfa-tokoferoli ei ole helposti saatavilla lääkeaine ja lisäksi satunnaistetut tutkimukset olisi tehtävä validoida sen käyttöä.
prospektiivisessa tutkimuksessa, johon osallistui 20 antrasykliinin ekstravasaatiota saanutta potilasta, DMSO 99%: lle annettiin kahdesti, 6 kertaa vuorokaudessa 2 viikon ajan.29 DMSO-hoidon jälkeen ei kuvattu haavaumia, vaikka alussa ilmeni turvotusta (85%), punoitusta (75%) ja kipua (60%). 3 kuukauden seurantajakson jälkeen 16 potilaalla 6 (38%) potilaalla ei ollut mitään näkyviä oireita ja 10 (63%) potilaalla oli pigmentoituneita oireita. Bertelli teki myös prospektiivisen tutkimuksen, jossa arvioitiin DMSO: n vaikutuksia antrasykliinien ekstravasaatioihin.Doksorubisiinin osuus oli 11 tapausta ja epirubisiinin 46 tapausta. Potilaista 99% sai DMSO: ta 8 tunnin välein 7 vuorokauden ajan. Seitsemälläkymmenellä prosentilla potilaista (40/57) ekstravasaatio hävisi täydellisesti 1 viikon kuluessa, yhdellä potilaalla oli jäljellä pehmytkudoksen kovettuma ja yhdellä potilaalla oli hyperpigmentaatiota.
näissä tapausraporteissa ja pienissä tutkimuksissa ekstravasaatiot diagnosoitiin kliinisesti eikä biopsialla. DMSO voi olla vaihtoehto ekstravasoitujen antrasykliinien, mitomysiini C: n ja aktinomysiini D: n hoidossa.suositellaan, että ekstravasoidulle alueelle levitetään ohut DMSO-kerros ja annetaan kuivua. Ei-occlusiivinen sidos tulee levittää 10-25 minuutin kuluessa. Nämä vaiheet toistetaan 8 tunnin välein 7 päivän ajan.23 vaikka DMSO: ta on käytetty käytännössä hoitovaihtoehtona, mahdollisten kokeiden puuttuminen voi rajoittaa sen käyttöä. Eons 2007-ekstravasaatio-ohjeissa suositellaan lisätutkimusten tekemistä; 50-99% DMSO: n käyttöä voidaan kuitenkin harkita lääkärin harkinnan mukaan.23 on tärkeää huomata, että yhdessäkään DMSO-prospektiivisissa tutkimuksissa ei käytetty sidosta, jotta iho voisi imeä DMSO: n täysin itseensä.
hyaluronidaasi: Hyaluronidaasin arvellaan kykenevän hajottamaan epiteelisolujen alla olevan solunulkoisen matriisin. Matriisi pitää kiinni suurista vesimolekyylimääristä, ja hajotessaan se pystyy vapauttamaan nesteen solunulkoiseen ympäristöön. Ekstravasaation tapauksessa se mahdollistaa nesteen lisääntymisen kohtaan, jolloin ihon todellinen pitoisuus kosketuskohdassa laimenee.31,32 hyaluronidaasia on käytetty Vinka-alkaloidi-ja taksaani-ekstravasaatioiden hoitoon.Hyaluronidaasia on annettu 33 annosta 150-1500 yksikköä, jotka on laimennettu 1 mL: lla ihonalaista tai intradermaalista suolaliuosta 1 tunnin kuluessa ekstravasaatiosta.
pienessä kliinisessä tutkimuksessa, johon osallistui 6 potilasta, joilla oli vinblastiinin (n = 1), vinkristiinin (n = 1) ja vinorelbiinin (N = 4) ekstravasaatio, 250 yksikköä hyaluronidaasia ruiskutettiin sisuskatetriin tai loukkaantumistapauksessa ihon alle (6 injektiota). Steroideja tai kylmäpakkauksia ei käytetty. Kipu hävisi kaikilla potilailla muutaman päivän kuluessa hyaluronidaasihoidosta. Yksi potilas valitti lievästi kivuliasta kovettumaa 3 kuukautta vinkristiinin ekstravasaation jälkeen.30 nämä raportit paljastavat lupaavia tietoja, mutta hyaluronidaasin käytöstä vinka-alkaloidien ekstravasaatioiden hoidossa ei ole vielä yleisesti näyttöä. Lisää tulevia kokeita on tehtävä. Eons 2007: n ekstravasaatio-ohjeissa suositellaan lisätutkimusten tekemistä; hyaluronidaasia voidaan kuitenkin pitää vaihtoehtona ehdotetuilla annoksilla lääkärin harkinnan mukaan.23
natriumtiosulfaatti: Natriumtiosulfaatti estää alkylointia ja kudosten tuhoutumista tarjoamalla substraatin alkyloinnille ihonalaisessa kudoksessa. Natriumtiosulfaatin on osoitettu olevan tehokas eläinkokeissa ja yhdessä tapausselostuksessa mekloretamiinin (typpisinappi) ekstravasaation hoidossa.Suositeltu annos on 2 mL 0, 17 M (liuos, jossa on 4 mL 10% natriumtiosulfaattia ja 6 mL steriiliä injektionesteisiin käytettävää vettä). Koska näyttöä ei ole, eons 2007: n ekstravasaatio-ohjeissa tätä ei suositella vastalääkkeeksi.22
Deksratsoksaani: FDA hyväksyi äskettäin deksratsoksaanin (Totect) antrasykliinin aiheuttamien ekstravasaatioiden hoitoon. Deksratsoksaanilla on kaksi vaikutusmekanismia: 1) se toimii raudan kelaattorina estäen rauta-antrasykliinikompleksien ja rautavälitteisten hydroksyyliradikaalien muodostumisen, jotka aiheuttavat oksidatiivisia vaurioita; ja 2) se stabiloi topoisomeraasi II: n ja tekee sen saavuttamattomaksi antrasykliinihoitoon. Deksratsoksaani estää entsyymin toimintaa niin, että antrasykliini ei enää vaikuta siihen ja estää terveiden solujen vaurioitumisen kudoksessa.
deksratsoksaanin teho osoitettiin kahdessa Euroopassa tehdyssä kliinisessä tutkimuksessa.Molemmat tutkimukset olivat prospektiivisia, avoimia, yksihaaraisia kliinisiä monikeskustutkimuksia, jotka tehtiin heinäkuusta 2001 elokuuhun 2005 ja joihin osallistui yhteensä 80 potilasta. Ensimmäiseen tutkimukseen otettiin potilaita 17 syöpäpaikalta Tanskassa ja toiseen tutkimukseen otettiin potilaita 34 syöpäpaikalta Tanskassa, Saksassa, Italiassa ja Alankomaissa. Antrasykliinin ekstravasaatio diagnosoitiin ja vahvistettiin 6 tunnin kuluessa deksratsoksaanista otetun biopsiakudoksen fluoresenssimikroskopialla. Otoskoko oli 32 arvioitavissa olevaa potilasta, jotta leikkausten ilmaantuvuus vähenisi vähintään 70% (yksipuolinen binomitesti, a=.025, ß=.20). Ensisijainen päätepiste oli kirurginen resektio ja nekroosi. 80 potilaasta 54 (tutkimus 1: n = 18; tutkimus 2: n = 36) oli arvioitavissa (n = 13 negatiivista koepalaa; N = 4 ei tehty koepaloja; n = 8 protokollan rikkomista), ja heidän keski-ikänsä oli 56 vuotta (vaihteluväli 34-81 vuotta). Arvioiduista potilaista 69 prosenttia (n = 37) oli naisia. Deksratsoksaani annettiin 1-2 tunnin infuusiona laskimoon.; 1 000 mg/m2 6 tunnin kuluessa; 1 000 mg/m2 24 tunnin kuluttua; ja 500 mg / m2 48 tunnin ekstravasaation jälkeen.36
potilaan teho ja turvallisuus arvioitiin päivinä 7, 14, 21 ja 28, ja teho päivänä 90, 36 yleisin syöpädiagnoosi oli rintasyöpä (50%), seuraavaksi lymfooma (39%) ja muut syöpätyypit (9%). Potilailla esiintyi doksorubisiinin (n = 23) tai epirubisiinin (n = 31) ekstravasaatioita. Ekstravasaation keskimääräinen pinta-ala oli tutkimuksessa 1 23, 6 cm2 ja tutkimuksessa 2 39 cm2. Yhdellätoista potilaalla ekstravasaatioalue oli yli 75 cm2. Tutkimuksissa 1 ja 1 ei havaittu leikkaustapauksia (2, 8%, 95%: n luottamusväli 0, 1% – 14, 5%) tutkimuksessa 2. Potilaalla, jolle kehittyi ekstravasaation seurauksena kudosnekroosi, oli hyvin suuri doksorubisiinin ekstravasaatioalue, jonka koko oli 253 cm2. Oireet lisääntyivät ekstravasaation jälkeisinä päivinä, kudosnekroosia alkoi esiintyä 9 päivää ekstravasaation jälkeen ja nekroosi leikattiin kirurgisesti. Tutkimuksessa 1 oli 1 (5, 6%) koepalan aiheuttama nekroosi, 6 (33.3%) tapauksia lykkäämisestä tai peruuttamisesta suunnitellun syöpähoidon, ja 9 (50%) sairaalahoitoa johtuu ekstravasation. Tutkimuksessa 2 oli 1 (2, 8%) ekstravasaatiosta johtuva nekroosi, 3 (8, 3%) biopsiasta johtuva nekroosi, 10 (27, 8%) ekstravasaation aiheuttama syöpähoidon lykkääminen tai peruuttaminen ja 13 (36, 1%) ekstravasaation aiheuttama sairaalahoito. 3 kuukauden seurannassa 88, 9%: lla (n = 16) ei ollut negatiivisia jälkiseurauksia tutkimuksessa 1 ja 63, 9%: lla (n = 23) tutkimuksessa 2. Viidellätoista 80 potilaasta esiintyi aistihäiriöitä (n = 9), ihon atrofiaa (N = 5), kipua (N = 10), epämuodostumia (n = 1) ja rajoittuneisuutta (n = 3). Suurin osa potilaista (71%) pystyi saamaan jatkohoitoa solunsalpaajahoidossa aikataulun mukaisesti.
yleisimpiä haittavaikutuksia olivat valkosolujen määrän lasku (72, 5%), hemoglobiiniarvon lasku (42, 5%), verihiutaleiden määrän lasku (26%), aspartaattiaminotransferaasiarvojen nousu (36, 8%), alaniiniaminotransferaasiarvojen nousu (23, 9%), pistoskohdan reaktio (27, 5%) ja pahoinvointi (18, 8%).36 kliinisten tutkimusten tulokset osoittivat, että deksratsoksaani on tehokas aine akuuttien antrasykliinien ekstravasaatioiden hoidossa ja viivästyneiden oireiden ehkäisyssä.
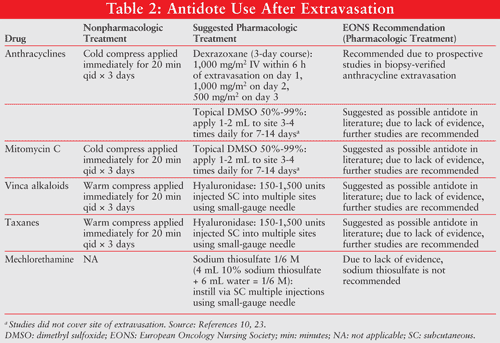
yhteenveto näistä hoitosuosituksista, mukaan lukien EONS 2007-ohjeet, on esitetty taulukossa 2.
proviisorin rooli
proviisorien tulee olla tiiviisti mukana kaikkien kemoterapian aiheuttamien ekstravasaatioiden arvioinnissa ja hoidossa. Ne voivat olla olennainen rooli useilla tavoilla, kuten: 1) politiikkojen ja protokollien kehittäminen; 2) potilas -, perhe-ja monitieteinen koulutus; 3) ekstravasaatioiden ja muiden hoidon jälkeisten haittavaikutusten dokumentointi ja raportointi; ja 4) hoidon asianmukaisen annostelun, annostelun ja tehokkuuden seuranta.
johtopäätös
kaikissa tarkastelluissa tutkimuksissa oli mukana aikuisia, koska lapsipotilailla olisi ollut suurentunut kiihtymys-ja juovien vetämisen riski. Tähän mennessä deksratsoksaani on ainoa ekstravasaatioaine, jota on tutkittu suurissa, prospektiivisissa monikeskustutkimuksissa, joissa ekstravasaatiotapausten diagnosointiin käytettiin objektiivisia, luotettavia testejä; tämä antaa vahvaa näyttöä deksratsoksaanin hyödyllisyydestä. Muista farmakologisista hoidoista, kuten DMSO: sta ja hyaluronidaasista, ei ole niiden yleisestä käytännön käytöstä huolimatta tehty laajoja tutkimuksia, minkä vuoksi Näyttöön perustuvat suositukset puuttuvat. Ekstravasaation hallinta on tehtävä lääkärin harkinnan mukaan yhteistyössä kaikkien terveydenhuollon tiimin jäsenten kanssa.
1. Infusion Nurses Society. Infuusio hoitotyön standardit käytännön. J Infus Nurs. 2006; 29(suppl 1): S1-S92.
2. Polovich M, White J, Kelleher L. kemoterapia ja Bioterapia ohjeet ja suositukset käytännön. 2. Pittsburgh, PA: Oncology Nursing Society; 2005.
3. Ener RA, Meglathery SB, Styler M. ekstravasation of systemic hemato-onkologic therapies. Ann Onkol. 2004;15:858-862.
4. Sauerland C, Egelking C, Wickman R, Corbi D. Vesicant ekstravasation part I: mechanisms, patogenesis, and nursing care to reduce risk. Oncol Nurs Forum. 2006;33:1134-1141.
5. Cassagnol M, Cohen H. Dermatologic toxicities of chemotherapeutic agents. US Pharm. 2008;33(1)(Oncology suppl):10-20.
6. Schulmeister L. Extravasation management. Semin Oncol Nurs. 2007;23:184-190.
7. Viale P. Chemotherapy and cutaneous toxicities: implications for oncology nurses. Semin Oncol Nurs. 2006;22:144-151.
8. Cox K, Stuart-Harris R, Abdini G, et al. The management of cytotoxic-drug extravasation: guide-lines drawn up by a working party for the Clinical Oncological Society of Australia. Med J Aust. 1988;148:185-189.
9. Schrijvers DL. Extravasation: kemoterapian pelätty komplikaatio. Ann Onkol. 2003; 14 (suppl 3):ii26-ii30.
10. Kansallinen Ekstravasaatiotietopalvelu. www.extravasation.org.uk/home.html. Accessed 25 maaliskuu 2009.
11. Lemmers N, geelit M, Sleijfer D, et al. Laskimoportin komplikaatiot 132: lla disseminoitunutta kivessyöpää sairastavalla potilaalla, joita hoidettiin polykemoterapialla. J Clin Onkol. 1996;14:2916-2922.
12. Shetty PC, Mody MK, Kastan DJ. Toimenpideradiologien asettamien 350 implantoidun rintaportin tulokset. J Vasc Interv Radiol. 1997;8:991-995.
13. Dorr RT. Vesipitoisen kemoterapian ekstravasaation vasta-aineet. Blood Rev. 1990;4: 41-60.
14. Langer SW, Sehested M, Jensen PB. Antrasykliinin ekstravasaation hoito deksratsoksaanilla. Clin Cancer Res. 2000; 6: 3680-3686.
15. Raymond E, Faivre S, Woynarowski JM, Chaney SG. Oksaliplatiini: vaikutusmekanismi ja Antineoplastinen aktiivisuus. Semin Onkol. 1998; 2 (täydennys 5): 4-12.
16. Rivory LP. Uudet lääkkeet paksusuolen syöpä-toimintamekanismit. Aust Prescr. 2002;25:108-110. www.australianprescriber.com/magazine/25/5/108/10/. Accessed 25 maaliskuu 2009.
17. Skeel RT. Handbook of Cancer Chemotherapy. 5.toim. New York, NY: Lippincott Williams & Wilkins; 1999.
18. Boyle DM, Engelking C. Vesicant extravasation: myths and realities. Oncol Nurs Forum. 1995;22:57-67.
19. Hadaway LC. Perifeerisen ekstravasaation estäminen ja hallinta. Hoivata. 2004;34:66-67.
20. Shulmeister L, Camp-Sorrell D. kemoterapian ekstravasaatio istutetuista porteista. Oncol Nurs Forum. 2000;27:531-538.
21. Debets JM, Wils JA, Schlangen JT. Harvinainen komplikaatio istutetuista keskuslaskimolaitteista: katetrin murtuma ja embolisaatio. Tuki Hoito Syöpä. 1995;3:432-434.
22. Gorski LA. Keskuslaskimolaitteen okkluusiot. Osa 2: Nonitromboottiset syyt ja hoito. Kotihoitaja. 2003;21:168-171.
23. Ekstravasation guidelines 2007. European Oncology Nursing Society. www.cancerworld.org/CancerWorld/getStaticModFile.aspx?id=2340. Accessed 25 maaliskuu 2009.
24. Rimso-50 (dimetyylisulfoksidi) pakkausseloste. Lake Forest, IL: Bioniche Pharma USA LLC; 2009.
25. Lawrence HJ, Hyvää yötä. Dimetyylisulfoksidi rajoittaa doksorubisiinin ekstravasaation aiheuttamia kudosvaurioita. Ann Intern Med. 1983;98:1025.
26. Olver IN, Schwarz MA. Use of dimethyl sulfoxide in limiting tissue damage caused by extravasation of doxorubicin . Cancer Treat Rep. 1983;67:407-408.
27. Berghammer P, Pohnl R, Baur M, Dittrich C. Docetaxel extravasation. Support Care Cancer. 2001;9:131-134.
28. Ludwig CU, Stoll HR, Obrist R, Obrecht JP. Prevention of cytotoxic drug-induced skin ulcers with dimethyl sulfoxide (DMSO) and alpha-tocopherole. Eur J Cancer Clin Oncol. 1987;23:327-329.
29. Olver IN, Aisner J, Hament A, et al. A prospective study of topical dimethyl sulfoxide for treating anthracycline extravasation. J Clin Oncol.1988;6:1732-1735.
30. Bertelli G. Prevention and management of extravasation of cytotoxic drugs. Drug Saf. 1995;12:245-255.
31. Balazs EA, Laurent TC, Jeanloz RW. Nomenclature of hyaluronic acid. Biochem J. 1986;235:903.
32. Girish KS, Kemparaju K. The magic glue hyaluronan and its eraser hyaluronidase. Life Sci. 2007;80:1921-1943.
33. Dorr T. Antidotes to vesicant chemotherapy extravasations. Blood Rev. 1990;4:41-60.
34. Owen OE, Dellatorre DL, Van Scott EJ, Cohen MR. Accidental intramuscular injection of mechlorethamine. Cancer. 1980;45:2225-2226.
35. Totect (dexrazoxane for injection) package insert. Copenhagen, Denmark: TopoTarget A/S; October 2007.
36. Mouridsen HT, Langer SW, Buter J, et al. Treatment of anthracycline extravasation with Savene (dexrazoxane). Results from two prospective clinical multicenter studies. Ann Oncol. 2007;18:546-550.
Leave a Reply