Epäorgaaninen kemia
deskriptiivinen epäorgaaninen kemia keskittyy yhdisteiden luokitteluun niiden ominaisuuksien perusteella. Osittain luokittelu keskittyy raskaimman alkuaineen (alkuaineen, jolla on suurin atomipaino) asemaan jaksollisessa järjestelmässä yhdisteessä, osittain ryhmittelemällä yhdisteitä niiden rakenteellisten samankaltaisuuksien perusteella.
epäorgaanisen kemian luokitukset:
Koordinaatiokoosteedit
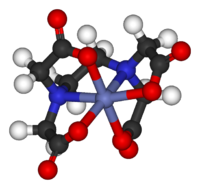
EDTA kelatoi oktaedrisesti koordinoidun Co3+ − ionin in−
Pääartikkeli: Koordinaatiokemia
klassisissa koordinaatioyhdisteissä esiintyy metalleja, jotka ovat sitoutuneet ”yksinäisiin elektronipareihin”, jotka asuvat ligandien pääryhmäatomeissa, kuten H2o, NH3, cl−ja CN -. Nykyaikaisissa koordinaatioyhdisteissä ligandeina voidaan käyttää lähes kaikkia orgaanisia ja epäorgaanisia yhdisteitä. ”Metalli” on yleensä ryhmien 3-13 metalli samoin kuin trans-lantanidit ja trans-aktinidit, mutta tietystä näkökulmasta kaikkia kemiallisia yhdisteitä voidaan kuvata koordinaatiokomplekseina.
koordinaatiokompleksien stereokemia voi olla melko rikas, kuten vihjataan Wernerin erottaessa kaksi enantiomeeriä 6+: sta, mikä on varhainen osoitus siitä, että siraalisuus ei ole luontaista orgaanisille yhdisteille. Ajankohtainen teema tässä erikoistumisessa on supramolekulaarinen koordinaatiokemia.
- esimerkkejä: −, 3+, TiCl4(THF)2.
pääryhmäyhdiste

näissä lajeissa on alkuaineita jaksollisen järjestelmän ryhmistä I, II, III, IV,V, VI, VII, 0 (vetyä lukuun ottamatta). Usein samankaltaisen reaktiivisuutensa vuoksi ryhmään 3 (Sc, Y ja La) ja ryhmään 12 (Zn, Cd ja Hg) kuuluvat yleensä myös alkuaineet, ja joskus myös lantanidit ja aktinidit.
pääryhmän yhdisteitä on tunnettu jo kemian alkuajoista lähtien, esimerkiksi alkuainerikkiä ja tislattavaa valkoista fosforia. Lavoisierin ja Priestleyn kokeet hapella, O2: lla, eivät ainoastaan tunnistaneet tärkeää diatomista kaasua, vaan avasivat tien yhdisteiden ja reaktioiden kuvaamiseen stoikiometristen suhteiden mukaan. Carl Boschin ja Fritz Haberin 1900-luvun alussa keksimä rautakatalyyttejä käyttävä ammoniakin käytännöllinen synteesi vaikutti syvästi ihmiskuntaan, mikä osoitti epäorgaanisen kemiallisen synteesin merkityksen.Tyypillisiä pääryhmän yhdisteitä ovat SiO2, SnCl4 ja N2O. Monet pääryhmäyhdisteet voidaan myös luokitella ”organometallisiksi”, koska ne sisältävät orgaanisia ryhmiä, esimerkiksi B(CH3)3). Pääryhmäyhdisteitä esiintyy luonnossa myös esimerkiksi fosfaattina DNA: ssa, minkä vuoksi ne voidaan luokitella bioorgaanisiksi. Vastaavasti ”epäorgaanisiksi” voidaan luokitella orgaanisia yhdisteitä, joilta puuttuvat (monet) vetyligandit, kuten fullereenit, buckytubet ja binääriset Hiilioksidit.
- esimerkkejä: tetrasulfuuritetranitridi S4N4, diboraani B2H6, silikonit, buckminsterfullereeni C60.
Siirtymämetalliyhdisteet
yhdisteitä, jotka sisältävät metalleja ryhmistä 4-11, pidetään siirtymämetalliyhdisteinä. Tähän ryhmään luetaan joskus myös yhdisteet, joissa on ryhmään 3 tai 12 kuuluva metalli, mutta luokitellaan usein myös pääryhmään kuuluviksi yhdisteiksi.
Siirtymämetalliyhdisteillä on rikas koordinaatiokemia, joka vaihtelee titaanin tetraedristä (esim.TiCl4) joidenkin nikkelikompleksien neliötasoon ja koboltin koordinaatiokompleksien oktaedriin. Erilaisia siirtymämetalleja löytyy biologisesti tärkeistä yhdisteistä, kuten hemoglobiinin sisältämästä raudasta.
- esimerkkejä: rautapentakarbonyyli, titaanitetrakloridi, sisplatiini
Organometalliyhdisteet

yleensä organometalliyhdisteiden katsotaan sisältävän m-c-h-ryhmän. Näissä lajeissa Metalli (M) voi olla joko pääryhmäelementti tai siirtymämetalli. Toiminnallisesti organometalliyhdisteen määritelmä on rennompi ja sisältää myös erittäin lipofiilisiä komplekseja, kuten metallikarbonyylejä ja jopa metallialkoksideja.
organometalliyhdisteitä pidetään lähinnä erityiskategoriana, koska orgaaniset ligandit ovat usein herkkiä hydrolyysille tai hapettumiselle, minkä vuoksi organometallikemiassa käytetään erikoistuneempia preparointimenetelmiä kuin Werner-tyyppisissä komplekseissa oli tapana. Synteettinen menetelmä, erityisesti kyky manipuloida komplekseja liuottimissa, joilla on alhainen koordinointiteho, mahdollisti hyvin heikosti koordinoivien ligandien kuten hiilivetyjen, H2: n ja N2: n tutkimisen. Koska ligandit ovat jossain mielessä petrokemikaaleja, organometallikemian alue on hyötynyt suuresti sen merkityksestä teollisuudelle.
- esimerkkejä: Cyclopentadienyliron dicarbonyl dimer (C5H5)Fe(CO)2CH3, ferrocene Fe(C5H5)2, molybdenum hexacarbonyl Mo(CO)6, triethylborane Et3B, Tris(dibenzylideneacetone)dipalladium(0) Pd2(dba)3)
Cluster compoundsEdit
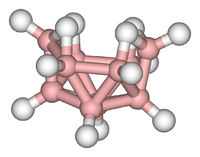

klustereita löytyy kaikista kemiallisten yhdisteiden luokista. Yleisesti hyväksytyn määritelmän mukaan klusteri koostuu minimaalisesti kolmiomaisesta joukosta atomeja, jotka ovat suoraan sitoutuneet toisiinsa. Mutta Metalli-Metalli sidotut dimetallikompleksit ovat erittäin merkityksellisiä alueella. Klustereita esiintyy ”puhtaissa” epäorgaanisissa järjestelmissä, organometallisessa kemiassa, pääryhmäkemiassa ja bioorgaanisessa kemiassa. Hyvin suurten klustereiden ja irtokuitukasvien välinen ero on yhä epäselvempi. Tämä rajapinta on nanotieteen tai nanoteknologian kemiallinen perusta, ja se syntyy erityisesti kadmiumselenidiklustereiden kvanttikokovaikutusten tutkimuksesta. Näin suuria klustereita voidaan kuvata joukkona molekyylin ja kiinteän aineen välissä olevia sidottuja atomeja.
- Examples: Fe3(CO)12, B10H14, 2−, 4FE-4S
Bioorganic compoundsEdit

määritelmän mukaan näitä yhdisteitä esiintyy luonnossa, mutta alakentässä on ihmisperäisiä lajeja, kuten saasteita (esim.metyylielohopea) ja lääkkeitä (esim. sisplatiini). Kenttä, joka sisältää monia näkökohtia biokemian, sisältää monenlaisia yhdisteitä, esim., fosfaatit DNA, ja myös metalli komplekseja, jotka sisältävät ligandeja, jotka vaihtelevat biologisten makromolekyylien, yleisesti peptidit, huonosti määritelty lajeja kuten humushappo, ja vesi (esim koordinoitu gadolinium komplekseja käytetään MRI). Perinteisesti bioorgaaninen kemia keskittyy hengityksen kannalta merkityksellisissä proteiineissa elektronien ja energian siirtoon. Lääke-epäorgaaninen kemia sisältää sekä ei-välttämättömien että olennaisten elementtien tutkimuksen, jossa käytetään diagnooseja ja hoitoja.
- esimerkkejä: hemoglobiini, metyylielohopea, karboksipeptidaasi
Solid state compoundsEdit
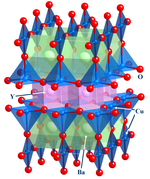
tämä tärkeä alue keskittyy materiaalien rakenteeseen, sidosaineisiin ja fysikaalisiin ominaisuuksiin. Käytännössä solid state-epäorgaaninen kemia käyttää menetelmiä, kuten kristallografiaa, saadakseen käsityksen ominaisuuksista, jotka johtuvat kiinteän aineen alayksiköiden yhteisistä vuorovaikutuksista. Kiinteän olomuodon kemiaan kuuluvat metallit ja niiden seokset tai metallien väliset johdannaiset. Siihen liittyviä aloja ovat tiivistynyt ainefysiikka, mineralogia ja materiaalitiede.
- esimerkkejä: piisirut, zeoliittit, YBa2Cu3O7
Leave a Reply