elektronit kuorissa
![]()
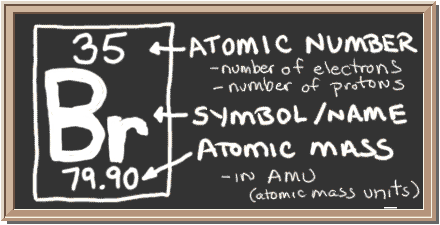
Tsekkaa liitutaulu. Tuossa laatikossa vasemmalla on kaikki tiedot, jotka sinun tarvitsee tietää yhdestä elementistä. Se kertoo yhden atomin massan, kuinka monta kappaletta sen sisällä on ja mihin se pitäisi jaksollisessa järjestelmässä sijoittaa.
nyt on vuorossa neljäs periodi/rivi elementeistä-taulukossa. Neutraalin atomin elektronien lukumäärä voi olla helppo tietää, mutta elektronien sijoittelu muuttuu hieman monimutkaisemmaksi. Katsotaanpa elektronien järjestelyjä neljännen jakson peruselementeissä (taulukon vasemmalla ja oikealla puolella) ja siirtymäelementtien monimutkaisempia järjestelyjä (rivin keskellä). Jos luulet, että tämä on vähän yli pääsi, mene takaisin ja katso elementtejä 1-18, joilla on organisaatioita, jotka ovat hieman yksinkertaisempia.
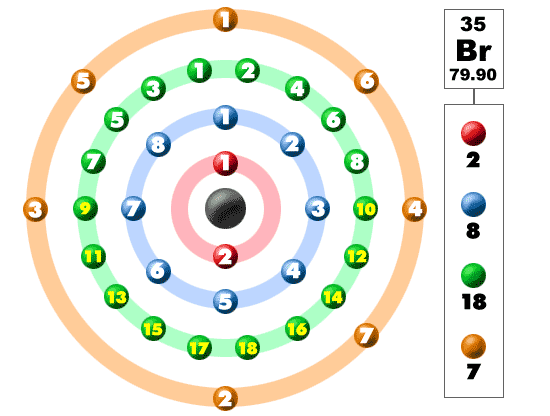
Katso alla oleva kuva. Jokainen noista värillisistä palloista on elektroni. Atomissa elektronit pyörivät keskustan ympäri, jota kutsutaan myös ytimeksi. Elektronit haluavat olla erillisissä kuorissa / orbitaaleissa. Kun opit lisää atomin rakenteesta, opit, että elektronit eivät pysy määritellyillä alueilla ytimen ympärillä. Niitä löytyy pilvistä, joilla voi olla erilaisia muotoja, kuten palloja ja käsipainoa muistuttavia muotoja. Joten muista, kun katsot hajoamistamme, että elektronit eivät ole aina mukavassa järjestyksessä, kuten tässä on esitetty.
bromi kuuluu alkuaineiden halogeeniperheeseen. Sen seuralaisia ovat fluori, kloori ja jodi. Muiden halogeenien tavoin bromin ulkokuoressa on seitsemän elektronia ja se on hyvin reaktiivinen. Bromia on monissa alkalimetallien suolayhdisteissä. Natriumbromidi on yhdiste, jota esiintyy merivedessä. Kuten kaikkia reaktiivisia alkuaineita, bromia ei koskaan esiinny luonnossa yksin. Se on aina osa yhdistettä muiden alkuaineiden kanssa.
Leave a Reply