2.4 B: Dehydraatiosynteesi
Dehydraatiosynteesi
useimmat makromolekyylit koostuvat yksittäisistä alayksiköistä eli rakennuspalikoista, joita kutsutaan monomeereiksi. Monomeerit yhdistyvät toisiinsa kovalenttisten sidosten kautta muodostaen suurempia molekyylejä, jotka tunnetaan polymeereinä. Tällöin monomeerit vapauttavat vesimolekyylejä sivutuotteina. Tämän tyyppinen reaktio tunnetaan dehydraatiosynteesinä, joka tarkoittaa ” koota samalla kun menettää vettä. ”Sitä pidetään myös kondensaatioreaktiona, sillä kaksi molekyyliä tiivistyy yhdeksi suuremmaksi molekyyliksi pienemmän molekyylin (veden) menettäessä.)
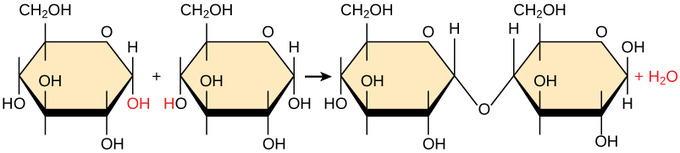
kahden ionisoimattoman monomeerin, kuten monosakkaridisokerin, välisessä dehydraatiosynteesireaktiossa yhden monomeerin vety yhdistyy toisen monomeerin hydroksyyliryhmään, jolloin prosessissa vapautuu vesimolekyyli. Kun yhdestä monomeerista poistetaan vety ja toisesta monomeerista hydroksyyliryhmä, monomeerit voivat jakaa elektroneja ja muodostaa kovalenttisen sidoksen. Näin yhteen liittyneet monomeerit dehydratoituvat suuremman molekyylin synteesin mahdollistamiseksi.
kun monomeerit ionisoituvat, kuten aminohappojen kanssa vesiympäristössä, kuten sytoplasmassa, kaksi vetyä yhden monomeerin positiivisesti varautuneesta päästä yhdistyy toisen monomeerin negatiivisesti varautuneen pään Happeen kanssa muodostaen jälleen vettä, joka vapautuu sivutuotteena ja jälleen yhdistää kaksi monomeeria kovalenttisella sidoksella.

kun ylimääräiset monomeerit liittyvät yhteen useiden dehydraatiosynteesireaktioiden kautta, toistuvien monomeerien ketju alkaa muodostaa polymeeriä. Erityyppiset monomeerit voivat yhdistyä monissa konfiguraatioissa, jolloin syntyy monimuotoinen ryhmä makromolekyylejä. Kolme biologisten makromolekyylien neljästä pääluokasta (kompleksiset hiilihydraatit, nukleiinihapot ja proteiinit) koostuvat monomeereista, jotka liittyvät yhteen dehydraatiosynteesireaktioiden kautta. Kompleksisia hiilihydraatteja muodostuu monosakkarideista, nukleiinihappoja muodostuu mononukleotideista ja proteiineja aminohapoista.
tavassa, jolla monomeerit voivat yhdistyä muodostaen polymeerejä, on suurta vaihtelua. Esimerkiksi glukoosimonomeerit ovat tärkkelyksen, glykogeenin ja selluloosan aineosia. Nämä kolme ovat hiilihydraateiksi luokiteltuja polysakkarideja, jotka ovat muodostuneet glukoosimonomeerien välisten useiden dehydraatiosynteesireaktioiden seurauksena. Kuitenkin tapa, jolla glukoosimonomeerit liittyvät yhteen, erityisesti toisiinsa liittyneiden monomeerien välisten kovalenttisten sidosten sijainnit ja kovalenttisten sidosten orientaatio (stereokemia), johtaa näihin kolmeen eri polysakkaridiin, joilla on vaihtelevia ominaisuuksia ja toimintoja. Nukleiinihapoissa ja proteiineissa monomeereja yhdistävien kovalenttisten sidosten sijainti ja stereokemia eivät vaihtele molekyylistä toiseen, vaan monomeerit (nukleiinihapoissa viisi eri monomeeriä, A, G, C, T ja U mononukleotidit; proteiineissa 21 erilaista aminohappomonomeeriä) yhdistyvät valtavana sekvenssinä. Jokainen proteiini tai nukleiinihappo, jonka sekvenssi on erilainen, on erilainen molekyyli, jolla on erilaiset ominaisuudet.
Leave a Reply