Léčba první linie pro Metastatické Vykastrovat odolné Rakoviny Prostaty
V roce 2019 Prostaty (PCa) představuje téměř 1 v 5 nových diagnóz rakoviny u mužů v USA.1 v posledních několika letech se celková incidence rakoviny prostaty (PCa) snížila přibližně o 7% ročně.1 prudký pokles incidence byl běžně připisován sníženému testování prostatického specifického antigenu (PSA) od roku 2008 do roku 2013. Snížené používání screeningu PSA bylo způsobeno doporučeními pracovní skupiny preventivních služeb Spojených států proti rutinnímu screeningu PSA. To byl D-třídy doporučení speciálně u mužů ve věku 75 let a starší, který byl vyhlášen v roce 2008 a později rozšířeno na všechny muže v roce 2011, vzhledem k rostoucí obavy overdiagnosis a overtreatment.2 i když prevalence testování PSA zastavil klesající a stabilizoval od roku 2013 do 2015,3 efekt screeningu snížení incidence pokročilých onemocnění je stále nejasná. Analýza velkého registru rakoviny pokrývajícího 89% americké populace uvedla, že celkový pokles výskytu PCa ve skutečnosti maskuje nárůst diagnóz ve vzdáleném stádiu od roku 2010 napříč věkem a rasou.4
bez Ohledu na léčbu, přibližně 20%-30% pacientů s lokalizovanou PCa pokrok metastatického onemocnění, které jsou běžně léčeny hormonální terapií.5 To lze podat chirurgickou kastrací (bilaterální orchiektomie) nebo lékařskou kastrací pomocí androgenní deprivační terapie (ADT). Obě metody dosažení vykastrovat hladiny sérového testosteronu, který je považován za standard péče pro léčbu metastatického hormonálně citlivé PCa (mHSPC). Nicméně, mHSPC je předurčen k postupu do metastatického vykastrovat-rezistentní karcinom prostaty (mCRPC).6 vykastrovat-rezistentní karcinom prostaty (CRPC) stav je definován jako progrese onemocnění i přes dosažení vykastrovat hladiny testosteronu (testosteronu v séru < 50 ng/dL nebo 1.7 nmol / L) a může se projevovat buď jako kontinuální vzestup hladin PSA v séru, progrese již existujícího onemocnění a / nebo výskyt nových metastáz.7 CRPC má střední přežití přibližně tři roky8 a je spojeno s významným zhoršením kvality života.9 přesný mechanismus přechodu z mHSPC na mCRPC je stále nejasný. Je však známo, že navzdory kastrátovým hladinám androgenů zůstává androgenní receptor (AR) aktivní a nadále řídí progresi PCa v CRPC.10 to vedlo k vývoji nových činidel zaměřených na další snížení produkce androgenů nebo blokování funkce AR. Existují však i jiné biologické cesty, které fungují nezávisle na androgenní signalizaci a také vedou k CRPC.
k Několika významným posunům došlo v možnosti léčby z mHSPC prostoru, což je značný přínos v přežití (viz „rychle Se vyvíjející řízení strategie metastazujícím Hormon-Senzitivní Rakoviny Prostaty“ odkaz), včetně zavedení chemoterapie v CHAARTED study11 a ÚPRK před soud,12 přidání abirateron acetát a prednison v šíři studii 13 a ÚPRK trial,14 přidání enzalutamide v OBLOUCÍCH trial15 a ENZAMET studie,16 a konečně, přidání apalutamide, orální nesteroidní anti-androgen, což jako enzalutamid se váže přímo na doménu vázající ligand AR a zabraňuje translokaci AR, vazbě DNA a transkripci zprostředkované AR.17 studie TITAN prokázala přínos celkového přežití (OS) u pacientů s mHSPC léčených apalutamidem.18 Apalutamide také prokázala přínos než placebo v non-metastatickým CRPC (nmCRP) nastavení v poli SPARTAN 3. fáze placebem kontrolované studii,19 podobný přínos, který prokázal enzalutamide léčených nonmetastatic vykastrovat-rezistentní karcinom prostaty (nmCRPC) pacientů, v PROSPER trial20 (viz „román ošetření pro non-metastatické vykastrovat-rezistentní karcinom prostaty“ odkaz). Tyto pokroky v léčbě v nastavení mHSPC a nmCRPC vyvolaly otázku, které možnosti léčby by měly být nabízeny pacientům v nastavení mCRPC.21
léčba mužů s CRPC se za posledních 15 let dramaticky změnila. Před rokem 2004, kdy pacienti selhali primární ADT, byla léčba podávána výhradně pro blednutí. Mezník zkoušky Tannock et al.22 a Petrlak et al.23 v roce 2004 byli první, kdo zavedl chemoterapii docetaxelem u pacientů s mCRPC, u nichž bylo prokázáno, že zlepšují jejich přežití. Nicméně, protože docetaxel byl schválen FDA, pět dalších prospěšných látek vykazujících výhodu přežití bylo schváleno FDA na základě randomizovaných klinických studií(tabulka 1). Mezi ně patří enzalutamide, a abirateron, které se konkrétně dotýkají androgenní osy, sipuleucel-T, který stimuluje imunitní systém;24 cabazitaxel, což je další chemoterapeutické činidlo;25 a radium-223, radionuklidové terapie.26 jiné léčby mCRPC ukázaly, že zlepšují výsledky, ale dosud byly schváleny FDA a budou projednány v dalším přezkumu. Vzhledem k výraznému nárůstu v několika FDA-schválené léčebné přípravky u pacientů s CRPC, lékaři jsou vyzváni, s nepřeberné množství možností léčby a množství potenciálních sekvencí těchto látek, aby klinické rozhodování v mCRPC výrazně složitější.
Tabulka 1. Látky, které byly schváleny pro léčbu metastatického vykastrovat-rezistentní rakovinou prostaty v USA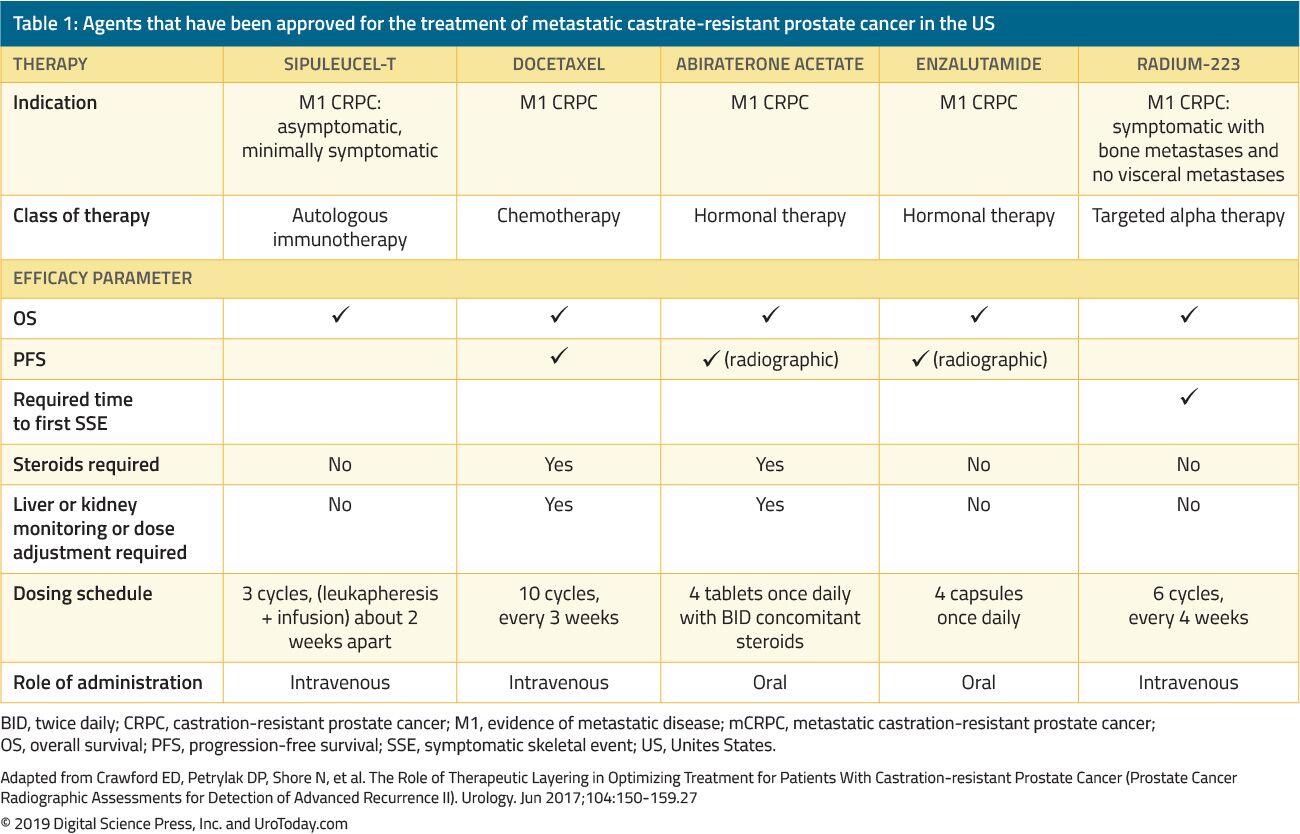
mCRPC je obvykle oslabující onemocnění, a pacienti budou s největší pravděpodobností těžit ze strategie řízení formován multidisciplinární tým složený z urology, onkology, radiační onkology, zdravotní sestry, psychologové a sociální pracovníci.28 při zvažování další systémové léčby, včetně léčby bolesti, zácpy, anorexie, nevolnosti, deprese a únavy, je nezbytné diskutovat o možnostech léčby paliací.
dalším zásadním bodem, který je třeba zvážit při stanovení vhodné sekvence léčby v tomto prostoru onemocnění, jsou související náklady. Pomocí modelů, které zahrnovaly další linie léčby před nebo po docetaxelu, průměrné náklady léčby mCRPC během průměrné období 28.1 měsíců byla přibližně 48.000 dolarů na pacienta.29 Tato cena je poměrně vysoká vzhledem k tomu, že pacienti mohou přijímat více řádků terapie a zvládnutím zdravotnických služeb v průběhu jejich onemocnění.30
Pouze dvě studie prokázaly, že mezní přínos v přežití u pacientů, zbývající na LHRH analogy místo přidání druhé a třetí linii terapie.31, 32 studie ukázaly, že CRPC není rezistentní na ADT, ale spíše přecitlivělý na něj.10 selekční tlak zprostředkovaný léčbou během ADT způsobí, že se AR zesílí a zajistí, že situace nebude eskalovat, ADT se nadále podává v nastavení mCRPC. Léčba zprostředkovaná selekční tlak také pokračuje po celou dobu životnosti nádoru, zesiluje potřebu správně sekvenční terapie. Protože však chybí prospektivní údaje, minimální potenciální přínos pokračující kastrace stále převažuje nad minimálním rizikem této léčby. Kromě toho byly všechny následně schválené léčby studovány u mužů s probíhající ADT, což přidalo další důvod, proč by mělo pokračovat.
než se ponoříme do skutečných dostupných možností léčby, je důležité si uvědomit, že stále není jasné, kdy zahájit léčbu u pacientů s mCRPC, kteří jsou zcela asymptomatičtí. Stále není známo, zda je dřívější léčba lepší, nebo zda bychom měli počkat, až se pacient stane symptomatickým a vyvine bolest. Před zahájením léčby bychom měli zvážit stávající komorbidity pacienta a očekávané nepříznivé účinky zahájení léčby. Pacienti s mCRPC v časném stádiu ve studii COU-AA-302, kteří dostávali abirateron, obvykle přežívali téměř o rok déle než pacienti, kteří dostávali placebo (medián OS, 53,6 měsíce oproti 41,8 měsíce, HR, 0,61; 95% CI, 0,43 až 0,87; p = .006).33 pacienti s mCRPC v rané fázi tedy měli prospěch z dřívějšího zahájení léčby abirateronem. Ve stejné studii u pacientů s asymptomatických nebo mírně symptomatických mCRPC, s výchozí hodnotou PSA < 15.6 ng/mL abirateron také vedlo k rychlejší a vyšší stupeň PSA pokles než placebo.34 ačkoli jsou v současné době dostupné údaje omezené, s největší pravděpodobností naznačují, že zahájení léčby dříve než později je výhodnější.33, 34
Schválena první linii možnosti léčby pro metastazující vykastrovat-rezistentní rakovinou prostaty,
Abirateron
Abirateron je antiandrogen, který je inhibitorem 17α-hydroxylázy/C17,20-lyázy (CYP17) enzymu. Na COU-AA-302 studie fáze III hodnotila abirateron v 1,088 chemo-naivní, asymptomatických nebo mírně symptomatických mCRPC pacientů bez viscerálních metastáz. V této studii byli pacienti randomizováni do abirateron acetát nebo placebo, oboje v kombinaci s prednisone35 (Obrázek 1). Pacienti byli stratifikováni buď podle výkonnostního stavu 0 nebo 1 Eastern Cooperative Oncology Group (ECOG) a asymptomatického nebo mírně symptomatického onemocnění.35 OS a přežití bez radiografické progrese (rPFS) byly koprimárními koncovými body. Soud prokázal, že po medián doby sledování byl 22,2 měsíce, došlo k výraznému zlepšení rPFS v abirateron rameno (medián 16.5 vs. 8.2 měsíců, HR 0.52, p < 0.001). V konečné analýze po mediánu follow-up 49.2 měsíců, OS end-point bylo výrazně pozitivní (34.7 vs. 30.3 měsíce, HR: 0.81, 95% CI: 0.70-0.93, p = 0.0033).36 je důležité si uvědomit, že mCRPC pokrývá široké prognostické spektrum, i když je dosud neléčený chemoterapií.37 v analýze ramene abirateronu ve studii cou-AA-302 měli pacienti, kteří neměli na začátku bolesti, normální hladiny alkalické fosfatázy a LDH a méně než 10 kostních metastáz, medián OS 42,6 měsíce.37 pacienti s více rizikovými faktory progrese však měli významně kratší medián OS.37 Při posuzování toxicity profil abirateron, zdálo se, že poskytují více nežádoucích účinků souvisejících s mineralokortikoidní přebytek a abnormality funkce jater, ale tyto byly většinou třídí 1-2 nežádoucí účinky. Nakonec se ukázalo, že abirateron je stejně účinný u starší populace (> 75 let).38
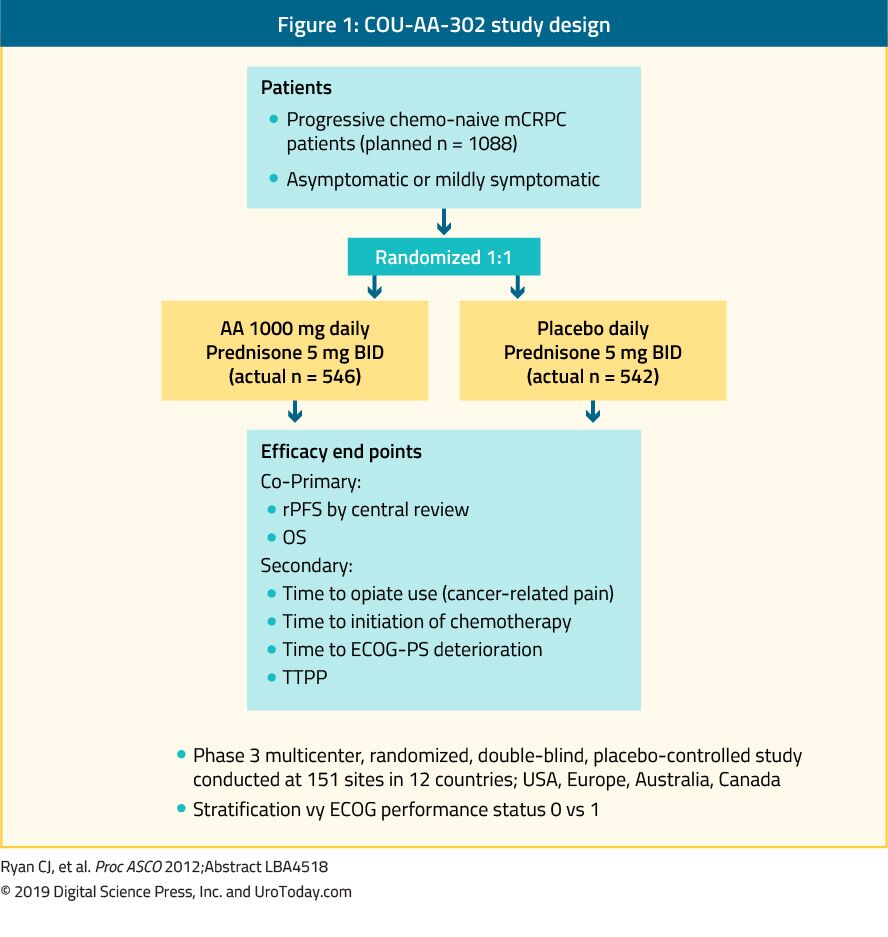
Obrázek 1. COU-AA-302 design studie
enzalutamid
enzalutamid je nesteroidní antiandrogen. Ten PŘEVAŽUJÍ studie, která je randomizovaná fáze III studie zahrnuty 1,717 chemoterapii pacientů s mCRPC pacientů a u pacientů s viscerální metastázy byly způsobilé stejně.39 tato studie srovnávala enzalutamid s placebem (Obrázek 2). Na PŘEVAŽOVAT studie ukázala významné zlepšení v enzalutamide léčených pacientů v obou ko-primární cílové parametry, které zahrnovaly rPFS (HR: 0.186; CI: 0.15-0.23, p < 0.0001) a OS (HR: 0.706; CI: 0.6-0.84, p < 0.001). Rozšířené sledování a konečná analýza potvrdily přínos v OS a rPFS pro enzalutamid.U 40 ze 78% pacientů léčených enzalutamidem bylo hlášeno snížení PSA o více než 50%. Nejčastějšími klinicky relevantními nežádoucími účinky byly únava a hypertenze. Enzalutamid byl také stejně účinný a dobře snášen u starších mužů (> 75 let)41 A u pacientů s viscerálními metastázami nebo bez nich.42 zdálo se však, že u mužů s jaterními metastázami neexistuje žádný zřetelný přínos.43 TERÉN soud ve srovnání enzalutamide s bicalutamid, starší antiandrogen, v randomizované, dvojitě zaslepené studie fáze II, ukazující významné zlepšení v PFS (15.7 months vs. 5.8 months, HR: 0.44, p < 0.0001) in favor of enzalutamide.44
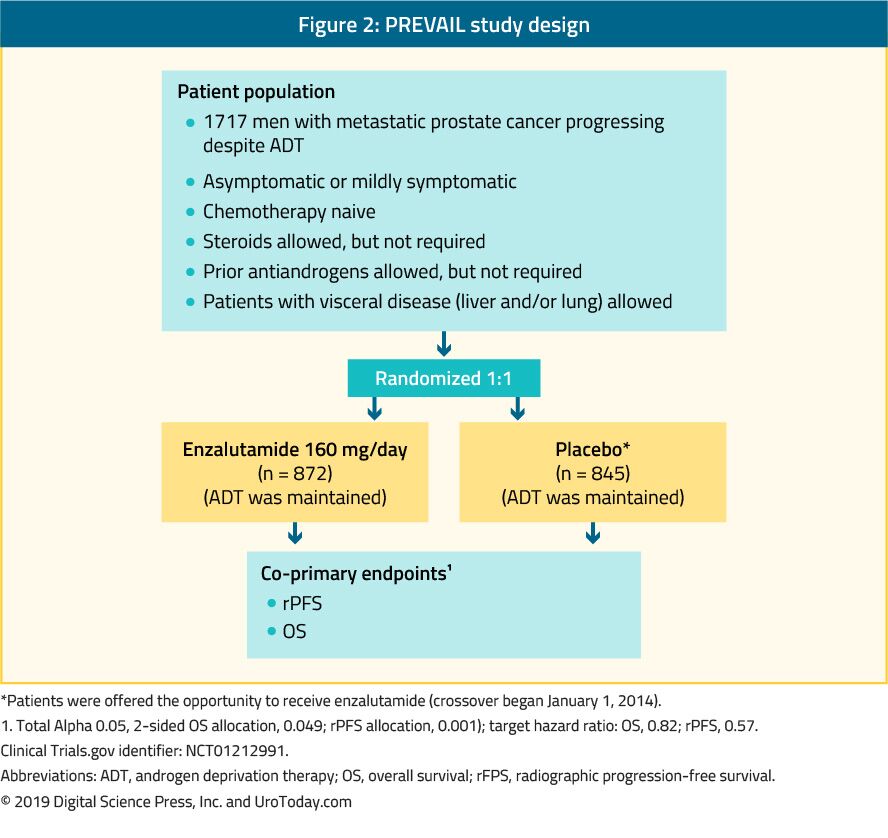
Figure 2. PREVAIL study design
Docetaxel
The landmark trial TAX 327 showed a significant improvement in median OS of 2-2.9 months in mCRPC patients treated with docetaxel-based chemotherapy when compared to patients who were treated with mitoxantrone plus prednisone therapy.22 The SWOG 9916 trial compared mitoxantrone to docetaxel and showed similar results23 (Figure 3). Standardní chemoterapie první linie je docetaxel 75 mg / m2 ve třech týdenních dávkách v kombinaci s prednisonem 5 mg dvakrát denně, až do deseti cyklů. Existuje několik důležitých prognostických faktorů, aby zvážila při podávání docetaxelu: viscerální metastázy, bolesti, anémie (Hb < 13 g/dL), kostní scan progrese, a před estramustin terapie. Tyto prognostické faktory mohou pomoci stratifikovat odpověď na docetaxel. Pomocí těchto prognostických faktorů lze nemoc rozdělit na nízké, střední a vysoké riziko, s významně odlišnými odpovídajícími odhady mediánu OS 25.7, 18, 7 a 12, 8 měsíců.45 ačkoli věk sám o sobě není kontraindikací léčby docetaxelem, pacienti musí být dostatečně fit, aby vydrželi tento typ léčby a komorbidity by měly být hodnoceny před zahájením léčby. U mužů, kteří jsou myšlenka být schopen tolerovat standardní dávkování docetaxelu, tento může být snížena ze 75 na 50 mg/m2 každé dva týdny, což ukazuje nižší stupeň 3-4 nežádoucích účinků a delší čas do selhání léčby.46
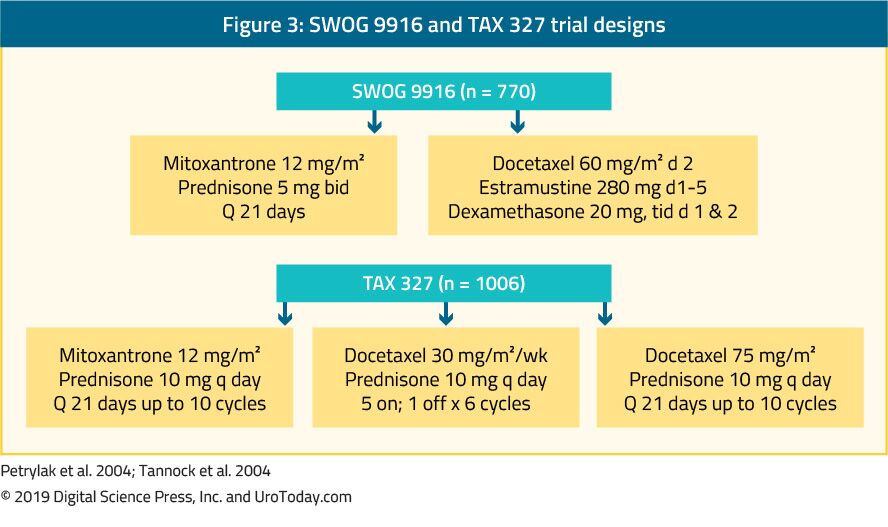
Obrázek 3. SWOG 9916 a DAŇOVÉ 327 zkušební vzory
Sipuleucel-T
Sipuleucel-T, autologní aktivní buněčné imunoterapie, bylo prokázáno, že ve fázi III klinické studie (IMPACT trial), které poskytují přínos v přežití u 512 asymptomatických nebo minimálně symptomatickým mCRPC pacientů, kdy ve srovnání s placebo24 (Obrázek 4). Po mediánu sledování 34 měsíců, medián přežití byl výrazně vyšší v sipuleucel-T (25.8 vs. 21.7 měsíců, s HR 0,78,p = 0.03).24 důležité je, že během léčby nebo po ní nebyl pozorován žádný pokles PSA a PFS byl v obou ramenech podobný. Celková tolerance k sipuleucel-T byla velmi dobrá, většinou se vyskytly nežádoucí účinky stupně 1-2. V současné době je tato léčba dostupná pouze v USA a v Evropě již není k dispozici.
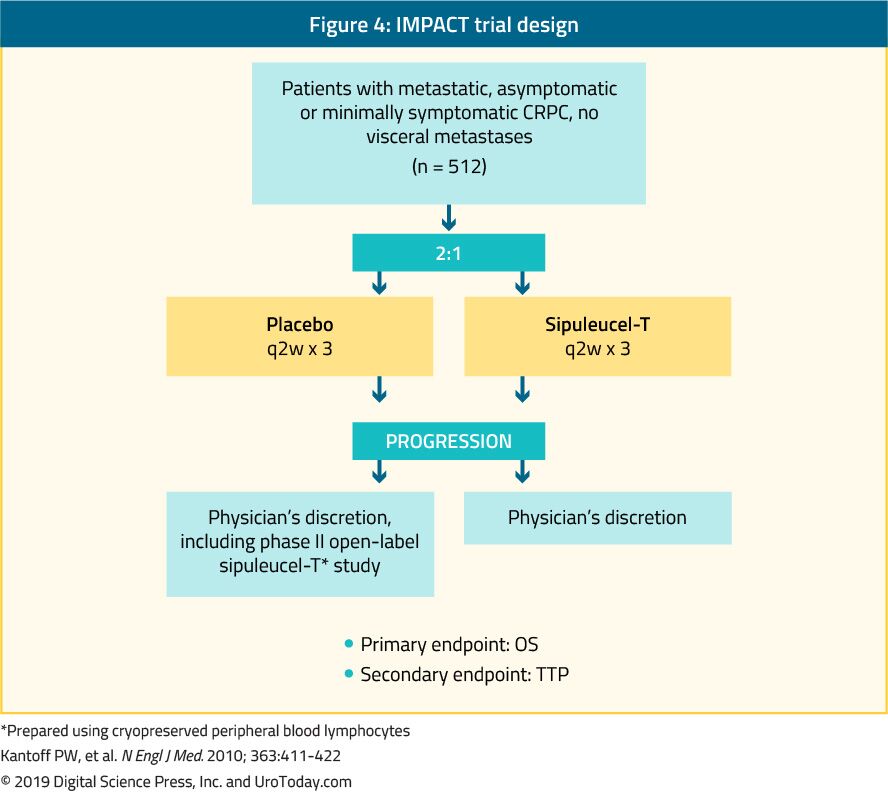
Obrázek 4. IMPACT trial design
závěry
v posledních 15 letech došlo k značnému vědeckému pokroku a investicím do vývoje léků u pacientů s mCRPC. To má za následek schválení FDA několika linií systémových terapií z důvodu zmírnění bolesti, minimalizace nežádoucích účinků onemocnění, a prodloužení OS. K dnešnímu dni je hlášený dopad na OS u pacientů s mCRPC z každého z těchto jednotlivých látek stále mírný, což má za následek přidání pouze několika měsíců. Je nutné zlepšit naše chápání nemoci biologie mCRPC, integrovat komplexní molekulární pochopení kastrace odpor, a analyzovat mechanismy rezistence na současná terapie pro zlepšení budoucího vývoje léčby. Je také důležité investovat a vyvíjet prediktivní biomarkery, které pomáhají při personalizaci terapie. A konečně, na více praktické vědomí, že více dat je potřeba na odpovídající druhou a třetí linii terapie a řazení a kombinace jsou k dispozici léky, které jsou podrobněji popsány v další recenzi článku („Za první linii léčby metastatického vykastrovat-rezistentní karcinom prostaty“).
Datum vydání: 19. listopadu 2019
Leave a Reply