kyselina Šťavelová
Meera Senthilingam
Tento týden se vydáme do Francie a objevte sloučenina, která ovlivnila zdraví velmi dobře známý velitel
Lars Öhrström
první září 1870 byl ponurý den pro Charles Louis Napoléon Bonaparte. Na Sedan, malé francouzské město, blízko Belgických hranic, velitel francouzské armády, Patrice de Mac-Mahon, byl zraněný a nemocný a slabý císař, lépe známý jako Napoléon III, musel vzdát a dát sám sebe jako vězeň nezdolného Pruské duo von Moltke a Bismarck. Takže válka v roce 1870 byla ztracena a mocenská rovnováha Evropy se výrazně naklonila na východ a všichni víme, jak to skončilo.

Zdroj: ©
Sedan, Francie,
Bylo to vše kvůli velké krystalické usazeniny vápníku, oxalátu, která se vytvořila v Napoléon ledviny? Pravděpodobně ne: zdá se, že válka byla prohrána, jakmile byla vyhlášena kvůli pruské technické a organizační nadřazenosti.
císař se však vůbec nechtěl chopit zbraní, přičemž někteří jeho poradci byli hlavními válečníky. Jak dobře byl schopen odolat a působit proti nim, zatímco je sužován velmi bolestivým stavem známým jako ledvinové kameny, je těžké vědět.
je snazší obrátit se na samotné ledvinové kameny, protože jsou náchylné k podrobným metodám vědeckého výslechu, jako je rentgenová difrakce. Jsou tvořeny dvěma jednoduchými složkami, pozitivními ionty vápníku, Ca2+ a negativními oxalátovými ionty, což dává sloučeninu dostatečně známou jednoduše jako oxalát vápenatý.
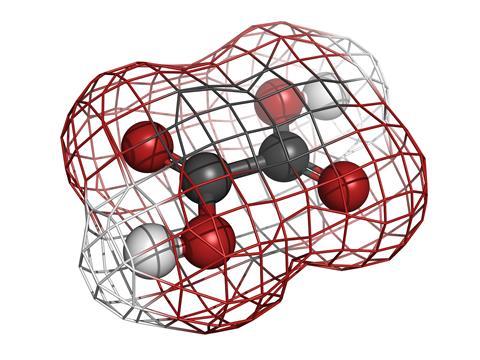
kyselina šťavelová je tématem tohoto podcastu a oxalátové anionty jsou to, co získáte spolu s ionty H+, když rozpustíte krystaly této silné kyseliny ve vodě. Kyselina šťavelová je malá molekula s chemickým vzorcem C2O4H2, ale je možná lepší reprezentován jako HOOC-single-bond-COOH: jen dvě karboxylové skupiny spojené dohromady, aby se to nejjednodušší organické di-kyseliny. Možná víte, tato chemická látka jako látka, která dělá rebarbory mají zvláštní kyselé tang na chuť, ale to je také nalezené v špenát a řadu dalších zeleniny, které většina z nás spokojeně jíst. Je také součástí našeho normálního metabolismu a vyskytuje se zcela přirozeně v našem těle.
Zdroj: ©
je pojmenována po rostlině, běžné dřevo šťovík, malé byliny, jejichž listy mají výraznou kyselou chuť, oživení, pokud se dostanete ztratil v lese, a má latinský název Oxalis acetosella.
Nejvýraznějším rysem této malé molekuly je její tvar. Vypadá to trochu jako dvě Y poskládaná dohromady tím, že se překrývají jejich základny. Atomy uhlíku jsou na dvou průsečících a atomy kyslíku na čtyřech koncích s protony (nebo ionty H+) visícími jeden po druhém na jednom z těchto kyslíků. Navíc je zcela plochý a když ztratil své protony, aby se stal oxalátovým aniontem, má záporné náboje umístěné na dvou atomech kyslíku.
většina technických aplikací kyseliny šťavelové visí na její plochosti a záporném náboji, stejně jako Napoléonovy problémy s ledvinami. V době před bitvou u Sedanu von Moltke úspěšně zapojil francouzskou armádu klasickým hnutím kleští, útočícím spíše ze dvou stran než uprostřed. Stejně tak mají oxalátové ionty dva elektronové páry na každém z negativních atomů kyslíku, které ze dvou stran snadno napadají jakýkoli kovový iont, který mu přijde do cesty. A stejně jako v sedanu budou následovat další oxalátové ionty, obklopující kov dvěma, třemi nebo čtyřmi oxalátovými ionty v závislosti na jeho velikosti.
tento efekt lze použít k odstranění nežádoucích sloučenin železa, zejména rzi, z kuchyňského nádobí a dokonce i mramoru. Jako metaři, kyselina šťavelová nebo oxaláty jsou komponenty v mnoha technických čisticích prostředků a tyto roztoky všechny práce na předpokladu, že kov-oxalátových sloučenin tvoří, jsou rozpustné ve vodě a proto může být snadno smýt.

zdroj: ©
ne tak oxalát vápenatý. Pozitivní ionty vápníku opravdu milují negativnější atomy kyslíku oxalátu a do té míry, že je jim jedno, zda atomy kyslíku oxalátu nesou záporný náboj nebo ne. Takže nejen, že dojde k pohybu kleští vpřed směrem k jednomu iontu vápníku, ale také dozadu, který se připojí k jinému v tomto směru. Jako každý vápenatých iontů je poměrně velký, čtyři oxalátových iontů shromáždí kolem každého kovových iontů (ve srovnání s tři pro železo), každá spojená s dalšími dvěma ionty vápníku v opačném směru. Tímto způsobem oxalát vápenatý poroste do nekonečné sítě, která bude zcela nerozpustná ve vodě. Jak více a více iontů vápníku a oxalátových iontů prochází ledvinami, krystaly budou růst, dokud se stav nestane docela bolestivým.
ale nebuďte znepokojeni, kromě některých velmi zvláštních zdravotních stavů se zdá, že normální nebo dokonce vysoký příjem iontů vápníku a kyseliny šťavelové z přírodních zdrojů nezvyšuje riziko ledvinových kamenů.
nerozpustnost oxalátů se také používá v technologii. Prvky vzácných zemin nebo lanthanoidy jsou v mnoha technických aplikacích stále důležitější. Prvním stupněm jejich zpracování a rafinace je často po počátečním vyluhování z rud vysrážet tyto prvky jako jejich oxaláty, protože stejně jako u oxalátu vápenatého jsou velmi nerozpustné.
na Rozdíl od jeho nešťastné setkání s šťavelanu vápenatého, Napoleon III je známo, že v chemii historie jako iniciátor margarínu rozvoj a tlačí na levný a praktický způsob pro výrobu hliníku v průmyslovém měřítku, ve své době nejdražší ze všech kovů. Neměl vidět později dosáhl cíle, ale je pozoruhodné, že chemické látky, které dal mu tolik bolesti, kyselina šťavelová, se také používá při výrobě a barvení pevný, otěru a korozi vrstva oxidu – také známý jako uv – povlak, který je nyní tak důležité v mnoha našich aplikací hliníku.
Meera Senthilingam
takže zdraví a průmysl se spojily. To byl Lars Öhrström z Chalmers Tekniska Högskola ve Švédsku, který vám přinesl ledvinu oslabující chemii kyseliny šťavelové. Příští týden se Lars vrátí se sloučeninou plně schopnou se chránit.
Lars Öhrström
To je jasné, když ferocenové bylo poprvé provedeno, ale zdá se, že byly zaznamenány jako ‚žlutá kal‘ na konci roku 1940 tím, že proces technici kontroly potrubí v Union Carbide cracker, který byl použit při výrobě malých uhlovodíků cyclopentadiene z dicyklopentadien.
To způsobilo docela rozruch, protože žádný stabilní molekula se skládá pouze z uhlovodíků a přechodných kovů bylo známo dříve, a tato sloučenina může být udržována na vzduchu při pokojové teplotě, aniž by se samovolně vznítit. Přežil také setkání s takovými notoricky známými zabijáky organokovových molekul, jako je voda, kyseliny nebo báze.
Meera Senthilingam
a objevte chemii, která to umožní v chemii příštího týdne ve svém prvku. Do té doby děkuji za poslech, jsem Meera Senthilingam
Leave a Reply