CIMAvax-EGF: nové terapeutické vakcíny pro pokročilé rakoviny plic
ZPRÁVA
CIMAvax-EGF: nové terapeutické vakcíny pro pokročilé rakoviny plic
Gisela González1, Agustin Lage1, Tania Crombet1, Gryssel Rodríguez1, Beatriz García1, Ariadna Cuevas1, Lisel Viña1, Norkis Arteaga1, Elia Neninger2
1Center Molekulární Imunologie, CIMAve. 216 rohu 15, Atabey, Playa, POBox 16 040, Havana, Kuba
2Hermanos Ameijeiras HospitalSan Lázaro # 701 e / Belascoín y Marqués González, Centro Habana, Havana City, Kuba.
abstrakt
jsou uvedeny výsledky umožňující Kubánské regulační agentuře (CECMED) udělit sanitární registraci vakcíně proti rakovině CIMAvax-EGF pro pokročilý nemalobuněčný karcinom plic (NSCLC). Jednalo se o první registraci terapeutické vakcíny na Kubě a také o první registraci vakcíny proti rakovině plic na světě. Proto je pacientům s rakovinou plic nabízena jedinečná terapeutická vakcína, která zvýší přežití a kvalitu jejich života. Za tímto účelem bylo třeba čelit významným předklinickým, klinickým, regulačním, produktivním a vyjednávacím výzvám. Výsledky získané v těchto oblastech vedly k 18 vědecké práce publikované v časopisech s vysokým dopadem a 4 objekty vynálezu, generování několika patentů na Kubě a dalších zemích. V předklinickém prostředí byla u různých druhů zvířat prokázána imunogenita, bezpečnost a protinádorové účinky. Klinická zkušenost začala v roce 1995. Až dosud bylo na Kubě uzavřeno pět klinických studií fáze I-II, dvě fáze II byly také uzavřeny, jedna na Kubě a druhá v Kanadě a Velké Británii a v současné době probíhá na Kubě studie fáze II-III s optimalizovaným harmonogramem a studie fáze III. V oblasti regulace byla navržena a provedena strategie rychlé registrace. K vývoji tohoto jedinečného produktu bylo zapotřebí nových regulačních koncepcí. Byl proveden škálovatelný, reprodukovatelný a kontrolovaný výrobní proces spolu se systémem kvality, který zajistil plnou shodu s GMP. Finanční prostředky na vývoj produktů pocházely z implementace nové strategie vyjednávání: vyjednávání nehmotných aktiv.
Klíčová slova: Rakovina vakcíny, NSCLC, Fast-Track Registrace, CIMAvax-EGF, Fáze II-III Klinické studie
ÚVOD
vztah mezi systémem tvoří receptor pro Epidermální Růstový Faktor (EGFR) a jeho ligandy s rozvojem rakoviny je dobře známý. U nádorů epidermoidního původu existuje nadměrná exprese EGFR, která se týká špatných prognóz a časných relapsů po operaci. Proto se tento systém stal důležitým cílem protinádorových terapií.
mechanismy buněčné proliferace jsou iniciovány vazbou EGF na EGFR. Náš terapeutický přístup spočívá v vakcíně s formulací EGF, která je imunogenní a vyvolává humorální imunitní odpověď. Produkce specifických anti-EGF protilátek, které se vážou na autologní EGF, brání jeho vazbě na EGFR, čímž spouští mechanismy buněčné proliferace odvozené z této interakce (1-4).
zde uvádíme výsledky registrace této vakcíny na Kubě (CIMAvax-EGF). To bylo součástí globální strategie zahrnující nové klinické, regulační, a technologické a obchodní příspěvky, a je podporován 18 mezinárodní vědecké práce a Duševní vlastnictví po celém světě. Popisujeme také inovace v různých oblastech, které umožnily registraci CIMAvax-EGF na Kubě a Peru.
VÝSLEDKY A DISKUSE
Očkování s EFG je bezpečná, imunogenní a zvyšuje přežití s dobrou kvalitou života u pacientů v pokročilých stádiích rakoviny plic
klinické zkušenosti s CIMAvax-EGF v therapeutics of non-small-cell lung cancer (NSCLC) v pokročilých stádiích začal v roce 1995. Až dosud bylo na Kubě uzavřeno pět klinických studií fáze I-II; byly uzavřeny 2 randomizované klinické studie fáze II, jedna na Kubě a druhá v Kanadě a Velké Británii a na Kubě probíhá studie fáze III. Více než 800 pacientů s pokročilým nádorovým onemocněním byly ošetřeny s CIMAvax–EGF, čímž prokazuje, je bezpečná, imunogenní a je schopen zvýšit přežití s dobrou kvalitou života.
hlavním cílem studií fáze I-II bylo rozhodnout o nejlepší formulaci vakcíny (nosný protein a adjuvans), dávce a léčebném schématu. Tyto výsledky prokázaly výhody proteinu P64k jako nosného proteinu a Montanidu ISA51 jako adjuvans. Byla také prokázána zvýšená imunogenita škálování dávky (5-7).
analýza souhrnných údajů ze všech fázi I-II studie ukázala významné zvýšení přežití u pacientů s lepší protilátkové odpovědi nebo dobré protilátek reagujících (GAR), a u pacientů s výraznější pokles v séru koncentrace EGF () vyplývající z očkování. Ve srovnání se souběžnou historickou kontrolou bylo také prokázáno významné zvýšení přežití všech očkovaných pacientů (7).
klinickém hodnocení fáze II byla provedena u 80 pacientů, kteří byli randomizováni do CIMAvax-EGF a nejlepší podpůrná péče (BSC) (40 pacientů) nebo pro léčbu BSC samotnou (40 pacientů), po ukončení první linie chemoterapie. Předchozí zjištění byla potvrzena v tomto pokusu. Přibližně 50% očkovaných pacientů bylo GAR a přežilo významně více než pacienti, kteří nedosáhli klasifikace GAR (kteří byli klasifikováni jako chudí respondéři na protilátky, PAR). Podobně pacienti s největším poklesem přežili významně více než pacienti, kteří toto snížení nevykazovali (Tabulka 1). Byla pozorována významná inverzní korelace mezi titry protilátek proti EGF a, které se vyskytly u očkovaných pacientů, ale ne u kontrol, což prokazuje, že byla způsobena očkováním (Obrázek 1).
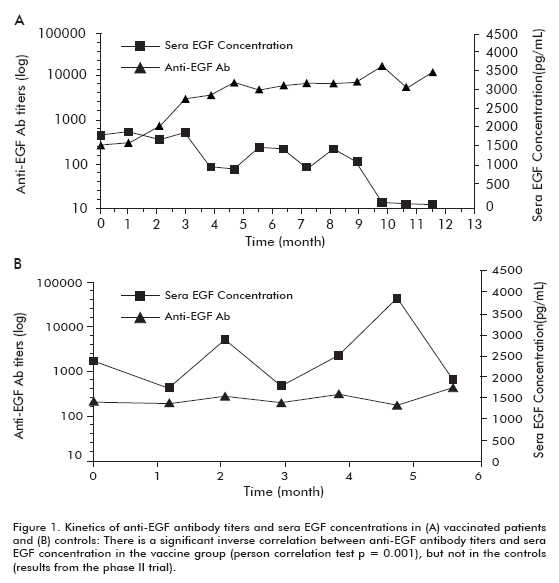
Tam byl zvýšený trend v přežití u všech očkovaných pacientů (18.53 ± 11.47; průměr ± medián), ve srovnání s non-očkovaných kontroly (7.55 ± 5.33), což bylo významné ve skupině pacientů ve věku 60 let nebo mladších (Log rank test; p < 0,05) (Obrázek 2) (8).
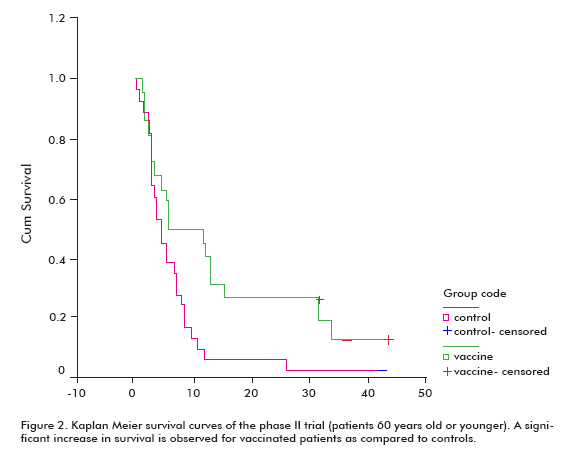
Jak vyplývá z konkurenčního testu in vitro, séra očkovaných pacientů inhibovala vazbu EGF na EGFR. Tato inhibice vazby byla úměrná titrům protilátek a přežití. Séra očkovaných pacientů navíc inhibovala fosforylaci EGFR v poměru k titrům protilátek proti EGF.
bylo studováno preferenční rozpoznání vazebného místa EGF/EGFR (smyčka B molekuly EGF). Pacienti, jejichž séra přednostně rozpoznávají smyčku B, přežili významně více než pacienti, kteří tento epitop nerozpoznali (9).
na Kubě byla nedávno uzavřena studie optimalizace dávky/plánu (fáze I-II). Ve svém návrhu byly zvažovány všechny prvky zvyšující imunogenitu v předchozích studiích, které zahrnovaly: Montanide ISA51 jako adjuvans, zvýšené dávky, čtyři místa vpichu a podání dvou dávek vakcíny před chemoterapií první linie, následované očkováním. Výsledky této studie prokázaly významné zvýšení imunogenity, přičemž 95% GAR dosáhlo desetinásobku předchozích maximálních titrů protilátek. Všechny očkované pa-tienty přežily významně více než kontroly ze studie fáze II (10).
byla také zjištěna zvýšená schopnost sér pacientů inhibovat vazbu EGF/EGFR a fosforylaci EGFR. Na měsíc sedm, po ukončení chemoterapie, protilátková odpověď posunul směrem smyčky B EFG molekuly, což by mohlo naznačovat zlepšení kvality imunitní odpovědi. Výsledky z této studie prokázaly, že existuje prostor pro zlepšení v reakci na CIMAvax-EGF, které může být dosaženo tím, že manipuluje dávku a léčebný plán (10).
výsledky těchto studií jsou validovány ve studii fáze III, která v současné době probíhá na Kubě.
Návrh a realizace regulační strategie pro vakcíny registrace, aby bylo k dispozici pro všechny advanced non-small-cell lung cancer pacientů,
CIMAvax-EGF je terapeutické vakcíny na rakovinu plic, která je ve světě unikátní. Byla navržena a implementována globální strategie; řídila se regulačními požadavky, pro rychlou registraci na Kubě. Blízký vztah mezi zadavatelem (CIM) a Kubánské Regulační Agentury (CECMED) měl účely stanovení požadavků pro získání produktu a jeho rychlé uplatnění ve prospěch pacientů s pokročilým nádorovým onemocněním bez jakékoliv jiné léčebné alternativy. Tato strategie zahrnovala návrh systému jakosti, kontroly kvality a specifikace, jakož i požadavky GMP na pokrytí různých kroků vývoje produktu. Tato globální strategie může být použita při vývoji dalších podobných produktů.
nashromážděné regulační zkušenosti a dokumentace vedly ke schválení klinických studií v různých zemích. Dokumentace obsahující všechny informace umožnila registraci CIMAvax-EGF na Kubě a Peru. Můžeme tedy konstatovat, že máme definovanou strategii pro registraci drog v různých zemích.
GMP výrobní proces, který vytváří produkt, který je škálovatelný, konzistentní a v souladu se specifikacemi,
první výzva navrhnout výrobní proces pro CIMAvax-EGF byla imunogenní EFG přípravy. Byl získán chemickou konjugací lidského rekombinantního EGF s rekombinantním membránovým proteinem P64k (z Neisseria meningitidis). Konjugát se injikuje společně s vhodným adjuvans(v současné době Montanid ISA 51 ze Seppic, Francie).
byl původně navržen proces v laboratorním měřítku. Později byl navržen a implementován škálovatelný (a škálovatelný) sanitární a reprodukovatelný proces v souladu s pokyny GMP. Rovněž byly navrženy a implementovány analytické testy In vitro a in vivo pro hodnocení kvality surovin a meziproduktů a konečných produktů.
všechny změny byly posouzeny a podporovány současnou regulační strategií. Výsledky ze studie ekvivalence, porovnat oba produkty, obdržel schválení CECMED z zmenšen proces aplikace a schválení produktu získaného v tomto procesu pro jeho klinické použití. Škálování a optimalizace výrobního procesu ustoupily publikaci (11) a novému předmětu vynálezu, přičemž patenty byly následně prezentovány v různých zemích.
Jednání o nehmotných nám poskytl finanční prostředky pro rozvoj projektu a také vzdělávací zkušenosti v naší společné práce s regulačními orgány z různých zemí,
Tento Projekt byl vyjednala se zahraničními partnery na základě nové koncepce „jednání o nehmotný majetek“, podporována především prostřednictvím duševního vlastnictví našeho produktu, že bylo ve vývoji. Tato vyjednávání strategie se skládala z licenční projektu pro jeho společný vývoj s ostatními zeměmi, což znamená, že zahraniční protějšky zahrnuty náklady na regulační opatření a klinických studiích na jejich území. V důsledku těchto jednání Kuba obdržela platby za milníky. Tento způsob vyjednávání nám také umožnil neustálou výměnu s odborníky zde i v zahraničí, čímž se zvýšily naše zkušenosti. Naše pozitivní výsledky s touto modalitou vyjednávání by mohly být aplikovány na další produkty, které v naší zemi probíhají.
RELEVANCE studie
CIMAvax-EGF je první terapeutická vakcína pro léčbu rakoviny registrovaná na Kubě a první registrovaná na světě pro léčbu rakoviny plic. Rakovina plic je nevyřešený zdravotní problém s více než 1, 3 miliony případů diagnostikovaných každý rok a stejným počtem úmrtí na celém světě. Na Kubě je to hlavní příčina úmrtí v důsledku rakoviny u obou pohlaví s výskytem více než 4000 zemřelých ročně. Terapie volby pro pacienty diagnostikované v pokročilých stádiích je terapie první linie chemoterapie, která může být podávána souběžně s radioterapií. To je paliativní, non kurativní léčba, s kompletní odpověď na chemoterapii je velmi vzácné, a objektivní odpovědi (úplné nebo částečné), vyskytující se pouze 25% pacientů.
CIMAvax-EGF nabízí alternativní léčbu u těchto pacientů, kteří již podstoupili chemoterapii první linie. Závažné nežádoucí účinky chemoterapie a / nebo radioterapie jsou dobře známy a vážně zhoršují kvalitu života. Místo toho očkování s CIMAvax-EGF generuje pouze mírné nebo středně závažné, spíše než závažné nežádoucí události, které mohou být řešeny s konvenční podpůrné péče, zatímco zlepšení přežití u pokročilé rakoviny plic pacientů a nabízí dobrou kvalitu života.
dosud bylo více než 800 Kubánců léčeno přípravkem CIMAvax-EGF ve více než 20 nemocnicích po celé zemi. Registrace přípravku CIMAvax-EGF umožňuje jeho rozšíření na všechny pacienty v zemi, u kterých byla diagnostikována pokročilá rakovina plic; Kuba se tak stala první zemí na světě s národním programem využívajícím tuto terapeutickou alternativu.
Pokud jde o ekonomické přínosy, prostřednictvím jednání o tomto projektu jsme získali 6.346 milionů USD. Vyjednávací strategie projektu je pro jeho společný vývoj s ostatními zeměmi, což znamená, že zahraniční protějšek pokrývá náklady klinických hodnocení v jejich vlastní zemi, což je cenově dostupné. Tyto zkoušky vyžadují investice ve výši milionů USD, a to je možné pouze tehdy, pokud je podporováno zahraničními protějšky. Současně tato strategie nabízí Kubě více klinických údajů, aniž by zde byly prováděny náklady na provádění zkoušek. Až dosud byly klinické studie prováděny v Kanadě, Velké Británii a Malajsii. V blízké budoucnosti začnou klinické studie v Číně a Evropě.
také v rámci této licenční strategie mají zahraniční protějšky na starosti registraci produktů v regionech, kde mají obchodní práva. Během registračních a marketingových procesů bude Kuba dostávat platby za milníky a později jako prodejní licenční poplatky.
světový trh vakcín proti rakovině je považován za řádově miliardy USD. Skutečnost, že Kuba má jedinečný produkt pro pokročilou léčbu rakoviny plic, nám může poskytnout exportní potenciál, který může financovat použití tohoto produktu v našem národním zdravotnickém systému.
ZÁVĚRY
Očkování s CIMAvax-EGF je bezpečná, imunogenní a vede ke zvýšení přežití s dobrou kvalitou života u pacientů s plicní nádory v pokročilých stádiích. Návrh a implementace regulační strategie pro registraci této vakcíny ji zpřístupnila
pro všechny případy pokročilých pacientů s nemalobuněčným karcinomem plic na Kubě. Tato pozitivní zkušenost by se mohla vztahovat na další podobné probíhající produkty. Byl vyvinut výrobní proces, který byl škálovatelný, konzistentní a reprodukovatelný a splňoval pokyny GMP, aby vytvořil produkt, který vyhovuje specifikacím. Zkušenosti v jednání nehmotného majetku byla velmi pozitivní, a poskytla nám finanční prostředky pro rozvoj projektu, a zároveň podporuje vzdělávací zkušenost odvozena od společné práce s regulačními orgány z různých zemí.
PODĚKOVÁNÍ
autoři chtějí poděkovat následujícím specialisté z Centra Molekulární Imunologie za jejich příspěvek k této práci: Rolando Pérez, Loany Calvo, Suhamy Pozornost, Belinda Sánchez, Irene Městě Beausoleil, Ernesto Chico, Airama Alvisa, Ileana Cartroman, Sergio Ochutnávka, Ana Veloso, Reinaldo Vrána, Yanelda Lopez, Yosniel Hernández, Antonio Vallin, Alejandro Portillo, Liuva Dřeva, Guido Ferrer, Diana Borges, Niuvis Pérez, Tamara García, Idaine Povodí, Mayra Santaelena, Joaquin Solozabal, Aida Rodriguez, Maria Elena Garcia, Addis Torres, Eric Chong, Carmen Roll, Mauricius Catala, Soraida Acosta, Barbara Wilkinson, Olga Torres, Normando Iznaga všechny z nich od Centra Molekulární Imunologie, a také Daniel González, Lourdes B Costa, Galina M Moya, Rolando Páez, Gerardo Guillén, Vivian Pujol , Dinorah Torres z Centra pro Genetické Inženýrství a Biotechnologie.
1. González G, Montero E, León K, Cohen IR, Lage a.autoimunizace na epidermální růstový faktor, součást im-munologického homunkulu. Autoimun Rev 2002; 1: 89-95.
2. Lage a, Crombet T, González G. cílení signalizace receptoru epidermálního růstového faktoru: časné výsledky a budoucí trendy v onkologii. Ann Med 2003; 5 (35): 327-36.
3. González G a Lage a. vakcíny proti rakovině pro hormonální imunitní deprivaci: Přístup k vakcinaci EGF: přední témata ve výzkumu rakoviny, Kapitola 11, vydavatelé Ed Nova, 2007.
4. González G a Lage a. vakcíny proti rakovině pro imunitní deprivaci hormon/růstový faktor: proveditelný přístup k léčbě rakoviny. Curr Cancer Drug Targets 2007; 7: 229-41.
5. González G, Crombet T, Torres F, Catala M, Alfonso L, Osorio M, et al. Vakcína proti rakovině založená na epidermálním růstovém faktoru pro léčbu nemalobuněčného karcinomu plic. Ann Oncol 2003; 14: 461-6.
6. Crombet T, Neninger E, Catalá M, García B, Leonard I, Martínez L, et al. Léčba pacientů s NSCLC vakcínou proti rakovině založenou na EGF. Zpráva o zkoušce fáze I. Rakovina Biol Ther 2006; 5 (2): 136-41.
7. González G, Crombet T, Neninger E, Viada C, Lage a. terapeutické očkování epidermálním růstovým faktorem (EGF) u pokročilého karcinomu plic: analýza shromážděných údajů ze tří klinických studií. Humpolec 2007; 3 (1): 8-13.
8. Neninger E, De la Torre A, Osorio M, Catald M, Bravo I, Mendoza M, et al. Fáze II randomizovaná kontrolovaná studie vakcíny proti epidermálnímu růstovému faktoru u pokročilého nemalobuněčného karcinomu plic. J Clin Oncol 2008; 26: 1452-8.
9. García B, Neninger E, De la Torre A, Leonard I, Martínez R, Viada C, et al. Účinná inhibice vazby epidermálního růstového faktoru / receptoru epidermálního růstového faktoru protilátkami proti Epidermálnímu růstovému faktoru souvisí s lepším přežitím u pokročilých pacientů s nemalobuněčným karcinomem plic léčených vakcínou proti Epidermálnímu růstovému faktoru. Clin Cancer Res 2008; 14 (3): 840-6.
10. Neninger E, Verdecia BG, Crombet T, Viada C, Pereda S, Leonard I, et al. Kombinace vakcíny proti rakovině založené na EGF s chemoterapií u pokročilého nemalobuněčného karcinomu plic. Jaromír Jágr 2009; 32: 92-9.
11. A, A, A, A, A, A, A, A, A, et al. Vývoj výrobního procesu pro vakcínu proti rakovině založenou na epidermálním růstovém faktoru. Bio-pharm Int, Vaccines Suppl, říjen 2008.
Leave a Reply