Řízení Chemoterapie Extravasations
NÁS Pharm. 2009; 34 (9) (onkologická suppl): 3-11.
ABSTRAKT: Intravenózní (IV) chemoterapeutické léky mají potenciál způsobit extravazálního poškození nebo odumření tkáně v místě podání. Přestože většině extravazací lze zabránit správným a důkladným podáním infuze, bylo rozpoznáno a studováno několik antidot, aby se zabránilo dalšímu poškození tkáně.
infiltrace a extravazace jsou dvě dobře známé, odlišné komplikace intravenózní infuzní terapie. Podle společnosti Infusion Nurses Society a Oncology Nursing Society obě komplikace zahrnují neúmyslný únik IV roztoku do okolní tkáně; typ roztoku se však liší. Infiltrace je neúmyslné podání nevesikantního nebo dráždivého roztoku nebo léku do okolních tkání.1,2 Nonvesicants jsou látky, které zřídka vyvolávají akutní reakce nebo ničí tkáň, když infiltrují. Dráždivé látky mohou vyvolat bolest v místě vpichu nebo podél žíly, se zánětlivou reakcí nebo bez ní, obvykle bez trvalého poškození tkáně. Dráždivé látky však mohou způsobit vředy měkkých tkání, pouze pokud je velké množství koncentrovaného roztoku léčiva neúmyslně extravazováno, aby vyvolalo zánětlivé reakce bez trvalého poškození tkáně.3,4
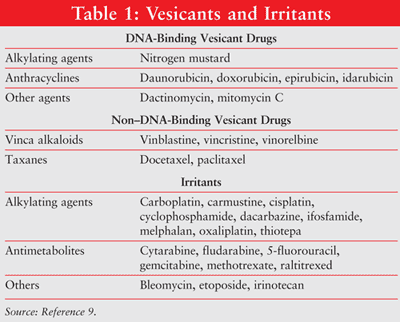
extravazace se týká neúmyslné instilace nebo úniku vezikantního materiálu do perivaskulárních a subkutánních prostorů během podávání léků.1,2 extravazace vede k lokálním reakcím od lokálního podráždění až po těžkou tkáňovou nekrózu kůže, okolní vaskulaturu a podpůrné struktury.5-8 chemoterapeutika mohou být klasifikována na základě jejich potenciálu způsobit lokální poškození tkáně jako vezikanty, dráždivé látky nebo nevesikanty. (Několik vesicants a dráždivých látek jsou uvedeny v TABULCE 1.9) náhodná extravazace IV drogy se vyskytuje v přibližně 0,1% až 6% z periferní IV infuze a 0,3% na 4,7% implantovaný venózní přístup port infuze.10-12
Patofyziologie Poškození Tkání
rozsah poškození tkáně závisí na chemoterapeutické agent má schopnost vázat na DNA. Mezi látky vázající DNA patří antracykliny, protinádorová antibiotika, analogy platiny a některá alkylační činidla.3,4 DNA-binding antineoplastics způsobit poškození tkáně o šíření smrtící DNA síťování nebo zlomů způsobené volnými radikály, které vedou k buněčné apoptózy.13-17 antineoplasty nevázající DNA (např., vinka alkaloidy, taxany, inhibitory topoizomerázy) interferují s mitózou. Látky, které nejsou vázány na DNA, se snadněji odstraňují z míst extravazace a způsobují menší poškození tkáně než činidla vázající DNA.17
rizikové faktory pro extravazaci
rizika pro extravazaci jsou multifaktoriální a jsou do značné míry modifikovatelná. Mnoho z těchto rizik pramení z chyb při používání a umístění zařízení. IV faktory zařízení, které ovlivňují riziko extravazace, zahrnují materiál jehly (tj. kov), Velikost kanyly (velký plast vs. malý plast) a typ katétru(tj. centrální žilní katétr). Kovové jehly mohou způsobit větší poškození při zavedení a jsou nepružné uvnitř cévy, zatímco jehly s velkým rozchodem mohou bránit průtoku krve a zpomalit ředění infuze.18,19 extravazace z CVC může nastat s posunem jehly z implantovaného venózního přístupového portu (IVAP), mechanickou okluzí a následným poškozením CVC, migrací katétru nebo tvorbou fibrinových rukávů a trombózou. Nesprávné umístění IVAP je pravděpodobnější u pacientů s novými zařízeními, u pacientů s významným pooperačním otokem a u obézních pacientů nebo žen s velkými prsy.20 Mechanické okluze může být v důsledku tvorby trombu, lék sraženina, retrográdní posunutí katétru, nebo pinch-off (tj. přerušovaný a poziční katetrizační okluze; to by mělo být podezření, pokud infuze okluze mohou být uvolněn tím, že pacient přesunout své rameno polohování).2,21,22 zamezení extravazace velmi závisí na správné údržbě místa IV a na zajištění správné rychlosti infuze. Tyto rizikové faktory jsou spojeny s antineoplastics používají pacienti a lékaři podávání léku.
Prevence
pečlivé sledování pacientů a vzdělávání pacientů a lékařů o rizicích a řízení zpuchýřující látka extravazace se zdají být základem prevence. Zatímco lékaři nést odpovědnost psaní přesné rozkazy, zdravotní sestry jsou odpovědné za zajištění kvalifikované a správné umístění zařízení a monitorování chemoterapie infuze vizuálně a přes pacienta rozhovory. Během podávání vezikantů by mělo být místo monitorováno na otok, zarudnutí a bolest. Vesikanty by měly být podávány v souladu s doporučeními výrobců (např. správné ředění, stanovená doba podání). IV linie by měly být propláchnuty před a po podání chemoterapie. Úlohou lékárníka by bylo pomoci vyvinout politiky, které zajistí řádné ověřování, označování a vydávání chemoterapeutických látek. Jeden způsob, jak by to mohlo být popraven, je použití diskriminační označení, když výdej zpuchýřující látka antineoplastics tak, že sestry používat příslušná preventivní opatření. Lékárníci mohou hrát nedílnou roli ve vzdělávání tím, že poskytuje informace o drogách a rutina v-služby pro všechny členy zdravotnického týmu o správném používání a správu různých chemoterapeutik. Aby bylo zajištěno provádění bezpečných postupů, je třeba přijmout multidisciplinární přístup založený na spolupráci. Podávání chemoterapie u pacientů vyžaduje řádné školení zaměstnanců a vzdělávání pacientů a administrativní podporu prostřednictvím realizace politiky.2,23
dokumentace událostí
každý případ extravazace musí být důkladně zdokumentován a ohlášen. Dokumentace slouží několika účelům, včetně poskytují přesný popis toho, co se stalo, ochrana zdravotnických pracovníků podílejících, shromažďování informací o extravasations, a zvýraznění deficity v praxi.23 dokumentace a podávání zpráv příslušným subjektům o nežádoucích účincích na léky a chybách v medikaci je dalším způsobem, jak lékárníci mohou pomoci předcházet budoucím událostem. Údaje získané z hlášených nežádoucích účinků a chyb v medikaci může být použit jako výukové nástroje zkoumat systémově prostředky, které tyto události nastat. Místní postupy a protokoly jsou rozhodující pro včasné rozpoznání a řízení extravazace a prevenci vážného poškození tkáně. Společné úsilí by mělo být provedeno s cílem zajistit včasné multidisciplinární pokusy vzdělávat všech členů zdravotnického týmu podílejících se na řízení těchto pacientů, jakmile událost nastala. Je třeba vyvinout další úsilí k zahájení politik, které by zabránily dalším událostem. Pokud jsou zásady zavedeny, měly by být snadno dostupné a pravidelně aktualizovány tak, aby odrážely současné postupy. Evropská onkologická Ošetřovatelská společnost (EONS) 2007 pokyny pro extravazaci poskytují navrhované údaje a šablony, které mohou být použity ke shromažďování informací v případě případu.23
Známky a Příznaky Extravazace
Známky a příznaky zpuchýřující látka extravazace zahrnují otok, zarudnutí a/nebo nepříjemné pocity, které jsou často popisované jako pálení nebo píchání. Odpor při podání léku, pomalý nebo stagnující infuze, a nedostatek nebo ztráta z návratu krve z kanyly IV, implantovaný port, nebo jiné centrální venózní přístupové zařízení mohou být ukazatele, které zpuchýřující látka extravazaci dochází.23 změna barvy a indurace kůže mohou dále postupovat s vývojem puchýřů nebo nekrózy a případně ulcerace a hlubokého poškození tkáně. Může trvat několik dní, než bude realizován plný rozsah poškození epitelu.
Léčba Chemoterapií Indukované Extravazace
léčebné postupy, které jsou využity pro řízení zpuchýřující látka extravazace zahrnovaly okamžité přerušení chemoterapie a chlazení nebo ředění místě extravazace. Pro snížení morbidity spojené s extravazací je nezbytné, aby lékaři byli dobře informováni o dostupných léčbách a pracovali rychle, aby se vyhnuli dalšímu poškození pacienta. Léčba nevesikantní extravazace obvykle zahrnuje zvýšení končetiny a ochlazení a obvykle nezahrnuje použití farmakologické terapie.23
Počáteční Řízení zpuchýřující látka Extravazace
Jednoduchost při poskytování rané intervence může být usnadněno tím, že k extravazaci kit k dispozici v rámci instituce. Většina extravazace sady obsahují jednorázové stříkačky a kanyly, studené-teplé zábaly, gázy, náplasti, sterilní a ochranné rukavice, a léky k léčbě extravazace (např. hyaluronidáza, dimethyl sulfoxidu 99%, dexrazoxan). Seznam obsahu soupravy by měl být umístěn v soupravě a pravidelné ověřování obsahu léku s aktualizovanými daty exspirace by měl pravidelně udržovat lékárník.2
Jednou puchýřotvorné dojde k extravazaci, lékař by měl okamžitě zastavit infuzi; nicméně, kanyly nebo noncoring port jehly by měly být uchovávány v místě a pokus odsajte zpuchýřující látka s 10 mL injekční stříkačka by měla být provedena. Oblast extravazace by měla být označena a vyfotografována; poté by měla být odstraněna kanyla nebo jehla a měl by být informován lékař. Pacienti mohou vyžadovat použití analgetik, aby pomohli zvládnout bolest, kterou mohou zažít. Jakmile byla přijata počáteční opatření, je velmi důležité důkladně zdokumentovat nežádoucí účinek a / nebo chybu v medikaci, ke které došlo.23
pro vinka alkaloidy, kde je indikováno rozptýlení nebo ředění vezikantu, aplikujte lokální teplo po dobu 20 minut 4krát denně po dobu 1 po dobu 2 dnů. Pro jiné zpuchýřující látka extravasations, včetně antracyklinů, počáteční léčba je zaměřena na lokalizaci a neutralizuje extravasated agent s studené obklady po dobu 20 minut 4 krát denně po dobu 1 až 2 dnů, omezení buněčné vychytávání těchto látek.23
Farmakologické Léčby
DMSO: DMSO je běžné rozpouštědlo, které proniká tkání a zvyšuje propustnost kůže, která může usnadnit absorpci z extravasated drog. Když se aplikuje lokálně, to má volný radikální úklidu/anti oxidační vlastnosti, které mohou urychlit odstranění extravasated drog. DMSO (Rimso-50) je k dispozici pouze pro maloobchodní nákup ve Spojených státech v 50% (obj./obj.) roztoku ve vodě. Toto řešení je schváleno FDA pouze pro léčbu recidivující intersticiální cystitidy.24 účinnost DMSO při léčbě extravazace chemoterapií byla poprvé popsána v několika kazuistikách a malých klinických studiích.
V jednom případě, 10 mg daunorubicin extravazace v 42-rok-starý muž byl ošetřen s hydrogenuhličitan sodný, dexametazonu (4 mg), ledové zábaly, a 1,5 mL lokální DMSO 70%, což bylo aplikováno každé 3 až 4 hodin po dobu 10 dnů. Tento režim poskytoval úlevu od bolesti a prevenci vředů.25
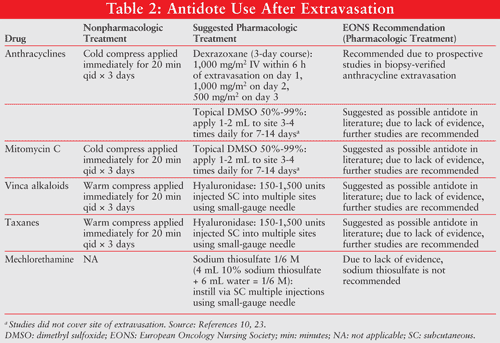
Olver a Schwarz uvedli tři případy extravazačního rozlišení s použitím DMSO.26 V jednom případě denní aplikace DMSO 99% po dobu 14 dnů vedla k úplnému vymizení bolesti během 2 dnů bez ulcerace u pacienta s extravazací doxorubicinu. Pacient také dostal 8,4% hydrogenuhličitanu sodného a odpovídající nefarmakologickou léčbu. (Viz tabulka 2 pro nefarmakologické možnosti.) V jiném případě byl 49letý muž, který dostával 4 až 6 mg doxorubicinu, léčen pro extravazaci doxorubicinu 5 mL 8.4% hydrogenuhličitan sodný, ledové obaly a DMSO 99% aplikované denně po dobu 14 dnů. Ulcerace nenastala, nicméně došlo k prodloužení lokte o velikosti 3 x 2,5 cm.26 Ve třetím případě, lokální aplikace DMSO 99% (každých 6 hodin po dobu 1 týdne, pak dvakrát denně na další týden) zabránit vředy; nicméně, reziduální pigmentace zůstal.26
Berghammer et al také hlásili případ extravazace docetaxelu.27 extravazát byl naředěn normálním (0,9%) fyziologickým roztokem a ošetřen ledovými obaly. DMSO byl aplikován 3krát každých 45 minut a perorální kortikosteroidy a diklofenak byly podány v den extravazace. Všechny příznaky vymizely během 24 hodin; avšak opožděné příznaky (hnědé zabarvení, hyperplazie kůže) se objevily 5. den a poté se zvýšily. Nebyl nutný žádný plastický chirurgický zákrok. Přestože DMSO v kombinaci s hypotermií a izotonickým fyziologickým roztokem nebyl účinný při prevenci opožděných příznaků, omezil zánět a nekrózu tkání.
Ludwig et al uvádí, že použití DMSO 90% a alfa-tokoferol 10% směsi do 48 hodin po extravasations antracyklinů nebo mitomycin C u 8 pacientů mělo za následek žádné kožní ulcerace nebo funkční nebo neurovaskulární poškození.28 alfa-tokoferol bohužel není snadno dostupným léčivým přípravkem a k ověření jeho použití by měly být provedeny další randomizované studie.
v prospektivní studii 20 pacientů s antracyklinovými extravazacemi byl DMSO 99% podáván dvakrát, 6krát denně po dobu 2 týdnů.29 po léčbě DMSO nebyly popsány žádné vředy, ačkoli počáteční otok (85%), erytém (75%) a bolest (60%) byly patrné. Po 3měsíčním sledování u 16 pacientů nemělo 6 (38%) pacientů žádné zjevné příznaky a 10 (63%) mělo pigmentované indurace. Bertelli také provedl prospektivní studii hodnotící účinky DMSO na antracyklinové extravazace.30 doxorubicinu představovalo 11 případů a epirubicin 46 případů. Pacienti byli léčeni DMSO 99% každých 8 hodin po dobu 7 dnů. Sedmdesát procent pacientů (40/57) měl kompletní řešení extravazace do 1 týdne, jeden pacient měl reziduální, měkké tkáně otok, a jeden pacient měl zbytkové hyperpigmentace.
v těchto kazuistikách a malých studiích byly extravazace diagnostikovány klinicky, nikoli biopsií. DMSO může být možnost pro léčbu extravasated antracykliny, mitomycin C, a aktinomycin D. doporučuje se, že tenká vrstva DMSO být aplikován na extravasated oblasti a nechá zaschnout. Neokluzivní obvaz by měl být aplikován během 10 až 25 minut. Tyto kroky by se měly opakovat každých 8 hodin po dobu 7 dnů.23 přestože byl DMSO v praxi používán jako možnost léčby, nedostatek prospektivních studií může omezit jeho použití. Pokyny pro extravazaci EONS 2007 doporučují provést další studie; DMSO 50% až 99% však může být zváženo pro použití podle uvážení klinického lékaře.23 je důležité si uvědomit, že žádná z prospektivních studií DMSO nepoužila obvaz, aby umožnila pokožce plně absorbovat DMSO.
hyaluronidáza: Předpokládá se, že hyaluronidáza je schopna rozkládat extracelulární matrici, která je základem epiteliálních buněk. Matrice drží velké množství molekul vody a po jejím rozpadu je schopna uvolnit tekutinu do extracelulárního prostředí. V případě extravazace umožňuje zvýšení tekutiny na místo, čímž se zředí skutečná koncentrace pokožky v místě kontaktu.31,32 hyaluronidáza byla použita pro léčbu vinka alkaloidů a taxanových extravazací.Bylo použito 33 dávek hyaluronidázy v rozmezí od 150 do 1 500 jednotek zředěných v 1 mL normálního fyziologického roztoku subkutánně nebo intradermálně do 1 hodiny po extravazaci.
V malé klinické studie 6 pacientů s vinblastin (n = 1), vinkristin (n = 1) a vinorelbin (n = 4) extravazace, 250 jednotek hyaluronidáza byly injikovány do centrálního žilního katetru, nebo subkutánně (6 injekcí) v případě zranění. Nebyly aplikovány žádné steroidy ani studené balíčky. Bolest ustoupila během několika dní po léčbě hyaluronidázou u všech pacientů. Jeden pacient si stěžoval na mírně bolestivou induraci 3 měsíce po extravazaci vinkristinu.30 tyto zprávy odhalují slibné informace; stále však existuje celkový nedostatek důkazů pro použití hyaluronidázy k léčbě extravazací alkaloidů vinca. Musí být provedeno více prospektivních studií. Pokyny pro extravazaci EONS 2007 doporučují provést další studie; hyaluronidáza však může být považována za možnost v doporučených dávkách podle uvážení lékaře.23
thiosíran sodný: Thiosíran sodný zabraňuje alkylaci a destrukci tkáně tím, že poskytuje substrát pro alkylaci v podkožní tkáni. Thiosíran sodný má bylo prokázáno, že být účinné při pokusech na zvířatech a v jednom případě zpráva pro léčbu mechlorethamine (dusík hořčice) extravazace.33,34 doporučená dávka je 2 mL 0,17 M (roztok 4 mL 10% thiosíranu sodného a 6 mL sterilní vody na injekci). Vzhledem k nedostatku důkazů pokyny pro extravazaci EONS 2007 toto nedoporučují jako antidotum.22
Dexrazoxan: Dexrazoxan (Totect) byl nedávno schválen FDA pro léčbu antracyklinem indukovaných extravazací. Dexrazoxan má dvojí mechanismus účinku: 1) působí jako železo chelatační látka, brání tvorbě iron-antracyklinových komplexech a železo-zprostředkované hydroxylové radikály, které způsobují oxidační poškození; a 2) stabilizuje topoizomerázy II a dělá to nedostupné antracyklinové chemoterapie. Dexrazoxan blokuje enzym tak, že již není ovlivněn antracyklinem a zabraňuje poškození zdravých buněk v tkáni.35
účinnost dexrazoxanu byla prokázána ve dvou klinických studiích prováděných v Evropě.36 obě studie byly prospektivní, otevřené, jednoramenné, multicentrické klinické studie provedené od července 2001 do srpna 2005, do kterých bylo zařazeno celkem 80 pacientů. Do první studie byli zařazeni pacienti ze 17 nádorových míst v Dánsku a do druhé studie byli zařazeni pacienti ze 34 nádorových míst v Dánsku, Německu, Itálii a Nizozemsku. Antracyklinové extravazace byla diagnostikována a potvrzena pomocí fluorescenční mikroskopie biopsii tkáně odebrané během 6 hodin dexrazoxanu. K prokázání 70% nebo většího snížení incidence chirurgického zákroku byla vyžadována velikost vzorku 32 hodnotitelných pacientů (jednostranný binomický test, a = .025, ß = .20). Primárním koncovým bodem byla rychlost chirurgické resekce a nekrózy. Padesát čtyři z 80 pacientů (studie 1: n = 18; studie 2: n = 36) byla hodnocena (n = 13 negativní biopsie; n = 4 ne biopsie provedena; n = 8 protokolu porušení), s průměrným věkem 56 let (rozmezí 34-81 let). Šedesát devět procent (n = 37) hodnocených pacientů byly ženy. Dexrazoxan byl podáván jako intravenózní infuze po dobu 1 až 2 hodin; 1 000 mg / m2 během 6 hodin; 1 000 mg / m2 po 24 hodinách; a 500 mg / m2 po 48 hodinách extravazace.36
Pacientů byla hodnocena účinnost a bezpečnost ve dnech 7, 14, 21, a 28, a na účinnosti v den 90.36 nejčastější rakovinou diagnóza byla rakovina prsu (50%), následuje lymfom (39%) a jiné typy rakoviny (9%). U pacientů došlo k extravazacím doxorubicinu (n = 23) nebo epirubicinu (n = 31). Průměrná plocha extravazace byla 23,6 cm2 ve studii 1 a 39 cm2 ve studii 2. Jedenáct pacientů mělo oblasti extravazace větší než 75 cm2. Tam byly žádné incidenty operaci ve studii 1 a 1 událost (2.8%, 95% CI 0.1%-14.5%) ve studii 2. Pacient, u kterého se vyvinula tkáňová nekróza způsobená extravazací, měl velmi velkou plochu extravazace doxorubicinu o rozměrech 253 cm2. Příznaky se zvýšily ve dnech po extravazaci, tkáňová nekróza se začala objevovat 9 dní po extravazaci pacienta a nekróza byla chirurgicky vyříznuta. Ve studii 1 došlo k 1 (5, 6%) incidentu nekrózy v důsledku biopsie, 6 (33.3%) případy odložení nebo zrušení plánované léčby rakoviny a 9 (50%) hospitalizací v důsledku extravazace. Ve studii 2 došlo k 1 (2.8%) incident nekrózy v důsledku extravazace, 3 (8.3%) případy nekrózy vzhledem k biopsii, 10 (27.8%) případů odklady nebo zrušení plánované léčby rakoviny vzhledem k extravazaci, a 13 (36.1%) případů hospitalizace v důsledku extravazace. Na 3-měsíční follow-up, 88.9% (n = 16) neměl žádné negativní následky ve studii 1 a 63.9% (n = 23) ve studii 2. Patnáct z 80 pacientů smyslové poruchy (n = 9), kožní atrofie (n = 5), bolest (n = 10), znetvoření (n = 1), a omezení (n = 3). Většina pacientů (71%) byla schopna podstoupit další chemoterapeutickou léčbu podle plánu.
mezi nejčastější nežádoucí účinky zahrnovaly snížení bílých krvinek (72.5%), pokles hemoglobinu (42.5%), snížení počtu krevních destiček (26%), zvýšení aspartátaminotransferázy (36.8%), zvýšení alaninaminotransferázy (23.9%), reakce v místě vpichu (27.5%) a nevolnost (18.8%).36 výsledky klinických studií ukázaly, že dexrazoxan je účinným činidlem pro léčbu akutních antracyklinových extravazací a prevenci opožděných příznaků.
souhrn těchto léčebných doporučení, včetně pokynů EONS 2007, je uveden v tabulce 2.
Role Lékárníka
Lékárníci by měli být úzce zapojeni do hodnocení a řízení všech chemoterapií indukované extravasations. Mohou hrát nedílnou roli několika způsoby, včetně: 1) rozvoj politiky a protokoly; 2) pacient, rodina a multidisciplinární vzdělávání; 3) dokumentace a hlášení extravasations a jiné nežádoucí reakce po terapii; a 4) sledování správné dávkování, podávání a účinnost léčby.
Závěr
Všechny studie přezkoumána zapojených dospělých, tak pediatrických pacientů by měl zvýšené riziko míchání a tahání čar. K dnešnímu dni, dexrazoxan je pouze extravazace agent, který byl zkoumán ve velké, multicentrické, prospektivní studie, které používají objektivní, spolehlivé testování k diagnostice extravazace případech; to poskytuje silný důkaz dexrazoxan je nástroj. Přes jejich běžné použití v praxi, jiné farmakologické léčby, jako je DMSO a hyaluronidáza, nebyly rozsáhle studovány; proto chybí doporučení založená na důkazech. Řízení extravazace by mělo být prováděno podle uvážení klinického lékaře ve spolupráci se všemi členy týmu zdravotní péče.
1. Společnost Infuzních Sester. Infuzní ošetřovatelské standardy praxe. J. 2006; 29 (suppl 1): S1-S92.
2. Polovič M, White J, Kelleher L. pokyny pro chemoterapii a bioterapii a doporučení pro praxi. 2.vydání. Pittsburgh, PA: onkologická Ošetřovatelská společnost; 2005.
3. Ener RA, Meglathery SB, Styler m. extravazace systémových hematoonkologických terapií. Ann Oncol. 2004;15:858-862.
4. Sauerland C, Egelking C, Wickman R, Corbi D. Vesicant extravazace část I: mechanismy, patogeneze, a ošetřovatelská péče ke snížení rizika. Oncol Nurs Fórum. 2006;33:1134-1141.
5. Cassagnol M, Cohen H. Dermatologic toxicities of chemotherapeutic agents. US Pharm. 2008;33(1)(Oncology suppl):10-20.
6. Schulmeister L. Extravasation management. Semin Oncol Nurs. 2007;23:184-190.
7. Viale P. Chemotherapy and cutaneous toxicities: implications for oncology nurses. Semin Oncol Nurs. 2006;22:144-151.
8. Cox K, Stuart-Harris R, Abdini G, et al. The management of cytotoxic-drug extravasation: guide-lines drawn up by a working party for the Clinical Oncological Society of Australia. Med J Aust. 1988;148:185-189.
9. Schrijvers DL. Extravasation: obávaná komplikace chemoterapie. Ann Oncol. 2003; 14 (suppl 3): iii26-iii30.
10. Národní Extravazační Informační Služba. www.extravasation.org.uk/home.html, přístup k 25. březnu 2009.
11. Lemmers N, Gels M, Sleijfer D, et al. Komplikace žilních přístupových portů u 132 pacientů s diseminovaným karcinomem varlat léčených polychemoterapií. J Clin Oncol. 1996;14:2916-2922.
12. Shetty PC, Mody MK, Kastan DJ. Výsledek 350 implantovaných hrudních portů umístěných intervenčními radiology. J Vasc Interviol. 1997;8:991-995.
13. Dorr RT. Antidota k extravazacím vezikantní chemoterapie. Krev Rev. 1990; 4: 41-60.
14. Langer SW, Sehested M, Jensen PB. Léčba antracyklinové extravazace dexrazoxanem. Clin Cancer Res. 2000; 6: 3680-3686.
15. Raymond E, Faivre S, Woynarowski JM, Chaney SG. Oxaliplatina: mechanismus účinku a antineoplastická aktivita. Semin Onkol. 1998; 2 (suppl 5): 4-12.
16. Rivory LP. Nové léky na kolorektální karcinom-mechanismy působení. Rakušan. 2002;25:108-110. www.australianprescriber.com/magazine/25/5/108/10/. přístup k 25. březnu 2009.
17. Skeel RT. příručka chemoterapie rakoviny. 5.vydání. New York, NY: Lippincott Williams & Wilkins; 1999.
18. Boyle DM, Engelking C. Vesicant extravazace: mýty a reality. Oncol Nurs Fórum. 1995;22:57-67.
19. Hadaway LC. Prevence a řízení periferní extravazace. Ošetřovatelství. 2004;34:66-67.
20. Shulmeister L, Camp-Sorrell D. extravazace chemoterapie z implantovaných portů. Oncol Nurs Fórum. 2000;27:531-538.
21. Debety JM, Wils JA, Schlangen JT. Vzácná komplikace implantovaných zařízení pro centrální žilní přístup: zlomenina katétru a embolizace. Podpora Rakoviny Péče. 1995;3:432-434.
22. Gorski LA. Okluze centrálního žilního přístupu. Část 2: Netrombotické příčiny a léčba. Domácí Zdravotní Sestra. 2003;21:168-171.
23. Extravazační pokyny 2007. Evropská Onkologická Ošetřovatelská Společnost. www.cancerworld.org/CancerWorld/getStaticModFile.aspx?id=2340, přístup k 25. březnu 2009.
24. Příbalová informace Rimso-50 (dimethylsulfoxid). Lake Forest, IL: Bioniche Pharma USA LLC; 2009.
25. Lawrence HJ, Dobrou noc SH. Dimethylsulfoxid omezující poškození tkáně způsobené extravazací doxorubicinových látek. Ann Intern Med. 1983;98:1025.
26. Olver dovnitř, Schwarz MA. Use of dimethyl sulfoxide in limiting tissue damage caused by extravasation of doxorubicin . Cancer Treat Rep. 1983;67:407-408.
27. Berghammer P, Pohnl R, Baur M, Dittrich C. Docetaxel extravasation. Support Care Cancer. 2001;9:131-134.
28. Ludwig CU, Stoll HR, Obrist R, Obrecht JP. Prevention of cytotoxic drug-induced skin ulcers with dimethyl sulfoxide (DMSO) and alpha-tocopherole. Eur J Cancer Clin Oncol. 1987;23:327-329.
29. Olver IN, Aisner J, Hament A, et al. A prospective study of topical dimethyl sulfoxide for treating anthracycline extravasation. J Clin Oncol.1988;6:1732-1735.
30. Bertelli G. Prevention and management of extravasation of cytotoxic drugs. Drug Saf. 1995;12:245-255.
31. Balazs EA, Laurent TC, Jeanloz RW. Nomenclature of hyaluronic acid. Biochem J. 1986;235:903.
32. Girish KS, Kemparaju K. The magic glue hyaluronan and its eraser hyaluronidase. Life Sci. 2007;80:1921-1943.
33. Dorr T. Antidotes to vesicant chemotherapy extravasations. Blood Rev. 1990;4:41-60.
34. Owen OE, Dellatorre DL, Van Scott EJ, Cohen MR. Accidental intramuscular injection of mechlorethamine. Cancer. 1980;45:2225-2226.
35. Totect (dexrazoxane for injection) package insert. Copenhagen, Denmark: TopoTarget A/S; October 2007.
36. Mouridsen HT, Langer SW, Buter J, et al. Treatment of anthracycline extravasation with Savene (dexrazoxane). Results from two prospective clinical multicenter studies. Ann Oncol. 2007;18:546-550.
Leave a Reply